文献DOI:10.1212/NXI.0000000000000374
文献PMID:28680916
文献原文链接:https://sci-hub.se/10.1212/NXI.0000000000000374
Lipoic acid in secondary progressive MS:A randomized controlled pilot trial
硫辛酸治疗继发性进行性MS--一项随机对照试验
摘要:
目的:确定硫辛酸(LA)是一种内源性抗氧化剂,是否能减缓全脑萎缩率,并且在继发进展型MS(SPMS)中是安全的。
方法:40-70岁SPMS患者参加单中心、2年、双盲、随机试验,每日口服1,200 mg LA与安慰剂。主要结果是年度变化脑容量(PCBV)的变化。次要结果是分割的脑、脊髓和视网膜下结构萎缩率、残疾、生活质量和安全性的变化。意向治疗分析使用线性混合模型。
结果:参与发生在2011年5月2日和2015年8月14日之间.LLA(n = 27)和安慰剂(n = 24)的研究组匹配平均年龄为58.5(标准差5.9)年,61%女性,平均疾病持续时间年龄为29.6(标准差9.5),中位数扩展残疾状况评分为6.0(四分位数范围1.75)。 2年后,与安慰剂相比,LA组的年化PCBV显著降低(20.21 [系数估计的标准误差(SEE)0.14] vs 20.65 [SEE 0.10],95%置信区间[CI] 0.157-0.727,p=0.002)。 LA中改进的定时25英尺步行几乎但没有明显好于对照组(20.535 [SEE 0.358] vs 0.137 [SEE 0.247],95%CI 21.37 to 0.03,p = 0.06)。 LA患者出现明显更多的胃肠道不适和跌倒更少。 LA队列中发生意外的肾功能衰竭(n = 1)和肾小球肾炎(n = 1)。通过药丸计数测量的依从性为87%。
结论:LA显示年度PCBV减少68%,并表明SPMS具有临床益处,同时在2年内保持良好的安全性,耐受性和依从性。
全文介绍:
到了20年,大多数患有复发缓解型MS(RRMS)的患者成为继发进展型MS(SPMS)。 SPMS病理生理学可能涉及线粒体功能障碍、小胶质细胞激活、血管内皮破坏和脑膜淋巴样组织的影响1。由此产生的神经变性和加速的脑萎缩与功能性残疾相关;因此,全脑萎缩是SPMS试验的当前金标准MRI替代结果测量2。针对特定的病理生理过程是治疗SPMS的合理策略。
硫辛酸(LA)是一种内源性抗氧化剂,具有多种生物功能,包括自由基清除、金属离子螯合、细胞内谷胱甘肽的再生和大分子的氧化损伤修复3。在线粒体中,LA /二氢硫辛酸氧化还原对是氧化呼吸的丙酮酸脱氢酶复合物的关键辅助因子,有助于核酸合成4。 LA调节对血管内皮完整性有重要作用的PKB / Akt信号通路,影响转录因子Nrf2,作为胰岛素模拟物5,6。我们的中心和其他人已经证明LA减少实验性自身免疫性脑脊髓炎(EAE)的残疾,减少炎症细胞向脊髓和视神经的迁移,并抑制巨噬细胞/小胶质细胞激活7,8。口服摄入LA的MS患者的血液水平与EAE相当9。在临床试验中,硫辛酸耐受性良好;常见的不良反应是胃肠道(GI)不耐受、头痛、恶臭尿和皮疹[10,11]。在这里,我们报告了一项为期2年的随机对照试验的结果,以确定LA是否降低全脑萎缩率,减缓临床恶化和在SPMS中是安全的。
方法研究设计
这是一项前瞻性、单中心、2年、II期、双盲、随机、安慰剂对照试验,每日1,200 mg口服外消旋LA,以回答以下主要研究问题:I 级证据:LA会减少 SPMS中全脑萎缩的发生率? 次要研究问题是确定LA是否会降低分割的脑、脊髓和视网膜下结构的萎缩率,减少残疾和生活质量的恶化,以及在SPMS中是否安全。 招募发生在2011年5月至2013年10月之间,最后一次访问是在2015年8月。该研究是在俄勒冈州波特兰的退伍军人事务部波特兰医疗保健系统(VAPORHCS)进行的,并在俄勒冈州波特兰市的俄勒冈健康与科学大学(OHSU)进行了一些程序处理。
参与者
入选标准为年龄40-70岁,之前的RRMS(2005McDonald标准)以及当前由SPMS定义的MS残疾进展,在过去5年内没有临床复发,由主要研究者(PI)根据病史和图表确定进展被定义为足以改变扩展残疾状态量表(EDSS)上的功能系统或实现有意义的功能变化(例如,由于认知下降而停止工作)13允许参与者开始,停止或继续研究期间醋酸格拉替雷或b-干扰素。排除标准是入组1年内使用那他珠单抗、免疫抑制剂、化疗或定期IV皮质类固醇治疗;入选后60天内复发皮质类固醇治疗;入组后30天内LA;MRI限制;自我报告的眼部疾病可能混淆光学相干断层扫描(OCT)解释;怀孕或哺乳;显著的活动性并发疾病;不受控制或胰岛素依赖性糖尿病,以及缺乏英语流利性交流的患者。由于前8个月招募缓慢,因此消除了EDSS限制6.0。
标准方案批准,注册和患者同意。
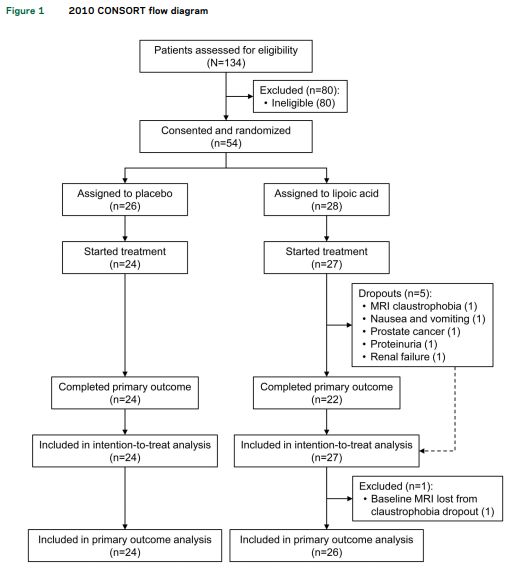
该研究得到了VAPORHCS和OHSU机构审查委员会的批准。所有参与者均获得书面同意。该研究在ClinicalTrials.gov(NCT01188811)上注册,并遵循2010 CONSORT指南进行。
研究人员角色
PI进行筛选访视和随机化的初始EDSS检查,评估不良事件(AEs),并作为研究监测。盲法神经病学家和神经病学高级从业者担任EDSS审查员。盲法研究协调员收集了流动数据,问卷和维护数据库。研究药物。 PI获得了研究性新药指征(编号110132)。 Pure Encapsulations(Sudbury,MA)提供含有600mg外消旋的明胶胶囊。
硫辛酸或安慰剂。
安慰剂胶囊含有Avicel(微纤维素晶体)和4.3 mg槲皮素(生物类黄酮),使安慰剂呈黄色,类似于LA。在重新测试样品胶囊后,通过Pure Encapsulations研究药物的期满延长一次,确定持续稳定性。
研究时间表。
筛选和基线访问间隔#30天。随后在第3,6,12,18和24个月进行的访问发生在62周。为安排目的,一个月被定义为4周。 MRI和OCT发生在基线、第12和24个月。在基线和每6个月收集临床结果指标。每次访问都进行安全实验室测量。在访问之间和研究完成之后发生电话呼叫以捕获AE。
结果
主要结果是使用萎缩标准化(SIENA)的结构图像评估在MRI上的年度百分比变化脑容积(PCBV)的差异。次要结果包括分割的脑,脊髓和视网膜下结构的萎缩率,残疾的变化,生活质量和安全性。
MRI采集协议 MRI采集和分析细节见Neurology.org/nn附录e-1。使用具有Quasar Dual梯度系统的Philips Achieva 3.0T X系列获得以下序列:(1)3D高分辨率磁化准备的快速采集梯度具有1 mm 3体素的回波(3D MP-RAGE),用于高分辨率结构(T1加权)信息。上颈髓通过定位有意包含在系列中; (2)具有1 mm 3体素的3D流体衰减反转恢复(3D FLAIR)系列; (3)传统的3 mm(0.3间隙)轴向2D质子密度/ T2加权序列,面内分辨率为1 mm 2; (4)3-mm矢状2D质子密度/ T2加权脊髓序列。没有使用血管内造影剂。
MRI分析
神经放射学家对MRI进行了意外检查。一名训练有素的MRI分析员进行了病变计数,体积测量和皮质厚度分析。 PI进行了脊髓横断面厚度和病变占位分析。两者均由研究神经放射学家指导。使用保留病理学的解剖分割(病变-TOADS)获得脑T2-高信号病变体积和图谱.15使用FSL工具创建充满病变的MP-RAGE图像。 SIENAX用于确定横断面的全脑,白色和灰质体积.16使用来自FSL包的SIENA测定全脑萎缩.16使用FIRST测量皮质下深灰质体积。皮质厚度,皮质体积用FreeSurfer(surfer.nmr.mgh.harvard.edu/)及其纵向加工流进行分割和分析.17在C1记录脊髓横截面积。为了描述目的,设计了从MS病灶占据的从枕骨大孔到C7下缘的脊髓相对百分比的内部估计。 MRI的质量评级(良好,公平,差,无法使用)。从分析中排除了不良和不可用的扫描。
OCT
参与者在药理学扩张后(1%托吡卡胺和0.5%盐酸丙美卡因)在每只眼睛中进行光谱域OCT(Cirrus HD-OCT; Carl Zeiss Meditec,Inc.,Dublin,CA)。用Optic Disc Cube 200 3 200和Macular Cube 512 3 128神经眼科医师获得周围毛细血管和黄斑扫描。排除的扫描具有混淆的发现,伪像,未对准或信号强度小于7。
临床措施。
EDSS捕获了残疾。在整个研究过程中,尽可能使用相同的EDSS检查员。门诊参与者的流动性测量是定时25英尺步行(T25FW),多发性硬化症行走量表(MSWS-12)问卷调查和活动特定平衡置信度(ABC)调查问卷18-20, 符号数字模态测试(SDMT)测试认知 21 , RAND36项简表健康调查评估了生活质量22, 安全监测。使用不良事件的通用术语标准4.0版(CTCAE v4.0)对AE进行分类。对复发,AE和早期研究终止就诊进行了计划外访问。每次就诊时检查安全监测实验室测试(全血细胞计数和肾脏和肝脏板)。哥伦比亚 - 自杀严重程度评定量表(C-SSRS)在每次就诊时进行。每年会有一个由3名成员组成的数据安全和监督委员会.
样本量,随机化和盲法
该研究有助于比较主要结果,PCBV,如Altmann等[23]所估算,使用1.51的SD对SIENA萎缩,2年研究长度与年度MRI,和60%效应大小。需要每臂23个样本大小以获得80%的功效和p,0.05的显着性。预计入学率增加以允许辍学。非基础研究药剂师在基于EDSS#4.5或.4.5.13的置换区组随机化后,以1:1的方式将参与者分配到LA或安慰剂。所有其他研究人员对治疗分配不知情。在分析期间,MRI用额外随机生成的数字标记,以进一步降低偏倚风险。统计分析由盲法统计学家进行,用于一级,二级和安全性结果测量。
统计方法
意向治疗(ITT)分析使用线性混合模型来评估LA对年化PCBV的影响。混合模型用于调整参与者内的序列相关性,以考虑纵向设计的重复测量,并包括所有研究参与者。通过标准模型诊断校正模型的参与者年龄,性别和MS持续时间,以确定过度影响的杠杆点。使用研究结果域内的Holm-Sidak校正来计算多重比较。通过标准诊断技术使用数据点杠杆,个体残差和库克距离的组合来识别异常数据点,以识别过度有影响的观察并将其从基线和2年变化分析中排除。参与者服用减少剂量的LA(n = 52)的数据在结果分析中没有得到不同的处理,因为他们的有限数量使得亚组评估难以处理。混合模型结果报告为变化率,方差由系数估计值(SEE)的标准误差表示。进行主要结果测量的事后分析,将基线全脑体积和基线T2-病变体积作为模型的协变量。所有分析均使用R 3.3.1和lme4包装中的附加实用程序进行.24,25
结果
在54名同意和随机化的患者中,51名参与者(27名LA和24名安慰剂)服用至少1剂研究药物并被纳入ITT分析(图1)。 46名参与者完成了研究(22名硫辛酸和24名安慰剂)。硫辛酸队列中的5名辍学者是因为MRI期间出现幽闭恐怖症,长期恶心和呕吐导致LA停止治疗,以及严重的并发疾病(前列腺癌,蛋白尿和肾功能恶化)。由于幽闭恐怖症的辍学没有完成基线MRI,因此PCB组的LAT队列ITT样本量为26(图1)。
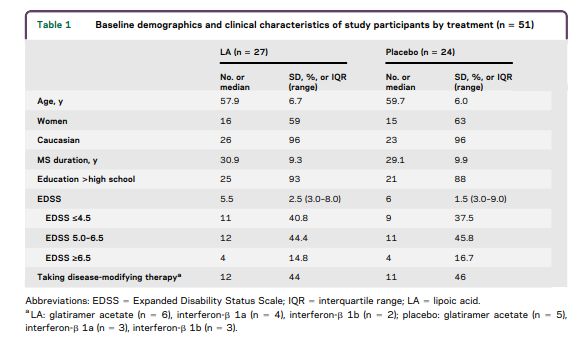
基线人口统计数据见表1。
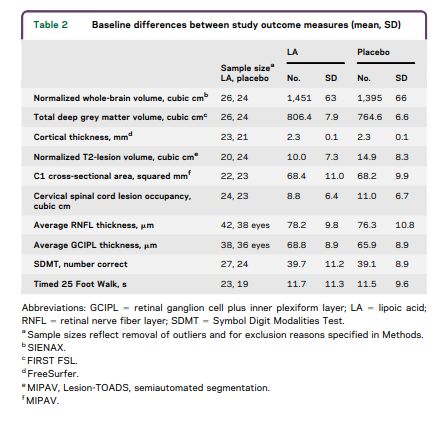
LA和对照组在年龄,性别,MS持续时间,教育和残疾方面总体匹配。治疗组之间没有显着差异(均为0.05)。表2列出了研究组主要研究结果测量的基线值。 LA队列具有显着更大的基线全脑(p = 50.004)和总深灰质体积(p = 0.042)。对照具有较大的基线标准化T2病变体积。通过药丸计数对研究药物的依从性为87%。对于大多数研究,两名参与者按照方案对一半剂量的LA进行了研究,其中一项针对胃炎和碱性磷酸酶水平升高。
脑萎缩率和继发性影像学结果
2年后,服用LA的参与者的年度PCBV显著低于对照组(20.21%[SEE 0.14])(20.65%[SEE 0.10],p = 0.002),LA治疗的有益效应观察为0.44%,全脑萎缩率改善60.29%(95%置信区间[CI] 0.157-0.727)。这一变化相当于LA与安慰剂相比脑萎缩率降低68%(图2A,表3)。在事后分析中,基线全脑容量与任何其他控制协变量(年龄,性别和疾病持续时间)无关,也不影响研究队列之间PCBV的差异。同样地,研究期间的T2病变体积变化与任何校正协变量无关,包括基线T2病变体积。显示研究完成者中对于LA的PCBV(20.45%[SEE 0.71])与对照(21.31%[SEE 1.10],p 50.001)的个体2年变化(图2B)。脑分割和OCT未显示研究组之间年度化变化率的显着差异; LA队列中T2病变体积的增加几乎与对照组无差异(414.6 [SEE 201.2] vs 33.1 [SEE] 134.7],第50.058页,表3)。
临床结果
在临床结果中,LA队列显示T25FW的改善与对照几乎但没有显着差异(20.535 [SEE 0.358] vs 0.137 [SEE 0.247],95%CI 21.37至0.03,p 50.060)。
不良事件
AE列于表e-1中。 LA和对照组之间的AE数量相似(分别为80和68,p = 50.87),每组有6个严重的AE(SAE)。在LA队列中发生更多胃肠道激惹(14 [SD 17%] vs 2 [SD 3%],p 50.007)和更少跌倒(12 [SD 15%] vs 26 [SD 38%],p 50.03)。一名硫辛酸参与者出现了一种非麻烦的水疱皮疹,类似于先前报道的皮疹,在研究完成后6周内消退11。每个研究队列中发生一次复发,既不影响随后的EDSS检查。 C-SSRS没有新的自杀行为,新实验室异常的队列之间没有差异;然而,只有那些服用LA的人需要按照方案减少剂量(n = 52)。与硫辛酸直接相关的SAE是呕吐和脱水需要住院治疗,这一问题一旦停止硫辛酸就解决了。导致辍学的显著AE是一名LA患者,其基线肌酐升高至肾功能衰竭,另一名患有肾小球肾炎引起的蛋白尿。咨询肾病专家并不认为2个AE与硫辛酸有关。附录e-2进一步讨论了AE。
讨论
这项为期两年、随机、双盲、安慰剂对照的试验性试验表明,SIENA每日口服LA含量为1200毫克的SIENA患者全脑萎缩年化率的显著降低。年度PCBV减少不受计划的年龄,性别和疾病持续时间的协变量的影响,也不受基线脑和T2病变体积的事后添加的影响。有人建议改善T25FW时间。
硫辛酸队列中的跌倒次数减少。整体LA安全,耐受性良好,依从性高,并且没有意外的有害AE或SAE归因于LA。
脑萎缩率的降低与ocrelizumab的大型3期试验(n = 5 731)相比有利,与120周内全脑萎缩率降低17.5% 26,与本研究相比 ocrelizumab试验仅包括原发进展型MS患者,男性较多(51%对39%),年轻(45岁vs 59岁),疾病持续时间较短(6.5 vs 30岁),残疾较少(EDSS 4.7 vs 5.4)。 ocrelizumab试验仅限于炎症性脑脊液患者,这是本研究未评估的特征。进展性MS人群中的其他疾病改善疗法试验未显示出脑萎缩率的强烈变化,或未使用该结果测量27-29。
PCBV减少用于SIENA的全脑评估,SIENA是一种强有力的基于登记的纵向萎缩测量30。脑分割未发现特定脑区对微分萎缩率负责。一种解释是样本量计算基于SIENA,而不是基于分割方法,产生异质结果并需要更大样本的技术.30分段体积可能更容易出现生理因素,包括水合状态和定位,而不是全脑测量.31或者,PCBV减少可能来自所有脑组织共同的影响。在较大样本中研究复制将阐明LA萎缩效应的性质。
LA队列中T2病变体积增加的建议具有不确定的意义。增加可能是真实的,因此代表LA的潜在有害影响,可能代表生理除MS之外的其他变化可能是由MR后处理质量问题引起的,或者可能与安慰剂不同.15需要进一步评估。整体而言,硫辛酸是安全的,耐受性良好。实验室异常局限于碱性磷酸酶的无症状升高,其在LA停止时有所改善。尽管没有明显可归因于LA的意外AE或SAE,但肾衰竭和肾小球肾炎病例引起关注。以前的LA研究尚未报告肾功能不全[9-11]。尽管如此,更接近的肾功能监测对于未来的LA研究是谨慎的,并建议在进一步评估之前推荐使用该剂量的LA。
作者在计划研究时未发现的潜在研究混杂因素是安慰剂中存在槲皮素(每日8.6 mg)。与其他生物类黄酮一样,槲皮素具有生物活性。虽然存在相互矛盾的报道,但Van Beek等人。发现每日10毫克口服槲皮素可增加炎症,加剧小鼠的主动和被动EAE。这提高了在本研究中槲皮素可能使对照恶化并夸大LA的影响的可能性32。 Van Beek研究中计算出的类似人体剂量为2 g,比安慰剂胶囊大几个数量级33。因此,虽然不太可能影响目前的研究结果,但未来的研究应该避免槲皮素排除这种可能性。
其他研究限制主要涉及该试验研究的小样本量,导致检测临床和次要成像结果的功率丧失,如上所述。鉴于此,尽管对照组与其他未经治疗的SPMS队列相比具有可比较的萎缩率,但可以从怀疑论中看到大脑萎缩率的强烈降低,这可以证实这一结果23,34脑容量或T2-的基线差异研究队列之间存在病变量;然而,事后分析未发现这些差异对研究结果的影响。未来研究中较大的样本量应纠正基线失衡。最后,由于未使用造影剂,MRI上炎症活动的基线和持续差异尚不清楚。
这项为期2年的每日1,200 mg LA试验表明,SPMS患者的PCBV显著低于对照组。虽然有人建议改善步行时间并且明显减少跌倒,但小样本量无法检测临床益处。虽然LA总体安全且耐受性良好,但未来的研究需要建立临床益处并探索LA在进展性MS中的作用机制。
作者的贡献
Rebecca Spain:研究概念和设计,研究监督,分析和解释数据,起草稿件并获得资金。 Katherine Powers:数据采集,MRI分析和稿件起草。 Charles Murchison:手稿的统计分析和起草。 Elizabeth Heriza:数据采集和手稿审查。 Kimberly Winges:审查OCT,数据分析和数据解释以及稿件审查。 Vijayshree Yadav,Michelle Cameron和Edward Kim:数据采集。 Fay Horak:学习概念和手稿评论。杰克西蒙:研究概念和设计,分析和解释数据,以及起草稿件。 Dennis Bourdette:研究概念和设计,研究监督,数据分析和解释,以及对手稿的批判性评论。
致谢
Pure Encapsulations,Sudbury,MA,提供了硫辛酸和安慰剂。作者感谢研究参与者Elizabeth Heriza博士的研究管理,以及数据安全和监测委员会的成员。
研究经费
由退伍军人事务部(B7493-W,R。Spain),NIH(UL1TR000128)提供支持。