NOX4 functions as a mitochondrial energetic sensor coupling cancer metabolic reprogramming to drug resistance Nat Commun. 2017 Oct 19;8(1):997. doi: 10.1038/s41467-017-01106-1 IF=12.124
背景
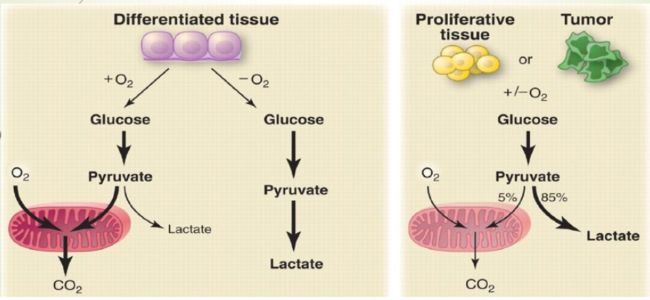
NOX4作为线粒体能量感应器,将肿瘤代谢重编程和治疗耐药联系起来。cancer metabolic reprogramming肿瘤代谢重编程,是新近关于肿瘤代谢的新名词,是指肿瘤细胞糖代谢主要以无氧糖酵解为主,不同于正常细胞有氧氧化磷酸化的产生ATP的高效率(32个ATP),无氧糖酵解只能产生少量的ATP(2个)和产生大量乳酸,消耗大量能量。不明白为什么肿瘤细胞采取效率更低下的无氧糖酵解,只好给它命名warburg效应。
沃伯格效应(Warburg effect) 是由德国生物化学家奥托·沃伯格(Otto Warburg,1883~1970)于1930年发现的。肿瘤细胞产生能量的方式极为特别: 健康细胞依靠线粒体氧化糖类分子释放出有用的能量, 而大多数肿瘤细胞则通过通过产能率相对较低糖酵解作用为自身供能。这种作用机制不需要氧气也不需要线粒体参与。恶性,生长迅速的肿瘤细胞通常的糖酵解率比他们的正常组织高达200倍。这种情况,即使在氧气充足的条件下也会发生。奥托华宝推测这种变化的代谢是癌症的根本原因。
NOX4,作为NADPH氧化酶(一种ATP-biding motif) 内一个亚基,论文结果显示当ATP与motif结合的时候,会影响NOX4的活性。那么NOX4的功能是什么?它是如何影响化疗耐药的呢?
线粒体内NOX4可以产生ROS,无氧糖酵解产生大量活性氧自由基(ROS),ROS会影响肿瘤细胞的增生和凋亡。调节NOX4上下游的位点需要进一步研究。
NOX4的耐药表型实验:NOX4是否调节化疗耐药?
细胞模型:renal cell carcinoma肾细胞癌,肾癌多由于von Hippel–Lindau (VHL) 基因的突变缺失所致。肾癌对化疗药物非常不敏感,天然的耐药细胞模型。
786-O肾癌模型,stably transfected with shVector and shNOX4,利用shNOX敲减细胞模型内NOX4的表达水平。
A498肾癌模型,transiently transfected with Scr and siNOX4,瞬时抑制NOX4表达水平。
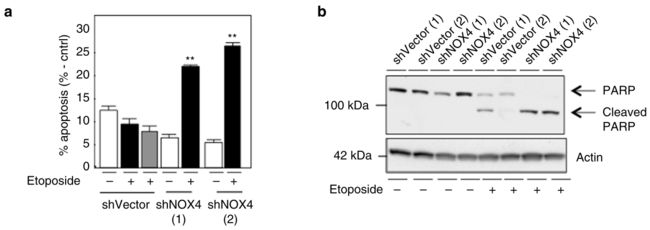
检测方法:上述细胞模型给予依托泊苷药物处理后,检测细胞凋亡情况,细胞凋亡的检测Annexin V staning、细胞流式仪、western检测cleaved PRAP(PARP又是细胞凋亡核心成员胱天蛋白酶(caspase)的切割底物)。
除此之外,还对下述问题进行简答:
1、是线粒体内的NOX4导致的耐药吗?NOX4在内质网、细胞核和细胞膜都有定位,到底是哪儿的NOX4介导的耐药。
专门针对线粒体NOX4的干扰方法:利用mitotempol药物处理细胞,专门清除掉线粒体超氧化酶,包括NOX4。然后在检测依托泊苷处理细胞后凋亡情况。
2、线粒体内ATP水平会影响耐药吗?因为之前结果显示ATP增多会抑制NOX4活性。
调节线粒体内ATP的方法:786-O培养液中加入半乳糖会增加线粒体内ATP;VHL转染缺失VHL的肾癌细胞会增加其线粒体内的ATP水平。
3、NOX4在ATP介导的耐药过程中是充分必要条件吗?whether NOX4 is neccesary and sufficient to mediated drug Resistance。
设计突变的NOX4,使得ATP不能与其结合,观察ATP对耐药的影响。与双荧光素酶实验异曲同工。
动物实验验证NOX4的耐药表型:动物水平NOX4是否导致耐药?
动物模型:裸鼠移植瘤模型,上述细胞水平的细胞模型,注射与裸鼠皮下,成瘤后,给予依托泊苷化疗,观察瘤体体积的变化。
786-O转染shVector的细胞注射于裸鼠左侧腹部皮下,5周后成瘤,测量体积。
786-O转染shNOX4的细胞注射于裸鼠右侧腹部皮下,……。
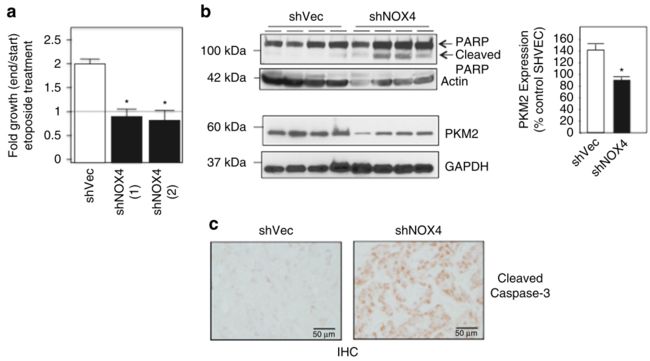
检测方法:成瘤模型成功后,给予依托泊苷化疗4天,每天测量瘤体体积共8天。以8天的体积比上化疗前体积,作为最后显示数值。同时为了验证主要是因为凋亡增加,而不是增生减弱,还检测的凋亡指标:cleaved PRAP(western)和cleaved caspase-3(免疫组化)。
人体水平是否有证据:NOX4导致耐药?
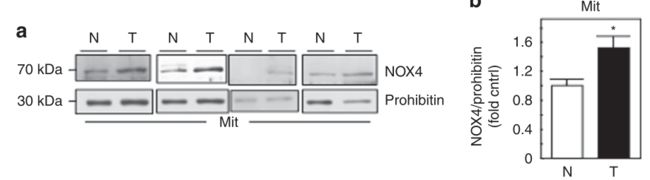
取肾癌组织和周围正常组织,分离线粒体,检测线粒体内NOX4表达水平,肾癌组织与正常组织相比,NOX4表达升高。
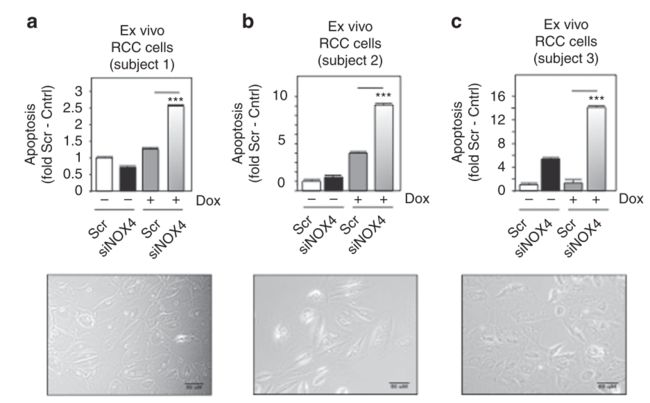
细胞模型(ex vivo实验):肾癌原代细胞模型,取肾癌组织,分离原代细胞进行培养,然后利用siNOX4瞬时抑制细胞内NOX4表达水平。给予多柔比星后,测定细胞凋亡情况。
NOX4调节耐药的下游靶基因,深入分子机制
PKM2:丙酮酸激酶2,参与糖酵解的最后一步,既往显示其与肿瘤细胞的生长和凋亡相关。推测PKM2可能为NOX4调节的靶基因。
1、PKM2是否调节药物治疗敏感性:siPKM2抑制786-O和A498细胞PKM2,细胞对化疗药物诱导的凋亡增加,assembly shNOX4。
2、PKM2是否被NOX4调节:PKM2表达在shNOX4抑制NOX4后,明显降低。
3、NOX4是否通过抑制PKM2的乙酰化,保护PKM2被降解:背景PKM2常常被乙酰化,然后溶酶体吞噬消化乙酰化的PKM2。shNOX4抑制786-O细胞后,检测PKM2乙酰化状态,乙酰化的PKM2明显增多,乙酰化的PKM2可以通过乙酰化抗体检测。
4、PKM2是否是被溶酶体吞噬消化降解:采用溶酶体降解抑制剂3-M抑制细胞内溶酶体降解通路,观察PKM2被降解减少,残留PKM2增多。
5、溶酶体降解既然参与PKM2的降解,且PKM2是调节化疗药物的敏感性,那么溶酶体通路是否会影响到化疗耐药呢?shNOX4的786-O细胞对依托泊苷药物敏感,但是如果用3-M抑制溶酶体降解通路后,其对依托泊苷敏感性明显下降。(因为PKM2滞留)
6、PKM2被乙酰化酶PACF在K350位点乙酰化,然后被溶酶体降解。那么乙酰化酶PACF是否影响肾癌细胞的化疗耐药: a、 siPACF干扰786-O细胞PACF的表达,给予依托泊苷后,检测细胞凋亡变化,凋亡减少,出现耐药,且检测细胞内PKM2表达增高。b、突变PACF乙酰化位点K450R(赖氨酸-精氨酸),乙酰化酶PACF不能发挥作用,shNOX4的786-O细胞,对依托泊苷敏感性增强,当转染PKM-K350R,对药物敏感性恢复耐药。
线粒体NOX4被ATP调节:NOX4的上游通路
我会怎么做:将细胞模型与或不与ATP共培养,观察线粒体NOX4功能变化,其中线粒体NOX4生物功能为产生ROS,那么检测加不加ATP后ROS的产生量,即可验证ATP调控NOX4。
作者1、明确NOX4定位在线粒体、2、线粒体有脂质体双层膜,NOX4是位于内膜还是外模、3、NOX4是否影响ROS的产生、4、最后才是ATP是否影响ROS的产生。
线粒体NOX4是能量代谢的感受器:
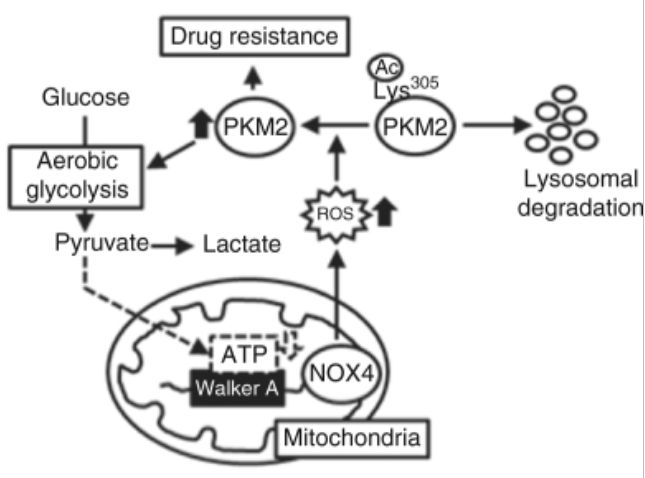
如何将细胞内ATP含量、NOX4活性和ROS联系起来?癌细胞由于wanburg效应,采用细胞浆内糖酵解的能量代谢方式,而不是采用在线粒体内氧化磷酸化,由于产能较低,细胞内ATP水平下降,线粒体内NOX4感受不到ATP的刺激,活性增强,ROS产生增多。而NOX4活性增强,会保护PKM2被溶酶体降解,最终PKM2抑制细胞凋亡,导致药物耐药。