新 型 疫 苗 成 功 案 例
一位来自加拿大里贾纳的女士被诊断为晚期肺癌,并且被告知仅有一年的生存期,但现在她已经幸运的处于缓解期,她说,这要感谢古巴的肺癌疫苗。
2016年,朱迪布莱登得到的是几乎毁灭性的诊断结果——四期肺癌。去年,Bryden前往古巴接受治疗,并接受了非小细胞肺癌疫苗--CIMAvax EGF治疗。这是一种专门针对于该非小细胞肺癌的治疗型疫苗(占所有肺癌的85%)。
在接受几个月的疫苗治疗后,Bryden说,最近她进行的肺部扫描没有发现肿瘤。
“当医生告诉我,我的生命只剩下一年时,我说我会证明他们错了!”她希望尽可能多的让加拿大国内像她这样,已经没有其他治疗选择的晚期肺癌患者能够知道古巴肺癌疫苗CIMAvax的存在。
在确诊后,Bryden接受了化疗和五次放射治疗,但仍然不能阻止癌症的进展。她的丈夫Lorne Bryden开始在网上寻找更多的治疗选择,他看到了CIMAvax。
他了解到疫苗通过引发患者自身免疫系统产生针对与癌细胞生长和繁殖有关的蛋白质的抗体而起作用。研究表明CIMAvax可以延长非小细胞癌患者的生存时间。一项临床试验发现,CIMAvax的对肺癌患者长期管理“非常安全”。
注射一年古巴肺癌疫苗CIMAvax的费用约为14,500美元。这对很多晚期患者来说是“值得的”。
先来看看到底肺癌四期是一种怎样的癌症发展阶段,四期的肺癌有多严重?
肺癌一共分为四期,一般认为,小细胞肺癌的广泛期和非小细胞肺癌的三期,四期都可以认为是肺癌晚期。此时癌细胞已经扩散到身体的其它部位,出现骨转移、肝转移、脑转移或其它部位转移,其最大特点是丧失了手术机会。
但是由于肺癌晚期可出现各个不同脏器的转移,可造成相应的症状,经常给患者带来很大的痛苦,甚至威胁到生命。
(1)骨转移:大约有50%肺癌病员最终会出现多个部位的骨转移。骨转移早期一般无任何症状,骨同位素扫描可发现有病变的骨骼。骨转移症状与肿瘤转移的部位、数量有关,如肺癌肋骨转移造成的胸痛,多表现为胸壁部位局限的、有明确压痛点的疼痛。
(2)肝转移:肝脏也是肺癌常见的转移部位,约有28-33%的肺癌出现肝转移。肝转移是原发性肺癌的癌细胞脱落后通过血液循环侵入肝脏并在肝脏种植生长,肝转移可以是单发或多个结节转移灶。最常见的症状为肝区疼痛,为持续性涨痛,同时可伴有食欲不振,消化不良等肝功能受损的表现。
(3)脑转移:肺癌病员出现无原因的头痛、呕吐、视觉障碍以及性格、脾气改变可能为肺癌转移到脑部造成的颅内高压或颅神经受损导致。常见于小细胞肺癌、腺癌类型。
(4)其它部位转移:肺癌除上述几种常见转移部位外,较少见的转移部位有皮肤、腹腔内、肌肉、皮下组织和心脏等部位的转移,症状常与转移部位相关。如转移到心脏可出现胸闷、心悸甚至气急、心律紊乱、晕厥等症状。
因此,肺癌四期患者若治疗不当,很可能造成身体的极度不适以及抗癌的信心。此次古巴学者研究出的两款新药,CimaVax和Vaxira提高了患者的五年生存率,相信能让更多像Judy Bryden女士一样的肺癌患者“逃离”肺癌的魔掌。
V a x i r a
Racotumomab(Vaxira®)疫苗长期以来一直用于刺激免疫系统保护和帮助人体抵抗导致感染和疾病的外来因子(主要是病毒或细菌)的能力。Racotumomab是CimaVax EGF后在古巴开发的第二种非小细胞肺癌疫苗。
V a x i r a 作 用 原 理
正如免疫系统在保护身体免受病毒和细菌感染时起作用一样,它还通过检测癌细胞并在许多情况下摧毁它们来保护身体免受癌症侵害。不幸的是,当癌细胞抑制免疫系统或隐藏逃避免疫系统监测时,或者当癌细胞数量庞大时会压制免疫系统。癌症疫苗通过让免疫系统识别并针对不同类型的癌症采取行动,这类似于其他疫苗的工作原理。
Racotumomab(Vaxira®)通过阻断肿瘤生长中存在的NeuGc GM3神经节苷脂的细胞和体液免疫应答起作用,从而延缓其发展并由此增加患者的预期寿命并改善生活质量。与传统的化疗和放射治疗癌症不同的是,racotumomab是一种耐受性良好的治疗方式,最常见的副作用是注射部位轻微疼痛以及虚弱乏力感。
临 床 试 验 数 据
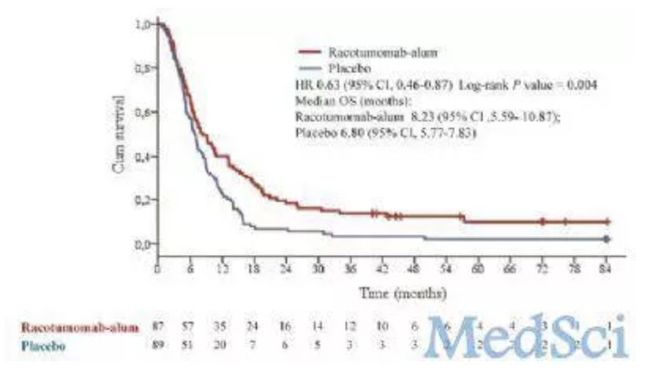
176位一线化疗后病情稳定的IIIb/IV期非小细胞肺癌患者被按1:1的比例随机分配到racotumomab组(每2周接种一次,每4周再次接种一次)或安慰剂组。
racotumomab组中位总生存期为8.23个月,安慰剂组中位总生存期为6.80个月(HR 0.63;95%CI 0.46-0.87;p=0.004)。racotumomab组中位无进展生存期为5.33个月,安慰剂组中位无进展生存期为3.90个月(HR 0.73,95%CI 0.53-0.99;p=0.039)。
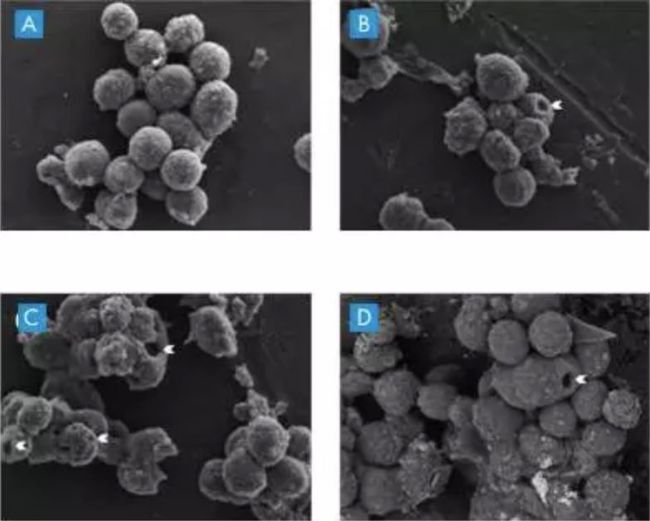
经验证,非小细胞肺癌患者使用racotumomab(Vaxira)免疫治疗,可以作为替代抗原,并使免疫系统活化,以使免疫系统在其表面产生抗癌细胞(表达式为NeuGcGM3)的特定反应杀死癌细胞,这种细胞毒性有别于细胞凋亡,它与温度无关,没有染色体固缩等特征。Vaxira是通过诱导癌细胞产生类似肿胀坏死的反应。
V a x i r a 安 全 性
racotumomab组最常见的不良反应是注射部位烧伤和疼痛、骨痛和乏力。这些患者获得了对NeuGcGM3神经节苷脂的IgM和IgG抗体反应。超免疫血清能够特异性识别和杀伤表达NeuGcGM3的L1210细胞系。有NeuGcGM3抗体的患者能够结合并杀灭超过30%的L1210细胞,这些患者的中位生存期也较长。
C i m a V a x
CimaVax是全球首个注册的用于晚期非小细胞肺癌的肺癌疫苗。经过哈瓦那分子免疫中心的科学家研发和测试,自1998年以来的大量临床试验证实了两种疫苗的安全性和有效性,并已获批进入临床应用。
CimaVax EGF是古巴分子免疫学中心和基因工程和生物技术中心共同开发的25年研究计划的结果。它是世界上首个用于3期和4期非小细胞肺癌疫苗,通常在化疗和放疗后给予。
C i m a V a x 作 用 原 理
CimaVax EGF通过靶向表皮生长因子(EGF)来发挥作用,表皮生长因子(EGF)是一种天然存在于体内的蛋白质。在一个健康人体内,EGF通过附着在细胞表面的受体上,给细胞提供生长和分裂的信号。在某些类型的癌症如非小细胞肺癌中,身体会产生过多的EGF,迫使细胞不受控制地生长和分裂。CimaVax EGF刺激免疫系统产生特异性针对EGF并与其结合的抗体。由于EGF不再附着于癌细胞上的受体,因此癌细胞不再接受生长和分裂的信号,从而减缓癌细胞失控的生长。
但是注意,CimaVax EGF不能阻止癌症的发展,更不能治愈癌症。而是启动了一种机制,通过这种机制,癌细胞的失控生长和分裂更加受到限制,从而将晚期侵袭性肺癌转变为慢性疾病。
C i m a V a x 评 估 内 容
CimaVax肺癌疫苗医疗评估内容包括以下病历摘要。
病理诊断
治疗经过及评效
目前病情是否稳定
CBC
ESR
全相关碱性磷酸酶血液(血清)谷氨酸草酰乙酸
转氨酶(SGOT)测试
血液(血清)谷氨酸丙酮酸转氨酶(SGPT)测试尿素
肌酸酐测试
尿酸测试
诱导期为两个月,可带回国内接受治疗。
临 床 数 据 汇 总
第一次试验研究(1995-1996),10名患者帮助从脑膜炎奈瑟氏球菌挑选载体蛋白P64。
第二(1997 - 1999年)和第三(1998 - 2001年)试点研究,20名患者帮助选择Montanide ISA 51作为佐剂。环磷酰胺pre-Rx作为免疫调节剂。通过测量抗EGF抗体,帮助鉴定Good(GAR)和Poor(PAR)抗体应答者。
第四次试点研究(2000-2003),通过43例患者区分临床结局GAR和PAR,前者与更长的生存时间相关联。低和高血清EGF浓度分别与GAR和PAR相关。高血清EGF浓度与NSCLC不良预后相关,表明CimaVax可能引发有效的抗EGF免疫应答。
第五次试点研究(2001-2005)显示高剂量疫苗可以安全地联合化疗,增加抗EGF抗体浓度。20名患者中有2名患者生存时间增加甚至达到缓解。
2016年,发表在临床癌症研究杂志上的重磅三期临床数据轰动全球。
试 验 结 论
CimaVax肺癌疫苗具有良好的耐受性,完成诱导期疫苗治疗的患者中位生存期显著提高。EGF浓度高的患者更能获益。
对于血清EGF高浓度(>870pg/mL)的患者,试验组(70人)对比对照组(25人)有显著生存受益(中位生存期14.66个月vs8.63个月,P=0.0001)。
CimaVax疫苗副作用温和,但起效缓慢,不适合当前病情进展的患者。
CimaVax疫苗的适应人群为血清EGF高浓度(>870pg/mL)的NSCLC患者,而高加索白人,吸烟,肺腺癌患者相对其他人群有显著优势。
该3期临床结果解答了2012年-2013年中国几百名非小细胞肺癌患者使用CimaVax疫苗为什么疗效不佳的疑问。
而对于肺腺癌患者,当前标准的维持治疗药物是培美曲赛(PFS 4.3个月,OS 13.4个月),CimaVax疫苗毫无优势。
截至2016年,3000多名晚期非小细胞肺癌患者接受了CimaVax-EGF疫苗,显示其安全,免疫原性和适度有效。
❤️美医小提示❤️
有很多人认为,延长4~6个月和没延长没什么区别,但事实上,医学上的每一点进步背后都是无数科学家付出了巨大的努力取得的,并且,关于癌症的研究进展每天都有新突破新进展,也许延长一个月的生命,就能等到新药物获批,就有新的希望!
该疫苗已在2017年在美国进行临床试验,并会在2022年完成,一旦疗效确定,这款疫苗将在美国上市,造福全球的肺癌患者!
文章来源:环宇达康全球专家