干扰素在新冠肺炎治疗中发挥抗病毒和免疫调节的双重作用
近日,《英国药理学杂志》(British Journal of Pharmacology)刊登了一篇有关探索治疗新冠肺炎药物的文章提到,虽然目前尚没有治疗新冠肺炎的灵丹妙药,但从现有药物中成功鉴定出一种可用于治疗该传染病的药物可能比研制出疫苗所需的时间更短。该论文的通讯作者、国际基础与临床药理学联盟(IUPHAR)命名和标准委员会主席、英国诺丁汉大学分子药理学助理教授Steve Alexander表示,目前用于治疗其他疾病的药物很可能会被重新利用。现有的证据显示,自20世纪70年代进入临床的广谱抗病毒药物干扰素,由于其独特的广谱抗病毒和免疫调节双重作用,成为一个潜在有效的抗新冠病毒药物。
新冠病毒是如何入侵人体的
不同于绝大多数由细胞组成的生物,病毒是一类无细胞结构的简单生物,仅由负责其繁衍的遗传物质核酸(RNA和DNA)以及保护遗传物质的蛋白质外壳组成。新型冠状病毒(2019-nCoV)的遗传物质是RNA,因其外壳像一顶皇冠而得名。如此简单的结构使它无法进行复制增殖,只能寄生于其他动物体内,借助于完整的细胞功能进行后代繁衍。
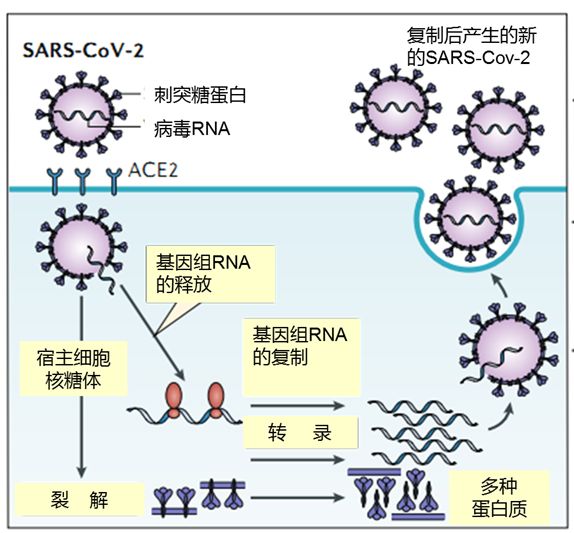
但是这些“求大神带”的病毒不是所有细胞都带得动,它们只入侵特定的细胞。当细胞拥有血管紧张素转化酶2(ACE2)的“标签”时,新冠病毒就凑上去“求组队”,在细胞中利用细胞的各种物质进行复制。巧的是,2003年的SARS冠状病毒(SARS-CoV)也是通过识别ACE2“标签”入侵细胞,但新型冠状病毒充分发挥“狗皮膏药”的精神,它与ACE2受体结合力更强。新冠病毒外壳蛋白(棘突蛋白上的多碱基弗林蛋白裂解位点)能够帮其侵染鼻咽、咽部上皮细胞,从而撬开呼吸道的第一道屏障,一般经过2-5天的快速复制后,进而蔓延入侵有丰富ACE2受体的下呼吸道组织。病毒入侵后,利用细胞的遗传物质,实现大量的自我增殖复制(见图1)。
图1. 2019-nCoV 的复制过程:
吸附-侵入-脱壳-生物合成-装配-释放
免疫系统如何防御病毒入侵
人体免疫分为先天性免疫和适应性免疫。
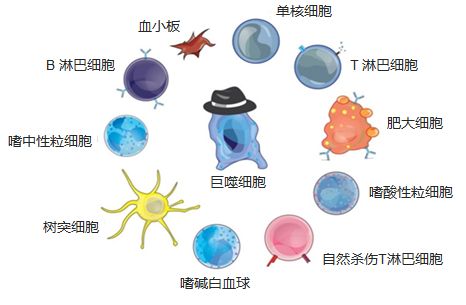
一旦病毒冲破人体第一道天然防御屏障(主要是皮肤和黏膜),体内的先天性免疫系统就会发挥作用,产生干扰素等细胞因子。其中,Ⅰ型干扰素与其受体结合后可触发其自身的信号级联反应,并启动多种抗病毒效应物的表达。另外,Ⅰ型干扰素可与免疫细胞膜表面受体结合,调动、增强自然杀伤细胞和细胞毒性T细胞等免疫细胞活性,防止病毒在细胞间传播、清除病毒感染的细胞(见图2)。先天性免疫系统具有“广谱性”,其工作原理是“使用相同的武器,防御不同的病原体”。
由于导致这一轮疫情的元凶——新冠病毒在人类为首次发现的病原体,人群尚未建立有效的特异性免疫。在该病毒感染时,先天性免疫首先发挥作用,通过免疫细胞对病原体的加工和抗原呈递,为适应性免疫应答的识别准备条件。适应性免疫系统则具有靶向性,通过产生特异性结合病原体的抗体等,对病原体实施高效、精准打击。
图2. 免疫系统的各种免疫细胞
内源性干扰素分泌不足或可导致病毒感染后病情加重
先天性免疫是一切免疫防护能力的基础。但是,今年4月香港大学的微生物系研究团队研究发现,新冠病毒的其中一个重要特征是,它们的“辅助蛋白”能帮助病毒在早期逃避人体的先天免疫反应,抑制干扰素和促炎症因子。5月7日,由法国国家科学研究中心、国家卫生和医学研究所以及里昂的高校、医院研究人员等组成的科研小组,对法国里昂等医院的新冠肺炎患者进行研究,发现约20%的患者中,血液中检测不到干扰素,而这批患者后来均病情转重。因此,研究人员认为,内源性干扰素分泌不足可能对人体免疫系统控制抑制病毒有负面影响。
新型冠状病毒的传染力强,各年龄段的人群都易感,对于多数老年人或有基础疾病的人来说,症状表现较重。儿童感染后症状相对较轻,也有部分人群可能因为机体免疫功能较强,在感染新冠病毒后症状轻微,或一直无明显症状(即无症状感染者)。这说明了自身免疫力较弱的人在感染新冠病毒后更易发展到重症。因此,对于免疫力较弱、干扰素分泌相对不足的患者,及时补充外源性干扰素将可有助于抑制病毒复制、缩短病程,并可提高人体免疫功能。
干扰素有良好的抗病毒作用
美国得克萨斯大学的研究团队,设计了考察干扰素α是否能抑制新型冠状病毒的体外实验,于2020年3月发表在预印本《bioRxiv》上。该研究通过在无法产生干扰素应答的Vero细胞中加入干扰素,观察其是否能抑制新型冠状病毒的复制。首先,用高剂量的干扰素α(1000 U/ml)预处理感染的细胞时,未观察到新型冠状病毒基因表达;而用低剂量(111 U/ml)处理后,检测到了少量新型冠状病毒基因的表达,证实了干扰素α对新型冠状病毒的抑制作用,且高剂量时可完全抑制病毒。
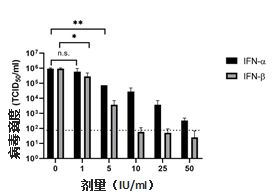
美国得克萨斯大学另一个研究团队探讨了干扰素抑制病毒的有效浓度范围。研究中采用不同浓度干扰素预处理Vero细胞,用新型冠状病毒感染细胞一定时间后测病毒滴度。结果发现,干扰素α和干扰素β的EC50(抑制半数病毒所需要的浓度)分别为1.35IU/ml和0.76 IU/ml,证实干扰素在体外能够有效抑制新型冠状病毒复制,且呈剂量依赖关系。
图3 干扰素的体外抑制新冠病毒的剂量-效价关系
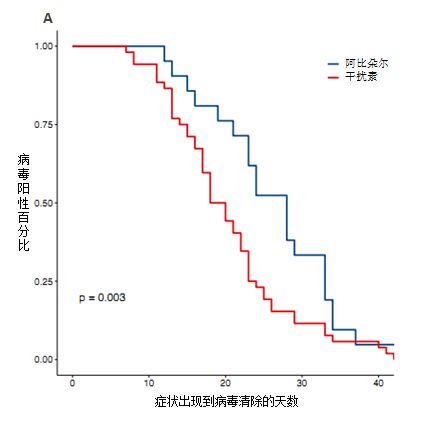
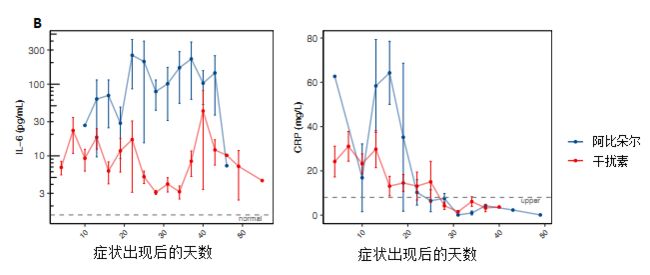
目前,已有多项干扰素治疗新冠肺炎的临床研究报道。其中,华中科技大学同济医学院研究人员进行的一项回顾性研究,分析了2020年1月~2月确诊的77名新冠肺炎住院患者的治疗效果。雾化吸入干扰素α治疗(500万IU/次,一天两次)与阿比朵尔(600mg/日)相比(结果见图4),干扰素治疗组可显著降低患者上呼吸道病毒载量,并缩短了血液中炎症反应指标(IL-6和CRP)复常的时间,且未见明显不良反应。
图4症状出现后不同治疗组病毒清除的天数(A)和炎症的持续时间(B)
干扰素由于其具有广谱抗病毒作用,且安全性良好,是抗病毒药物联合使用中常见的联合用药之一。香港大学袁国勇团队于5月8日发表在《Lancet》上的文章显示,该研究针对轻型至中型新冠肺炎确诊患者开展了一项随机、对照、多中心Ⅱ期临床试验,试验组使用三联抗病毒治疗(干扰素+洛匹那韦/利托那韦+利巴韦林),对照组为洛匹那韦/利托那韦。结果显示,患者早期给予抗病毒治疗,与对照组相比,三联组可显著缩短症状恢复的时间(三联组vs对照组:4天vs 8天),并缩短病毒脱落时间(7天vs 12天)和住院时间(9.0天vs 14.5天),并且对炎症指标的复常也有促进作用。该研究团队在讨论部分中谈到:“对于任何新出现的传染病,总是希望能尽快研发出特异性抗病毒药物,但一种新的抗病毒药物的临床开发至少需要数年甚至十几年才有可能应用于临床。因此,通过评估曾用于治疗其他病毒感染的广谱抗病毒药物,是应对病毒感染疫情大流行最可行的方法。”
基于抗病毒药物种类少以及抗病毒作用有限的现实,对抗病毒最有效的方法是提高人体自身的免疫力。干扰素在这次新冠疫情中老药新用,不仅可以有效抑制新型冠状病毒的复制,还可以早期干预以提高机体固有免疫,使易感细胞处于抗病毒状态。因此,在新型冠状病毒感染早期,及时补充外源性干扰素,可有助于清除病毒,缩短病程,提高患者治愈率。
另外,近些年随着干扰素新剂型的研发,有更多局部使用的治疗方法应用于临床抗病毒治疗。如前所述,在新冠病毒感染早期,鼻咽部是病毒入侵且快速复制的部位,使用干扰素α2b喷雾剂在鼻、咽部局部给药,可在局部抑制病毒复制,同时有助于提高局部固有免疫。对有新冠病毒感染者接触史的高风险人群,给予干扰素局部早期干预,是非常值得探索的研究方向。
特约供稿:首都医科大学附属北京地坛医院感染性疾病诊疗中心主任医师蒋荣猛
参考文献:
1.Lan J, Ge J, Yu J, et al. Structure of the SARS-CoV-2 spike receptor-binding domain bound to the ACE2 receptor. Nature 581, 215–220 (2020). doi: https://doi.org/10.1038/s41586-020-2180-5.
2.Risitano AM, Mastellos DC, Huber-Lang M. et al. Complement as a target in COVID-19[J]. Nat Rev Immunol. 2020 Apr 23. doi: 10.1038/s41577-020-0320-7.
3.Chu H, Chan JF, Wang Y, et al. Comparative replication and immune activation profiles of SARS-CoV-2 and SARS-CoV in human lungs: an ex vivo study with implications for the pathogenesis of COVID-19. Clin Infect Dis. 2020;ciaa410. doi:10.1093/cid/ciaa410
4.Sophie Trouillet-Assant, et al, Type I IFN immunoprofiling in COVID-19 patients.doi: https://doi.org/10.1016/j.jaci.2020.04.029.
5.Emily Mantlo, Natalya Bukreyeva, Junki Maruyama, et al. Potent Antiviral Activities of Type I Interferons to SARS-CoV-2 Infection. bioRxiv 2020.04.02.022764. doi: https://doi.org/10.1101/2020.04.02.022764
6.Kumari G. Lokugamage, Adam Hage, et al. SARS-CoV-2 is sensitive to type I interferon pretreatment.bioRxiv 2020.03.07.982264; doi: https://doi.org/10.1101/2020.03.07.982264
7.Qiong Zhou, et al. Interferon-α2b treatment for COVID-19[J]. Frontiers in Immunology. doi: 10.3389/fimmu.2020.01061.
8.Ivan Fan-Ngai Hung, Kwok-Cheung Lung, Eugene Yuk-Keung Tso,et al. Triple combination of interferon beta-1b, lopinavir–ritonavir, and ribavirin in the treatment of patients admitted to hospital with COVID-19: an open-label, randomised, phase 2 trial[J]. The lancet. doi:https://doi.org/10.1016/S0140-6736(20)31042-4