肠道-甲状腺轴如何影响健康
现如今,甲状腺疾病的发病率逐年递增,而女性更是甲状腺疾病的重灾区,据统计,每八名女性中就有一人患有甲状腺疾病。而甲状腺问题和肠道问题往往是齐头并进的。
本文我们将探讨肠道与甲状腺联系背后的科学事实,并提供有用的干预措施,助你走上改善肠道和甲状腺健康的道路。
01 甲状腺及其功能
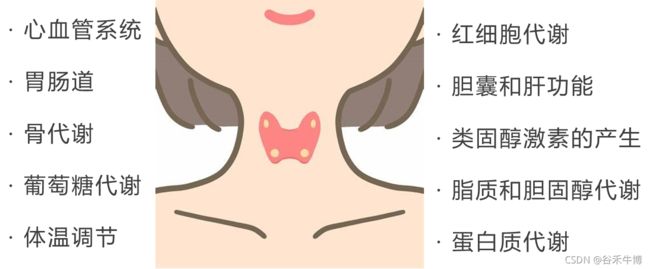
甲状腺是位于颈部底部的一个小而重要的内分泌腺。
甲状腺如何参与调节新陈代谢?
甲状腺的工作是确保体内的细胞正常工作,通过激素来发送信息到每一个细胞。它生产两种重要的激素,分别是T4和T3(具体意思见本节末“名词小讲堂”),激素的工作是指导体内的细胞工作,何时该消耗氧气养分,从而维持体内新陈代谢的过程。
人体内的每个细胞都有这些激素的受体,甲状腺的作用包括:
同时呢,甲状腺也是受约束的,它何时发送信息是被脑部的垂体监控着的,垂体会感受血液中的激素含量高低,以促甲状腺激素(TSH)的形式发出指示。可以看到,这是一个精密运作的系统。
然而,甲状腺激素的产生、转化和摄取过程非常复杂,如果任何一步出错,就会出现甲状腺功异常的症状。
▲甲状腺过度活跃——甲亢
甲状腺过度活跃,发出太多激素时,就会出现甲亢,新陈代谢就会加快,表现为心率过快,持续饥饿,体重下降,出汗,焦虑,难以入睡。
▲甲状腺活动不足——甲状腺功能减退症
甲状腺活动不足时,就会出现甲状腺功能减退症,也就是甲状腺发出激素太少,没有足够的量去唤醒体内细胞,新陈代谢减慢,表现为体重增长,怕冷,关节肿大,感觉忧郁。
名词小讲堂:
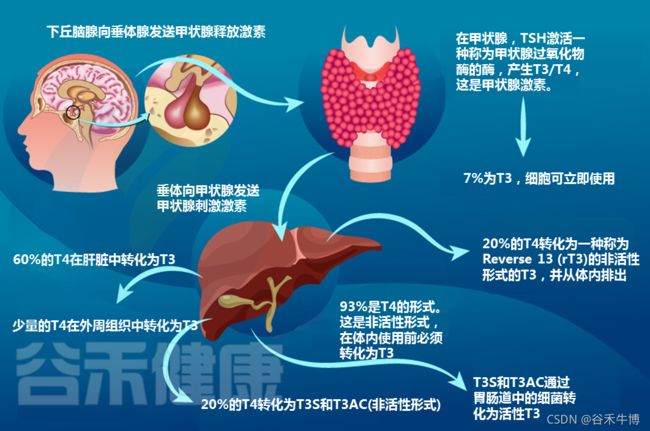
促甲状腺激素释放激素 (TRH):这种激素在下丘脑中产生,它向垂体发出信号以产生多少促甲状腺激素 (TSH)。
促甲状腺激素(TSH):由垂体产生,TSH 刺激甲状腺产生甲状腺激素 T4 和 T3。TSH 水平升高可能表明甲状腺功能低下。需要注意的是,并非所有甲状腺功能减退症患者都符合这种模式。如果甲状腺激素水平低,TSH 水平低也可能表明存在问题。
甲状腺素 (T4) 和三碘甲状腺原氨酸 (T3):统称为“甲状腺激素”,T4 和 T3 由甲状腺产生。T4 是甲状腺激素的非活性形式,必须先转化为 T3,然后身体才能使用它。
总 T4 和 T3:它们与蛋白质载体结合,可以在血液中循环
游离 T4 和 T3:它们与载体分离,可以与细胞受体结合并发挥其功能 。
甲状腺结合球蛋白 (TBG): TBG 是与 T4 和 T3 结合并通过血液运输这些激素的蛋白质载体。过多的 TBG 会导致游离 T4 和 T3 水平降低。
甲状腺抗体:在自身免疫的情况下,这些抗体会攻击并损害甲状腺。我查看甲状腺过氧化物酶 (TPO) 抗体 (Ab)和甲状腺球蛋白 (Tg) Ab。这些抗体可以在临床甲状腺功能减退症发生前数年出现,因此及早发现它们尤为重要。
02 肠道影响甲状腺
目前研究表明,良好的甲状腺健康始于肠道。随着我们对肠道微生物群的了解不断加深,可以看到研究表明,生活在人体内的微生物群在甲状腺功能减退症和自身免疫性甲状腺疾病中发挥着重要作用。
甲状腺疾病,例如桥本甲状腺炎或甲状腺功能减退症,通常与不孕症、荷尔蒙失衡、体重增加、疲劳或焦虑等症状有关。
甲状腺功能障碍的胃肠道症状很多,包括吞咽困难、胃灼热、消化不良、产酸减少、恶心或呕吐、胆囊不适、腹部不适、胀气、腹胀、腹泻、便秘和一般消化道不适,包括肠易激综合征 (IBS)。
肠道对甲状腺的影响
█ 始 于 炎 症
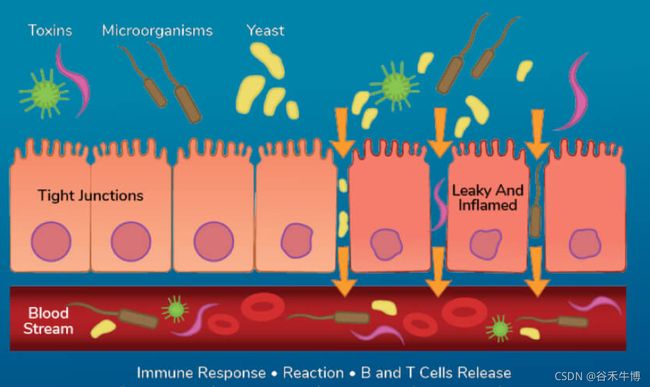
导致自身免疫性疾病的最常见炎症来源之一是肠道通透性过高或“肠漏”。这就是肠道-甲状腺有关联的地方。
桥本氏病是一种器官特异性自身免疫性疾病。就其核心而言,桥本氏病的根源在于炎症,在大量病例中,炎症可能始于甲状腺之外。
肠黏膜在过境点充当“海关”的角色。肠黏膜(肠内层)允许食物中的营养物质进入粘膜下层,从而利于我们吸收营养物质,同时将食物中潜在的有害物质和细菌的碎片排除在粘膜下层之外,那里会引发炎症和免疫反应。
炎症如何引发桥本氏病?
同样,促甲状腺激素释放激素 (TRH) 和促甲状腺激素 (TSH) 都会影响肠相关淋巴组织的发展。T4可防止肠道上皮内淋巴细胞 (IEL) 的过度表达,从而导致肠道炎症。
随着时间的推移,粘膜下层持续暴露于炎症和免疫诱因会导致身体产生抗体。抗体是识别和对抗病毒和细菌的特殊蛋白质。这些抗体还可以开始识别和攻击宿主的身体组织,包括甲状腺组织,并破坏甲状腺产生或使用甲状腺激素的能力,从而导致桥本氏病。
而肠道微生物群通过抑制促炎细胞因子(如 IL-6、TNF-α、NFK-b)和促进抗炎细胞因子(如 IL-10)来调节炎症。
█ 助攻—甲状腺营养素
甲状腺需要特定的营养才能正常运作;缺乏或过量摄入其中任何一项都可能导致甲状腺功能障碍。
△ 肠道菌群影响营养的吸收,包括微量元素
肠道菌群可以加工和分解食物,以便更好地吸收营养。与此同时,肠道菌群本身也需要营养来维持生命。某些菌以糖和碳水化合物为生,而其他细菌则以脂肪和其他矿物质为生,当这些微生物不平衡时,会影响营养获取。
△ 微量营养素对于健康的甲状腺至关重要
肠道微生物群的组成会影响身体吸收关键微量营养素的能力,例如碘、硒、锌、铁、B族维生素、维生素 A、酪氨酸等,所有这些微量元素对健康的甲状腺功能都是必不可少的。
△ 自身免疫性甲状腺疾病患者通常缺乏微量营养素
其中与甲状腺相关的特别重要的营养素是硒,碘,锌。如果体内有炎症、菌群失调等,那么这些营养素的吸收可能会被影响。
★碘:充足的碘对健康的甲状腺功能至关重要;然而,太少或太多都会将甲状腺推向甲状腺功能减退或甲状腺功能亢进。在世界范围内,碘缺乏是甲状腺功能减退症的最常见原因。推荐的每日碘摄入量(150 微克/天)。
★ 硒:硒是参与健康甲状腺功能的几种抗氧化酶的重要辅助因子。硒需要将 T4 转换为 T3。
低硒可能会降低甲状腺中的抗氧化保护机制,增加甲状腺对氧化应激的敏感性,从而增加甲状腺自身免疫病的风险,包括格雷夫斯病。缺硒会加剧因碘摄入不足而引起的疾病。
★ 锌:甲状腺激素的合成需要锌,缺锌会导致甲状腺功能减退。
碘、硒和甲状腺之间有着独特的关系。
一方面,碘摄入量的增加可能会加剧对甲状腺的免疫攻击,因此对于桥本氏病患者来说,补充碘并不是一件好事儿。
另一方面,当碘与硒一起服用时,不会发生同样的自身免疫性发作。通过平衡碘和硒的摄入量,可以避免那些负面的免疫影响。
这个过程的成功在很大程度上也取决于胆囊中初级胆汁酸的产生。这些初级胆汁酸在消耗脂肪后从胆囊分泌到小肠中,在那里肠道细菌将它们代谢成所谓的“次级胆汁酸”,从而增加脱碘酶的活性。更重要的是,这些胆汁酸依赖于上述矿物质硒,肠道和甲状腺健康问题患者通常会耗尽硒。
参与甲状腺激素代谢的最重要的初级和二级胆汁酸的组成
甲状腺功能减退症也会阻碍胆囊流出胆汁,从而进一步影响 T4/T3 转换。这种胆汁也具有天然抗菌作用,这可能进一步解释了甲状腺疾病与特定细菌性肠道感染(如SIBO)之间的联系。
█ 执行—免疫响应
肠道的另一个重要功能是承载体内 70% 的免疫组织。免疫系统的这部分统称为肠道相关淋巴组织。肠道相关淋巴组织包括几种类型的淋巴组织,这些组织储存免疫细胞,例如 T 和 B 淋巴细胞,它们进行攻击并产生针对抗原的抗体,抗原是免疫系统识别为潜在威胁的分子。
当肠道的这些保护功能中的任何一个受到损害时,就会出现问题。当肠道屏障变得可渗透时(即“肠漏综合征”),大的蛋白质分子会逃逸到血液中。由于这些蛋白质不属于肠道之外,身体会产生免疫反应并攻击它们。研究表明,这些攻击在桥本等自身免疫性疾病的发展中发挥作用。
健康的肠道微生物群会影响免疫系统,并且对甲状腺功能也有重要影响,特别是对桥本甲状腺炎和格雷夫斯等自身免疫性甲状腺疾病。
- 自身免疫性甲状腺病与消化道疾病的关联
桥本甲状腺炎和格雷夫斯病通常与特定的消化系统疾病共存,包括腹腔疾病和非腹腔小麦敏感性。研究表明,患有自身免疫性甲状腺疾病的人患乳糜泻的可能性是一般人群的 4-5 倍。这可以(至少部分地)通过肠道屏障功能受损来解释,这使得抗原更容易通过并在遗传易感个体中引发自身免疫性疾病。
最常见的自身免疫性甲状腺疾病是桥本氏症,约占甲状腺自身免疫性疾病的 90%。这意味着甲状腺正受到自身免疫系统的攻击。这与肠漏和分子模拟有关,它们会诱使身体攻击你自身的甲状腺。
研究表明,肠道微生物群的失调,会影响整体甲状腺健康,甚至导致和加剧桥本氏症。2007 年的一项研究发现,在有自身免疫性甲状腺功能减退症病史的人群中,54% 的人的 SIBO(小肠细菌过度生长)呼气测试呈阳性,而对照组的这一比例为 5%。
- 分子模拟
每当身体暴露在危险的外部入侵者面前时,免疫系统都会记住它的结构,特别是它的蛋白质序列,以便它可以对该病原体形成完美的防御并在未来识别它。
但是,免疫系统的识别系统并不完美。只要一个分子的结构和蛋白质序列足够相似,免疫系统就会被弄混,攻击身体组织的类似分子,从而导致自身免疫性疾病。
不幸的是,甲状腺有两种常见的分身,使其面临自身免疫攻击的风险:麸质和酪蛋白(一种在乳制品中发现的蛋白质),由于肠道渗漏,这两种物质很可能在血液中泛滥。
█ 质变—不活跃 T4 --> 活跃 T3
甲状腺激素强烈影响胃和小肠的紧密连接。这些紧密连接是两个细胞的紧密相关区域,它们的膜结合在一起形成肠道的不可渗透屏障。
T3 和 T4可以保护肠粘膜内层免受压力引起的溃疡形成。在另一项研究中,胃溃疡的内镜检查发现低 T3、低 T4 和逆T3 水平异常。
与甲状腺健康相关的最常被忽略的因素之一可能是 T4 到 T3 的转换。
甲状腺主要产生不活跃的 T4。它需要其他组织,例如肠道,才能将其转化为活性激素 T3,而 T3 负责能量、新陈代谢、体温等等。
- 肠道菌群帮助T4转化为T3
大约 20% 的 T4 在胃肠道中以 T3 硫酸盐 (T3S) 和三碘甲腺乙酸 (T3AC) 的形式转化为 T3。T3S 和 T3AC 转化为活性 T3 需要一种叫做肠道硫酸酯酶的酶。
肠道硫酸酯酶从何而来? 健康的肠道菌群。
肠道菌群失调,显著降低了 T3S 和 T3AC 向 T3 的转化。这就是肠道功能不佳的人可能有甲状腺症状但实验室结果正常的原因之一。
碘甲状腺原氨酸脱碘酶在 T4 向其活性形式 T3 的转化中起核心作用。据推测,肠道和肠道微生物群会影响这些酶的活性。
但可能还不止这些,因为在肠壁中发现了脱碘酶活性,并且至少一项动物研究表明肠道菌群具有结合甲状腺激素的能力。
█ 加剧—其他病征
胃酸过少或胃酸过低会增加肠道通透性、炎症和感染。研究表明,萎缩性胃炎(一种与胃酸过少有关的疾病)与自身免疫性甲状腺疾病之间存在很强的关联。
- 肠道功能对于甲状腺激素至关重要的例子
便秘会损害激素清除并导致雌激素升高,从而提高甲状腺结合球蛋白 (TBG) 水平并减少身体可用的游离甲状腺激素的量。
另一方面,甲状腺功能低下会减慢转运时间,导致便秘并增加炎症、感染和吸收不良。
循环中甲状腺激素水平低会导致肠道运动受损和便秘,从而使激素失衡的循环持续下去。
03 甲状腺影响肠道
➤ 甲状腺如何影响肠道/消化系统
口腔中产生富含酶的唾液开始分解食物,特别是淀粉。然而,研究表明,大量患有自身免疫性甲状腺疾病(如桥本氏病)的人缺乏足够的唾液并出现“口干”。
这部分是由于促炎细胞因子的过度产生,阻碍了唾液的正常产生。
甲状腺在胃酸的产生中也起着非常重要的作用,这会导致胃酸、营养缺乏等症状,以及其他消化系统疾病,如SIBO(小肠细菌过度生长)和 SIFO(小肠真菌过度生长)。
研究还表明,甲状腺功能减退症通过显著降低胃食管活动,导致胃肠功能障碍,因此,建议消化不良患者检查甲状腺功能。萎缩性胃炎与自身免疫性甲状腺疾病之间存在联系。
还有其他器官在适当吸收、分解大量和微量营养素方面发挥着至关重要的作用,这些过程也受到甲状腺健康的影响。
- 甲状腺影响肝脏
研究表明,肝脏是受甲状腺功能亢进症和甲状腺功能减退症影响最大的器官。如果肝脏功能不正常,消化就会停止。但如果没有健康的甲状腺,肝脏就无法发挥最佳功能。不健康的甲状腺会导致不健康的肝脏,这会影响胆囊并阻碍消化、营养吸收和 T4/T3 转换的过程。
➤ 甲状腺如何影响便秘
食物进入嘴巴,然后从另一端出来所需的时间,我们称之为转运时间。便秘患者通常转运时间较长,缓慢的转运会在雌激素清除方面造成一些问题。肝脏负责结合雌激素,然后将其释放到肠道中,以便在大便时将其排出体外。
问题在于,当这些结合雌激素在肠道中停留的时间过长时,某些生物体就能够取消肝脏所做的工作并将雌激素释放回循环中。
本质上,不是去消除雌激素,而是将其回收利用,而雌激素水平会继续上升。雌激素的升高会增加一种叫做 TBG(甲状腺结合球蛋白)的物质。这种过量的 TBG 会与活性 T3 激素结合,使其无法用于提供能量。
更糟糕的是,随着 T3 被 TBG 包裹,它会减慢肝脏的速度。肝脏可以处理较少的雌激素,而已经升高的雌激素会变得更高。这也是为什么以激素替代疗法或避孕药的形式添加雌激素通常会导致体重增加。
04 甲状腺功能异常的几大常见原因
- 自身免疫反应
自身免疫性甲状腺炎,或称桥本氏病,是一种身份识别错误的案例。
免疫系统将甲状腺误认为是外来病原体,并产生甲状腺抗体来攻击它,逐渐破坏甲状腺组织。这会显著损害甲状腺的功能,导致甲状腺激素水平低下,且导致甲状腺功能减退。
✦ 在美国每100人中约有5人患该病
自身免疫性甲状腺炎,女性发病率至少是男性的8倍。迄今为止,自身免疫是西方男性和女性甲状腺功能减退症的最常见原因,约占成人甲状腺功能减退症的 90%。
在西方,桥本氏病也是甲状腺肿的常见原因(而在世界其他地区,碘缺乏症常常是罪魁祸首)。
✦ 幽门螺杆菌感染与桥本氏病之间可能存在联系
在桥本氏病患者中发现了一种特别毒力的幽门螺杆菌菌株,治疗感染可降低甲状腺自身抗体。
这种幽门螺杆菌菌株可以引发甲状腺自身免疫,因为它和参与甲状腺激素合成的酶具有非常相似的基因序列。这种相似性可能会导致与甲状腺组织的破坏性交叉反应和随后的自身免疫。
2. 接触环境毒素
越来越多的研究表明,人类活动(如工业和农业)释放的人为污染物或毒素会干扰甲状腺功能。
甲状腺非常容易受到环境毒素的损害,并且很容易积累重金属和毒素(模拟甲状腺激素结构或含有卤素的毒素)。
✦ 重金属
镉、铅、汞和铝可以通过多种机制影响甲状腺。接触汞可能会干扰脱碘酶(脱碘酶在甲状腺激素的激活和失活中很重要),从而破坏甲状腺功能。汞接触的常见来源包括鱼类和贝类、牙科用汞合金、来自工业的空气中汞蒸气。
其中许多毒素会对甲状腺造成直接或间接损害:
- 干扰T4和T3的生产
- 减少可用的甲状腺受体
- 阻碍 T4 向 T3 的转化
- 在生产、转化和再吸收过程中引起其他问题
✦工业化学品
高氯酸盐、多氯联苯 (PCB) 和二恶英是常见的工业污染物,已被发现会破坏甲状腺功能。
✦ 杀虫剂和除草剂
杀虫剂和除草剂可以通过抑制甲状腺激素基因表达、阻碍甲状腺对碘的吸收、与甲状腺激素转运蛋白结合、减少细胞对甲状腺激素的吸收以及增加甲状腺激素从体内的清除来干扰甲状腺。
✦日常用品中的毒素
以下也会伤害到甲状腺的物质:
阻燃剂(存在于电脑和电视屏幕、家具、地毯衬垫等中);
增塑剂(双酚 A 和邻苯二甲酸盐等);
三氯生(洗手液中的一种抗菌化学物质);
全氟辛酸(来自不粘炊具和防污织物的 PFOA)
3. 肠道菌群失调
肠道与甲状腺之间的关系既深刻又复杂;肠道健康会影响甲状腺功能,反之亦然。
甲状腺疾病发展和治疗中重要因素之间的相互作用
(1)碘可能对微生物群有毒,微生物群影响碘的摄取。
(2)自身免疫性甲状腺疾病(AITD)患者改变了微生物群。另一方面,由细菌过度生长引起的漏肠综合征增加了AITD的患病率。
(3)菌群进行雌激素循环,男女菌群组成不同。
(4)肥胖导致菌群改变
✦ 肠道菌群在格雷夫斯病的发展中起着关键作用
格雷夫斯病患者的肠道微生物多样性较低,普氏菌和副流感嗜血杆菌的丰度较高,而Alistipes和粪杆菌的丰度较低。
肠道微生物可能通过以下几种机制影响自身免疫性甲状腺功能亢进症的进展:
- 患有格雷夫斯病的人表现出,参与产T细胞的肠道细菌的丰度较低,这有助于预防甲状腺自身免疫。
- 在大鼠研究中,肠道细菌可以调节肠道碘摄取、甲状腺激素降解和甲状腺激素的肠肝再循环,从而导致体内甲状腺激素水平的升高或降低。类似的过程很可能发生在人类身上。
- 格雷夫斯病患者表现出针对肠道病原体Yersinia enterocolitica和Helicobacter pylori的高水平抗体,这表明慢性肠道感染和随之而来的免疫失调可能促进甲状腺功能亢进的发病机制。
总之,这些发现表明肠道微生态失调可能是自身免疫性甲状腺功能亢进症发展的关键节点。
4. 血糖失衡
甲状腺功能亢进引起的新陈代谢增加,导致身体组织对葡萄糖的需求增加,通过肌肉中的糖原分解和肝脏中的糖异生增加内源性葡萄糖的产生。
在一些甲亢患者中,胰岛素抵抗的存在会影响多余葡萄糖的处理,这种现象是身体细胞对激素胰岛素反应不佳,不能轻易从血液中吸收葡萄糖。胰岛素抵抗和甲状腺功能亢进之间的联系机制尚未得到充分解释,但可能与甲状腺功能亢进中炎症信号分子的循环水平较高有关,这会损害胰岛素敏感性。
✦ 甲状腺和血糖之间相互影响
甲状腺会影响血糖代谢,如果甲状腺功能不正常,血糖平衡可能会失控,但血糖也会影响甲状腺。
研究表明,胰岛素抵抗(在长期高血糖人群中很常见)会增加桥本氏病患者甲状腺的破坏。
低血糖(低血糖)也会通过抑制垂体的功能来损害甲状腺健康(垂体产生 TSH,刺激甲状腺产生 T4 和 T3)。
如果患有代谢综合征,甲状腺功能也可能会受到影响。
饮食和生活方式的改变可以显著提高胰岛素敏感性,为甲状腺功能亢进症的功能医学治疗提供辅助支持。
5. 食物不耐受
麸质不耐症似乎与桥本氏病密切相关。许多患有桥本氏病的人还患有乳糜泻(一种自身免疫性疾病),而无麸质饮食可以改善甲状腺健康。
一项针对 280 名格雷夫斯病患者和 120 名桥本病患者的研究发现,5.5% 的患者抗麦胶蛋白抗体 (AGA) 呈阳性。这是一项具有统计学意义的发现,当然AGA 只是麸质敏感性的一个标志物,需要进一步研究。
格雷夫斯病患者也表现出高抗谷氨酸脱羧酶抗体,这表明对麸质敏感。研究人员指出,乳糜泻和自身免疫性甲状腺疾病具有共同的免疫机制。
✦ 为什么它们之间有关联?
麦胶蛋白是麸质的蛋白质部分,由于其分子结构与甲状腺组织相似,因此可能引发格雷夫斯病。当肠道屏障受损时(由于肠道菌群失调和抗生素的使用等因素),麦胶蛋白会逃离肠道,进入血液。在体循环中,免疫系统将麦胶蛋白标记为一种威胁,标志着它将被破坏;然而,在这个过程中,它也会不经意地“标记”甲状腺组织,并开始攻击甲状腺。
✦ 为什么建议甲状腺患者进行无麸质饮食?
乳糜泻影响 1% - 5% 的美国人,但许多人没有明显症状,并且可能不知道自己患有乳糜泻。
即使在非自身免疫性引起的甲状腺疾病患者中,分子模拟现象仍然会影响甲状腺功能。
食用麸质后,对麸质的免疫反应可持续长达六个月。
✦ 促甲状腺肿食物也会给甲状腺功能低下者带来问题
所谓“促甲状腺肿食物”是通过干扰甲状腺对碘的吸收而引起甲状腺肿大的食物。在低浓度时,可以通过补充碘来抵消致甲状腺肿的影响;但是大量的摄入会对甲状腺产生负面影响。
部分致甲状腺肿的食物包括:
- 十字花科蔬菜:如西兰花、花椰菜、卷心菜、白菜等
- 蔷薇科水果:如樱桃、桃子、覆盆子、草莓、杏等
- 其他食物,如红薯、竹笋、大豆和尤卡等
6. 下丘脑-垂体-肾上腺轴功能障碍和压力
甲状腺与 HPA 轴紧密相连。下丘脑产生 TRH,它刺激垂体产生 TSH,向甲状腺发出信号以产生 T4 和 T3。下丘脑和/或垂体的中断会干扰这一过程并影响甲状腺。
下丘脑-垂体-肾上腺轴(HPA 轴)是身体的中枢应激反应系统。HPA 轴协调皮质醇的释放,皮质醇是一种激素,可以让我们的身体对直接威胁做出快速反应。然而,慢性压力会破坏这一过程并导致 HPA 轴功能障碍。
✦ 慢性压力
慢性压力会促进炎性细胞因子的释放,从而降低下丘脑和垂体(进而降低甲状腺)的功能,抑制甲状腺激素的转换,导致甲状腺激素抵抗,并影响其他对正常甲状腺功能重要的激素。
细胞因子产生的改变也可能与自身免疫有关,如果你患有桥本氏病,就需要考虑HPA轴功能障碍和应激因素。
✦ 过度运动
需要注意的是,过度运动也会破坏 HPA 轴并可能加剧甲状腺功能减退症。过度、剧烈的运动会给你的身体带来压力,并可能对甲状腺健康产生负面影响。
7. 营养缺乏
鉴于麸质、免疫系统和甲状腺功能之间存在复杂的相互作用,因此甲状腺功能亢进症患者必须避免麸质。 然而,仅仅是无麸质饮食可能不足以纠正与甲状腺功能亢进相关的肠道菌群失调、慢性炎症和营养缺乏;这涉及到了我们接下来要讲的“AIP饮食”。
AIP饮食是指通过去除常见有问题的食物来治愈肠漏,从而减少体内炎症并治愈自身免疫性疾病。
✩ AIP饮食实践指南:
- 将水果限制在每天 1-2 份,并确保它们的升糖指数(碳水化合物消化速度的排名)较低;
- 每天包括 6-8 份蔬菜;
- 每顿饭的目标是 80% 的蔬菜和 20% 的肉或鱼;
- 专注于酱汁、蘸酱和肉汤;
- 加入大量油脂(椰子油、鸭油、牛油、鳄梨油、橄榄油),在适当的温度下煮熟;
- 不要在跑步时进食,并确保彻底咀嚼食物;
- 自己发酵蔬菜;
- 多喝过滤水;
- 检查食物标签,以确保是合规成分。
甲状腺需要特定的营养素才能正常运作;缺乏其中任何一项都可能导致甲状腺功能减退症。
✦ 维生素
除了前面章节节我们讲过的,硒,碘之类的微量元素之外,维生素也是必不可少的。
观察性研究将低维生素 D 与格雷夫斯病的发生联系起来;维生素 D 是一种有效的免疫调节剂。低水平的营养素可能使个体易患免疫失调,进而导致甲状腺自身免疫。<具体补充干预见下一章节>
8. 免疫系统在经历生育后发生变化
在女性中,在怀孕后出现自身免疫性甲状腺疾病的情况并不少见。
怀孕会增加T调节细胞的活性,这使得母亲的身体对在她体内生长的宝宝保持“耐受性”。然而产后,这种自然的免疫抑制状态就丧失了,免疫系统可能会向相反的方向倾斜,导致自身耐受性丧失,并产生针对自身组织(包括甲状腺)的自身抗体。
这就解释了为什么一些女性会在产后出现自身免疫性甲状腺疾病,包括桥本氏病和格雷夫斯病。
05 干预治疗方案
一、 干预可以从治愈肠道开始(肠道-甲状腺轴)
肠道修复的四个阶段:
- 去 除 刺 激 肠 道 的 诱 因
☑ 潜在的食物诱因
在3-6 周内,不食用任何可能的食物刺激物。从日常饮食中去除食物过敏原和其他可能的加重因素。比如:麸质、乳制品、玉米、大豆、坚果、豆类/豆类(包括花生)以及巧克力、红茶和咖啡等兴奋剂。
咖啡可能会与麸质发生交叉反应,刺激肠道。
减少致甲状腺肿食物的摄入量(减轻它们带来的危害);
选择合适的加工方式(煮沸和蒸煮可以减少食物的致甲状腺肿含量)。
☑ 药物
去除非甾体抗炎药、质子泵抑制剂 (PPI)、不必要的抗生素和节育措施。停药前请咨询医生。
☑ 生活压力
就像前面提到的,慢性压力实际上可以改变你的微生物组的构成。它还会扰乱 HPA 轴(下丘脑-垂体-肾上腺),影响体内几乎所有的激素。
☑ 肠道菌群检测
如果有任何慢性肠道或甲状腺问题,可以通过肠道菌群健康检测,了解自身菌群代谢或营养状况存在哪些异常,从而有针对性地进行干预。
2. 尝 试 消 化 酶
重要的消化酶会随着年龄的增长或使用不足而耗尽。当我们康复时,服用有针对性的消化酶一段时间会有所帮助。
☑ 甜菜碱盐酸盐
如果胃酸过少(胃酸过低)或吃得很饱,可能需要一些甜菜碱盐酸盐的帮助。可以询问医生。
☑ 考虑使用联合消化助剂
由消化酶和甜菜碱盐酸盐的混合物组合的产品,以支持蛋白质、脂肪和碳水化合物的最佳消化。可分解面筋和乳糖酶以消化乳制品。当患者在进食后出现胀气和腹胀、便秘或仅进食少量食物后有饱腹感时,餐前服用这类产品可能会有所帮助。
3. 重 塑 肠 道 菌 群
☑ 发酵蔬菜
这是让一些有益菌进入肠道的好方法。生的、培养的、有机蔬菜,如泡菜、酸菜和其他发酵蔬菜,如甜菜和胡萝卜,可以促进肠道中有益菌的生长。
☑ 益生菌
患有甲状腺疾病的女性可以考虑使用益生菌,如乳酸菌和双歧杆菌等。抵御病原体、增加有益免疫反应、保护胃肠道屏障功能并促进酶活性,可以更好地从食物中吸收营养。
注意:如果您的消化系统症状恶化,或者在引入益生菌食物或补充剂时出现极度胀气或腹胀,建议减少或不用益生菌,或遵医嘱。
☑ 可发酵纤维
食用富含可发酵纤维的食物可以改善肠道健康。比如苹果、柑橘类水果、胡萝卜、洋葱、大蒜、芦笋和绿色香蕉粉。
☑ 摄入足够的碘和硒
前面提到过,在饮食中摄入足够的碘和硒是避免补充的好方法。海鲜和碘盐是碘的良好来源,而巴西坚果是硒的极好来源。
4. 修 复
☑ 抗炎饮食
抗炎饮食对桥本氏病患者非常有益的。这种饮食不含引发免疫反应的食物,如茄属植物、鸡蛋、乳制品、谷物和豆类(仅举几例)。详见:谷禾健康:深度解析 | 炎症,肠道菌群以及抗炎饮食
☑ 有机食品
吃有机产品将帮助避免有害毒素,如杀虫剂、除草剂等。
☑ 姜黄素提取物
虽然吃姜黄有益于整体健康,但建议补充活性成分姜黄素的同时治愈肠道。
二、 干预措施(针对甲状腺问题)
- 药物选择
药物可能并非在所有情况下都必要,如果需要使用药物,提倡使用安全、剂量适当的药物来治疗特定的甲状腺和肠道健康状况。
2. 个性化的补充
肠道菌群检测后发现,很多有肠道/甲状腺问题的人都缺乏营养,通常建议除了改变饮食外,还应针对性补充一些优质维生素和微量元素(铁、硒、锌等)。
☑ 维生素
抗氧化营养素,如维生素 C 和 E,对于减轻格雷夫斯病中的过度氧化应激至关重要。
维生素 D 缺乏在格雷夫斯病患者中很常见,补充可能对格雷夫斯病复发具有保护作用。
☑ 微量元素
前面章节已提到过碘、硒等微量元素及相应的功能。它们可能存在于以下食物:
☑ 其他
omega-3 脂肪酸、二十碳五烯酸 (EPA) 和二十二碳六烯酸 (DHA) 以及谷胱甘肽具有抗炎和抗氧化特性,可能有助于抵消与甲状腺功能亢进相关的过度氧化应激。
左旋肉碱是一种类似氨基酸的物质,每天 2-4 克的高剂量可抑制 T4 和 T3 进入细胞核,从而降低甲亢的影响。左旋肉碱生物利用度最高的形式是乙酰左旋肉碱。
蜂草和柠檬香脂等植物药也被用来平衡甲状腺功能亢进,并且可能与其他饮食和生活方式改变一起作为有用的辅助治疗。
3. 生活方式的改变
☑ 管理压力
减轻慢性压力可以帮助缓解导致甲状腺问题的任何 HPA 轴功能障碍。瑜伽、冥想、呼吸练习和正念等措施都可以产生效果。
☑ 养成良好的睡眠习惯
睡眠是整体健康的必要条件,也是肠道健康的先决条件。争取每晚睡 8 小时左右,在凉爽、黑暗的房间里安静地入眠,并限制接触人造光。
☑ 制定可持续的锻炼计划
定期锻炼有益于肠道健康、血糖代谢正常,缓解压力,但需要注意的是要达到适当的平衡,不要过度训练。
☑ 足够的阳光
阳光照射已被证明对自身免疫性疾病具有保护作用。
☑ 优质水源
反渗透过滤器可以有效去除对甲状腺有害的毒素,如高氯酸盐、杀虫剂、多氯联苯、各种重金属等。
☑ 限制塑料的使用
尽可能不要饮用塑料容器中的食物或将食物存放在塑料容器中。如果确实需要选择使用某些塑料产品,请寻找“不含 BPA”的选项。当然,不含 BPA 的产品可能仍然含有其他潜在干扰甲状腺作用的双酚衍生物。
生活方式的改变是甲状腺功能亢进症康复的基本要素,通过日常减压练习来管理压力,获得充足的高质量睡眠,定期进行健身活动,保持健康的免疫功能,这是为治愈甲状腺问题和长期维持健康的先决条件。
我们可以看到,甲状腺功能亢进的诊断不一定需要导致终生依赖药物、侵入性手术或完全破坏甲状腺功能。通过功能医学方法(包括肠道健康检测,个性化饮食及生活方式干预等),不仅可以缓解甲状腺功能亢进的症状,还可能逆转导致甲状腺功能亢进的潜在疾病。
主要参考文献:
Knezevic J, Starchl C, Tmava Berisha A, Amrein K. Thyroid-Gut-Axis: How Does the Microbiota Influence Thyroid Function? Nutrients. 2020 Jun 12;12(6):1769. doi: 10.3390/nu12061769.
Fröhlich E, Wahl R. Microbiota and Thyroid Interaction in Health and Disease. Trends Endocrinol Metab. 2019 Aug;30(8):479-490. doi: 10.1016/j.tem.2019.05.008. Epub 2019 Jun 27. PMID: 31257166.
Soldin OP, O'Mara DM, Aschner M. Thyroid hormones and methylmercury toxicity. Biol Trace Elem Res. 2008;126(1-3):1-12. doi:10.1007/s12011-008-8199-3
Croce L, Di Dalmazi G, Orsolini F, et al. Graves' Disease and the Post-partum Period: An Intriguing Relationship. Front Endocrinol (Lausanne). 2019;10:853.
Richardson VM, Staskal DF, Ross DG, Diliberto JJ, DeVito MJ, Birnbaum LS. Possible mechanisms of thyroid hormone disruption in mice by BDE 47, a major polybrominated diphenyl ether congener. Toxicol Appl Pharmacol. 2008 Feb 1;226(3):244-50.
Sapolsky RM, Krey LC, McEwen BS. The neuroendocrinology of stress and aging: the glucocorticoid cascade hypothesis. Endocr Rev. 1986 Aug;7(3):284-301. doi: 10.1210/edrv-7-3-284. PMID: 3527687.
Duntas LH. The Role of Iodine and Selenium in Autoimmune Thyroiditis. Horm Metab Res. 2015 Sep;47(10):721-6. doi: 10.1055/s-0035-1559631. Epub 2015 Sep 11. PMID: 26361258.
Sanna, A.; Firinu, D.; Zavattari, P.; Valera, P. Zinc Status and Autoimmunity: A Systematic Review and Meta-Analysis. Nutrients 2018, 10, 68.
Shahbaz A, Aziz K, Umair M, Sachmechi I. Prolonged Duration of Hashitoxicosis in a Patient with Hashimoto's Thyroiditis: A Case Report and Review of Literature. Cureus. 2018;10(6):e2804. Published 2018 Jun 14. doi:10.7759/cureus.2804
de Herder WW, Hazenberg MP, Pennock-Schröder AM, Oosterlaken AC, Rutgers M, Visser TJ. On the enterohepatic cycle of triiodothyronine in rats; importance of the intestinal microflora. Life Sci. 1989;45(9):849-56.
Abbott RD, Sadowski A, Alt A3. Efficacy of the Autoimmune Protocol Diet as Part of a Multi-disciplinary, Supported Lifestyle Intervention for Hashimoto’s Thyroiditis. Cureus. 2019 Apr 27;11(4):e4556. doi: 10.7759/cureus.4556.
P. Monteleone, D. Parrini, P. Faviana et al., “Female infertility related to thyroid autoimmunity: the ovarian follicle hypothesis,” The American Journal of Reproductive Immunology, vol. 66, no. 2, pp. 108–114, 2011
Mugunthan K, Mugunthan N, van Driel ML. Treatment for subclinical hyperthyroidism in adults. Cochrane Database Syst Rev. 2018;2018(7):CD010371. Published 2018 Jul 26. doi:10.1002/14651858.CD010371.pub2