如何在细胞疗法CAR-T靶点同质化激烈竞争中突围?
6月22日,NMPA公示,复兴凯特CD19靶点自体CAR-T细胞治疗产品阿基仑赛注射液正式获批,这意味着我国迎来首款获批上市的CAR-T细胞治疗产品。
Insight数据库显示,目前有20多家企业布局“重押”CAR-T疗法,包括药明巨诺、科济制药、传奇生物、上海优卡迪生物、恒润达生生物、驯鹿医疗等,已进入临床阶段的项目36个,但CAR-T疗法布局的靶点主要聚焦在CD19、BCMA,CAR-T靶点同质化程度较为严重,如何在细胞疗法CAR-T靶点同质化激烈竞争的格局中突围呢?
今天,我们就来聊聊CAR-T细胞疗法的“姊妹“—NK细胞免疫疗法。
NK细胞可非特异性直接杀伤肿瘤细胞,这种天然杀伤活性无MHC限制,不依赖抗体,也不需要抗原致敏,NK细胞还具有很强的免疫调节功能,与机体其他多种免疫细胞相互作用,调节机体的免疫状态和免疫功能。NK细胞疗法作为一种可行的治疗策略,逐渐成为仅次于T细胞疗法的免疫新星。
NK细胞的抗肿瘤途径
NK细胞与T细胞、B细胞不同,NK细胞不需要特异性的抗原致敏刺激就可识别并杀伤靶细胞。可通过多种途径抑制肿瘤细胞的生长和扩散:
1)在肿瘤微环境趋化因子和黏附因子的引导下,NK细胞募集到肿瘤发生的部位,促使肿瘤组织中NK细胞浸润程度增加,使得NK细胞表面活化受体识别肿瘤细胞表面相应配体,释放穿孔素、颗粒酶等杀伤介质,直接杀伤肿瘤细胞;
2)活化的NK细胞可表达死亡诱导配体-Fas配体(FASLG,又称 TNFSF6),可与肿瘤坏死因子相关诱导凋亡配体(TNF related apoptosis inducing ligand,TRAIL)结合,诱导肿瘤细胞凋亡;
3)通过抗体依赖性细胞介导的细胞毒作用(antibody dependent cell-mediated cytotoxicity,ADCC),NK细胞通过细胞表面的FcγRIII(CD16)和肿瘤抗原特异性抗体Fc段结合,识别并杀伤肿瘤细胞;
4)NK细胞通过产生细胞因子(IFNγ、TNFα、IL1、IL10、GM-CSF等)和趋化因子(CCL3、CCL4)将其他免疫细胞募集到炎症部位,诱导其活化,并增殖产生固有和适应性免疫应答。
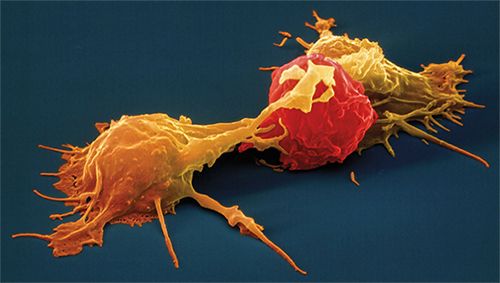
图1|NK 细胞(黄色部分)攻击肿瘤细胞(红色部分)[1]
NK细胞的来源
目前治疗性NK细胞的来源比较广泛,包括自体NK细胞和替代性NK细胞,后者包括脐带血NK细胞、干细胞来源的NK细胞、细胞因子诱导的记忆样NK细胞和嵌合抗原受体(CAR)-NK细胞。由于细胞的分离、转导和扩增过程中面临的挑战,原代NK细胞并不是产生CAR细胞产物的理想原料。因此,CAR-NK细胞的临床试验目前主要集中于干细胞或祖细胞来源的产品上。
同立海源生物自主研发的AMMS®NK细胞培养试剂盒套装,国内首款通过美国FDA DMF II类备案,备案号DMF 035588。该款试剂盒采用自体外周血或脐血细胞中分离得到的单个核细胞,经体外操作使NK细胞活化扩增,最终得到高纯度高效应的NK细胞。经过大量的测试数据表明,该款试剂盒处于国内领先地位。
NK细胞免疫疗法
目前,NK细胞抗肿瘤的研究正在如火如荼地开展,主要包括:
1)针对NK细胞抑制型或激活型受体的单克隆抗体(monoclonal antibody,mAb);
2)联合NK细胞和单抗药(如免疫检查点抑制剂、免疫因子)来诱导抗体特异的细胞毒性;
3)NK细胞过继性免疫疗法。
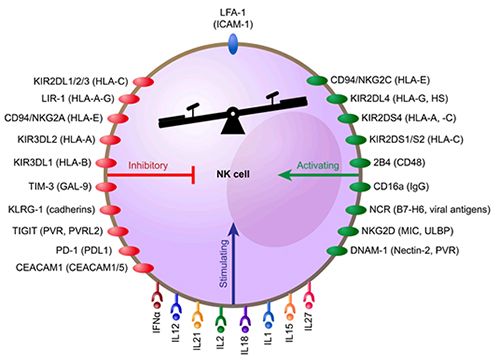
图2| NK细胞的活化受体、抑制受体及其功能和配体[2]
NK细胞的下方显示NK细胞的细胞因子和相应的细胞因子受体。抑制受体(红色)与相应的配体(括号中)显示在NK细胞的左侧,活化受体(绿色)与相应的配体(括号中)显示在NK细胞的右侧,NK细胞上的LFA-1(蓝色)与靶细胞上的ICAM-1结合,将向靶细胞释放颗粒酶,这是有效裂解靶细胞所必需的。
1)靶向NK细胞的单克隆抗体
NK细胞对肿瘤的识别主要依赖于其表达的多种激活受体和抑制受体,两者间的平衡决定着NK细胞的杀伤作用。
NK细胞表面的激活受体包括NKG2D(也称为 CD314 和 KLRK1)、DNAM-1(也称为 CD226)、天然细胞毒性受体 (NCRs)、FcγRIII (CD16)等,这些激活受体结合配体后,能引发细胞因子如IFN-γ、TNF-α的分泌。以NK细胞表面活化受体CD16/NKG2D为靶点的双特异性分子、TAA/CD16/NKG2D、TAA/CD16/NKp46三特异性抗体等,可以靶向NK细胞识别并杀伤肿瘤细胞。
NK细胞表面的抑制受体包括NKG2A/CD94、TIGIT、PD1、KIR2DL1/2/3等,与MHC-I类分子结合,可抑制NK细胞活化,如在研人源化抗抑制受体单克隆抗体IPH2101。
2)基于免疫检查点抑制剂、细胞因子的免疫疗法
NK细胞作为杀伤肿瘤细胞的免疫武器,需要找到肿瘤细胞才能够发挥作用。肿瘤细胞表面表达的应激蛋白是NK细胞的识别标记,但肿瘤细胞会通过蛋白脱落躲避免疫系统的监视,主要是MICA和MICB两类蛋白,免疫检查点抑制剂,可解除NK细胞的抑制信号,靶向MICA 和 MICB的抗体可增加癌细胞表面MICA 和MICB的水平,让NK细胞能够有效识别肿瘤。免疫检查点抑制剂还包括T细胞免疫球蛋白粘蛋白受体3(TIM-3)、淋巴细胞激活基因3(LAG-3)。基于细胞因子的免疫疗法主要包括IL-2疗法、IL-15疗法和TGF-β抑制剂。
众所周知,IL-2可以诱导NK细胞的增殖,提高其溶细胞活性,基于IL-2的免疫疗法已被批准用于治疗一小部分转移性肾细胞癌、黑色素瘤以及急性髓细胞性白血病患者。在靶向NK细胞方面,IL-15可能比IL-2更具优势。IL-15可以扩增NK细胞群并增加NK细胞活化受体的表达,而不诱导Treg细胞群的扩增。TGF-β是机体内一个能调节细胞生长和分化等多种生物学效应的重要家族,其Ι型和Ⅱ型受体是一类丝氨酸/苏氨酸激酶糖蛋白。Ι型TGF-β受体抑制剂Galunisertib对AML和结肠癌均有效,其能促进NK细胞上NKG2D表达的恢复,以及TNF、IFN-γ的释放。
3)NK细胞过继性免疫疗法
NK细胞过继性免疫疗法是细胞生物治疗方法之一,通过向肿瘤患者回输经体外诱导培养的NK细胞,使其在机体中发挥直接或间接杀伤肿瘤细胞的作用,从而达到治疗肿瘤的目的。目前主要包括自体NK细胞输注、同种异体NK细胞输注和CAR-NK细胞疗法。
CAR-NK即通过基因工程修饰,在NK细胞表面表达能够和肿瘤特异性抗原结合的CAR,回输后能够特异性识别带有特定抗原的肿瘤细胞,引发免疫反应从而达到清除肿瘤细胞的目的。血液肿瘤特异性靶点包括CD19、CD20、CD33、CD138、CS-1、CD-5、EBNA3C等,实体瘤特异性靶点包括HER2、GD2、PSCA和EGFRvIII等。
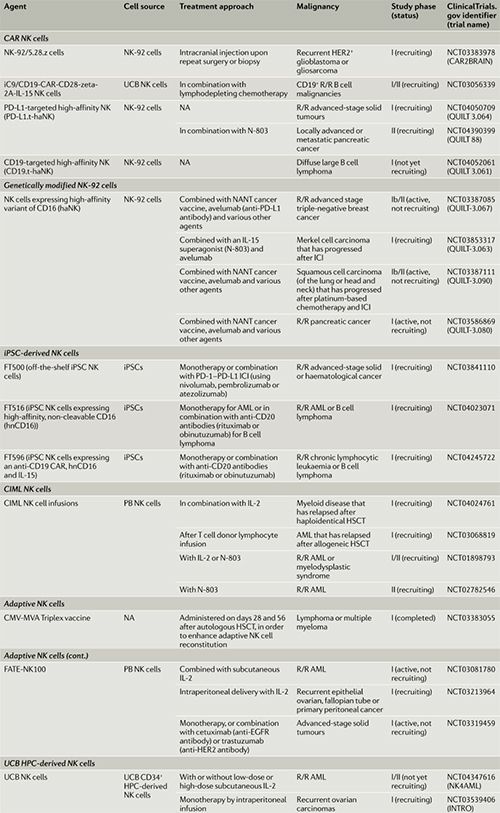
表1|部分正在进行的治疗性NK细胞产品的临床试验[3]
表2| 部分NK细胞衔接器和NK细胞定向细胞因子疗法临床试验[3]
NK细胞疗法近5年融资大事件
随着NK细胞疗法临床价值的凸显,无论是生物技术初创公司还是制药巨头,纷纷布局NK细胞疗法赛道,想了解NK细胞免疫疗法在研企业的小伙伴,点击这里。据不完全统计,近年来国内外NK细胞领域交易额累计达到50亿美元。从资本动态来看,多数NK细胞疗法企业的融资处于种子轮到B轮之间。无论是产品临床研究还是资本支持,NK细胞疗法都有很大的上升空间。相对于拥挤火热的T细胞疗法赛道,NK细胞疗法正处方兴未艾的阶段,随着基础研究的深入和资本的持续助力,NK细胞疗法将是一个面向百亿蓝海市场的朝阳产业。
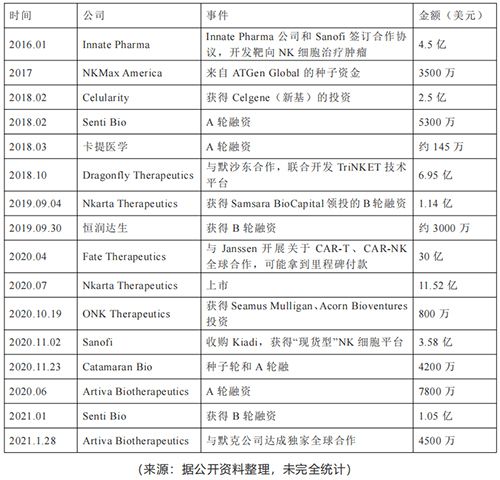
表3|近5年NK细胞疗法合作、融资大事件
小结:
NK细胞作为固有免疫中重要的效应细胞,具有强大的抗肿瘤功能,基于NK细胞的免疫疗法研究也正如火如荼地展开,随着对NK细胞的分子特征和功能的进一步探索,基于NK细胞靶向免疫治疗将成为肿瘤免疫治疗的新突破。
参考文献:
[1] Mitch Leslie. Engineered natural killer cells may be the next great cancer immunotherapy. Secience. 2018. doi:10.1126/science.aav4154.
[2] Carlsten M, Järås M. Natural Killer Cells in Myeloid Malignancies: Immune Surveillance, NK Cell Dysfunction, and Pharmacological Opportunities to Bolster the Endogenous NK Cells. Front Immunol. 2019 Oct 11;10:2357.
doi: 10.3389/fimmu.2019.02357.
[3] Myers, J.A., Miller, J.S. Exploring the NK cell platform for cancer immunotherapy. Nat Rev Clin Oncol. 18, 85–100 (2021). https://doi.org/10.1038/s41571-020-0426-7.