从 PK/PD 角度浅谈新冠肺炎患者治疗中奈诺沙星用药方案合理性
李鑫1,2,3,徐晓勇4,陈渊成3,5*
(1 复旦大学附属华山医院抗生素研究所, 上海, 200040; 2 卫健委抗生素临床药理重点实验室, 上海, 200040; 3 国家老年疾病临床医学研究中心, 上海, 200040; 4 浙江医药股份有限公司, 绍兴, 312366; 5 复旦大学附属华山医院一期临床研究室, 上海, 200040)
(* 通讯作者: 联系电话: 021-54602085, Email: [email protected])
(第一作者: 联系电话: 021-52888193, Email: [email protected])
近日,《柳叶刀-呼吸病学》杂志在线发表的通讯文章《2019 冠状病毒发热门诊的治疗和分流策略》提到,对诊断为病毒性肺炎且伴呼吸困难、缺氧的患者,使用呼吸喹诺酮 (莫西沙星和左氧氟沙星)+阿比朵尔治疗未好转时,考虑采用抗病毒+抗菌 (肺炎链球菌和金葡菌) 的核心治疗方法,其中推荐奈诺沙星作为抗感染治疗选用药物之一,给药方案 750 mg,每日一次 [1] 。本文将从药动学 (Pharmacokinetics, PK)、药效学 (Pharmacodynamics, PD) 和 PK/PD 角度介绍奈诺沙星,据此阐述对奈诺沙星治疗方案的看法。
奈诺沙星在健康受试者中药动学线性特征明显,消除速度适中,在体内广泛分布。多剂口服苹果酸奈诺沙星胶囊 500 mg 或 750 mg,每日一次,连续 10 天,在体内基本无蓄积 (表 1);达稳态时药动学参数与首剂给药接近,峰浓度分别为 7.0 和 9.1 mg/L,半衰期约 12 h。
表 1:多剂口服不同剂量奈诺沙星药动学参数
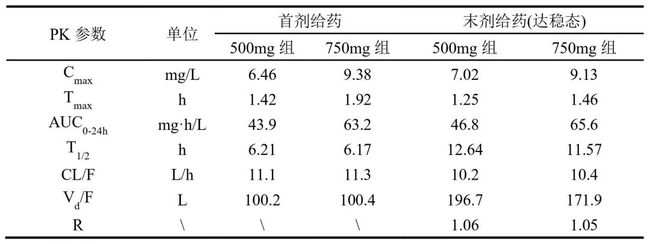
注: R 蓄积系数
奈诺沙星在 CAP 患者中的药动学与健康受试者类似。每日口服奈诺沙星 500 mg 或 750 mg 后,连续 10 天,峰浓度分别为 4.8 mg/L 和 7.2 mg/L,AUC0-24 h 分别为 46.9 mg·h/L 和 70.0 mg·h/L,T1/2 约 9 h[2]。
2. 药效学
体外抗菌作用研究显示,奈诺沙星对 PRSP 和 MRSA 具有高度抗菌活性。奈诺沙星对临床分离 PRSP 的 MIC50 和 MIC90 均为 0.06 mg/L,优于左氧氟沙星,与莫西沙星相仿;对 MRSA 的 MIC50 和 MIC90 分别为 0.5 mg/L 和 1 mg/L,优于左氧氟沙星和莫西沙星,与万古霉素和利奈唑胺相当[3]。对于 CAP 其他常见病原菌如肺炎克雷伯菌和肺炎支原体也显示良好体外抗菌活性 (表 2)[4]。CAP 患者感染的革兰阳性菌主要为肺炎链球菌和金葡菌。III 期临床试验研究中,奈诺沙星对这两种菌 MIC90 均为 0.125 mg/L,提示具有良好抗菌活性[5]。
表 2:奈诺沙星体外药敏结果 (单位: mg/L)

MIC: 最低抑菌浓度
苹果酸奈诺沙星胶囊 II 期临床试验采用多中心、随机、双盲双模拟、平行对照设计,分为试验药奈诺沙星 500 mg 组和 750 mg 组,以及对照药左氧氟沙星 500 mg 组,均为每日一次,连续 7~10 天口服给药,治疗社区获得性肺炎。累计入组中国成人 CAP 患者 192 例,三组临床治愈率分别为 93.3%,87.3% 和 88.5%,奈诺沙星 500 mg 与 750 mg 治疗 CAP 的临床疗效不劣于左氧氟沙星 500 mg。其中,入组的 4 例金葡菌感染 CAP 患者中 3 例为 MRSA 感染,2 例在奈诺沙星 500 mg 组,1 例在奈诺沙星 750 mg 组,均成功治愈。三组的微生物清除率分别为 83.3%、83.3% 和 80.0%,三组之间微生物清除率均无统计学差异 (P>0.05)。结果提示,奈诺沙星 500 mg 以及 750 mg 口服 7~10 天疗程对 CAP 具有良好的临床和微生物学疗效[6]。
3. PK/PD
奈诺沙星 PK/PD 特点主要为浓度依赖性。目前已报道的奈诺沙星 PK/PD 研究均采用体外模型研究靶值或喹诺酮类药物靶值。体外 PK/PD 研究表明,PK/PD 指数 fAUC0-24 h/MIC、fCmax/MIC 和%fT>MIC 与奈诺沙星抗菌作用均有良好相关性 (f 为游离分数),使菌落计数降低至基线千分之一的靶值分别为 47.05,5.07 和 54.3%[7]。其他喹诺酮类抗菌药物动物 PK/PD 研究多有报道,疗效相关 PK/PD 指数为 fAUC/MIC 和 fCmax/MIC,对肺炎链球菌达到抑菌作用的靶值为 fAUC0-24 h/MIC = 25~50,对葡萄球菌和革兰阴性菌为 fAUC0-24 h/MIC ≥ 80~125 及 fCmax/MIC>10[8]。
奈诺沙星 500 mg 和 750 mg 给药方案对肺炎链球菌AUC0-24 h/MIC90 分别为 375 和 560,Cmax/MIC90 为 38.5 和 57.5,均高于文献报道靶值;对金葡菌的 AUC0-24 h/MIC90 分别为 93.8 和 140,Cmax/MIC90 为 9.6 和 14.4,500 mg 给药后 PK/PD 指数与靶值相近,750 mg 可达靶值以上。以 fAUC0-24 h/MIC = 47.05 为靶值进行蒙特卡洛模拟,奈诺沙星 500 mg,每日一次连续 10 天口服给药对肺炎链球菌和金葡菌累积响应百分率 (Cumulative fraction of response,CFR) 分别为 98% 和 95%,提高剂量至 750 mg 后均可达 99% 以上;对于 MIC ≤ 0.5 mg/L 的菌株,500 mg 连续给药达标概率 (Probability of target attainment,PTA) 可达 98% 以上,750 mg 接近 100% (图 1)。对于 MIC ≤ 1 mg/L 的菌株,500 mg 连续给药 PTA 仅为 20%,750 mg 为 80% (图 1)。文献报道,喹诺酮类抗菌药对金葡菌靶值通常高于 47.05,因此,对于 MIC 为 1 mg/L 的金葡菌感染,实际 PTA 低于 80%[9]。
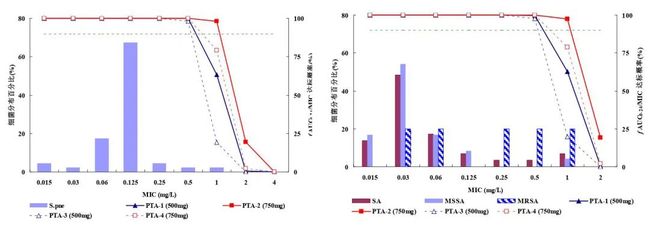
图 1:奈诺沙星对肺炎链球菌(左图)和金黄色葡萄球菌(右图)的 MIC 分布及其 fAUC0-24/MIC 达标概率 (PTA) 曲线 [实线和虚线分别代表靶值取 35(菌落计数降至基线 10%) 和 47(菌落计数降至基线 1‰), 柱状图表示 MIC 分布频率,水平虚线表示 90% 达标概率)
PK/PD 分析结果显示,奈诺沙星 500 mg 和 750 mg 连续给药治疗肺炎链球菌和金葡菌感染 CAP 预期可获得良好临床和微生物疗效。与 500 mg 相比,750 mg 给药提高达标概率,对于 MIC 较高的菌株 (如 1 mg/L) 引起的感染仍可获得较好治疗效果。
4. 安全性
一项 II 期临床研究中,奈诺沙星 500 mg 和 750 mg 给药组发生的与试验药物有关的不良事件 (adverse event, AE) 均为轻度或中度,包括食欲缺乏、恶心、呕吐、胃部不适等,患者可耐受。三个给药组 (奈诺沙星 500 mg、奈诺沙星 750 mg 和左氧氟沙星 500 mg) 药物相关不良事件发生率分别为 30.6%, 35.6% 和 25.0%,差异无统计学意义 (P>0.05)[6]。奈诺沙星全面 QT 临床研究显示,单剂口服奈诺沙星 500 mg 和 750 mg、莫西沙星 400 mg 后经基线和安慰剂校正的 QTc 间期(ΔΔQTc)改变分别为 8.1ms、10.4ms 和 13.6ms,提示奈诺沙星 500 mg 无 QTc 间期延长风险,750 mg 有潜在延长风险 (通常认为 5~10ms 之间无风险,10~15 mg 之间有潜在风险)[10]。考虑到 II 期临床试验中 500 mg 组不良反应发生率略低于 750 mg 组及 500 mg 无 QTc 间期延长风险,采用 500 mg 作为 III 期临床试验剂量。III 期临床试验研究中,500 mg 组药物相关 AE 发生率为 19.4%[11]。表 3 对两项 II 期和一项 III 期口服奈诺沙星临床试验中药物相关 AE 进行总结,其中最常报告的包括中性粒细胞减少、恶心、丙氨酸转氨酶升高和白细胞减少等[12]。
表 3:口服奈诺沙星药物相关不良事件(≥ 1%) (点击查看大图)

a 包括中性粒细胞百分比或计数降低和中性粒细胞减少症
b 包括白细胞计数减少和白细胞减少症
c 包括 QT 间期延长和校正 QT 间期延长
d 包括血小板计数增加和血小板增多症
5. 新冠肺炎患者治疗方案
柳叶刀论文提出奈诺沙星用于阿比朵尔+莫西沙星/左氧氟沙星治疗后仍进展恶化的患者,给药方案为 750 mg,每日 1 次,从 PK/PD 角度看临床可以采用该剂量方案,但需考虑如下几点: ①750 mg 尚未开展验证性临床研究,仅开展了探索性临床研究,纳入 59 例患者;②健康人研究显示 750 mg 有潜在的 QTc 间期延长风险,此对病毒性肺炎患者可能同样适用;③病毒性肺炎患者需有明确病原学诊断依据和体外药敏结果,支持使用喹诺酮抗菌药。
综上所述,奈诺沙星胶囊 500 mg 和 750 mg 对 CAP 患者均有良好的有效性和安全性。500 mg 有 357 例确证性临床试验证据,且安全性比 750 mg 略好,可首先推荐用于合并细菌感染患者的治疗。PK/PD 分析提示对于 MIC 较高(例如 MIC = 1 mg/L)的菌株引起的感染,750 mg 仍可获得较好的治疗效果。对于 500 mg 治疗无好转,怀疑或病原学诊断为 PRSP 和 MRSA 感染的患者,临床医生可使用奈诺沙星 750 mg,每日一次给药方案,在关注疗效的同时,应将患者安全性放在首要地位。
参考文献:
[1] Zhang J., Zhou L., Yang Y., et al., Therapeutic and triage strategies for 2019 novel coronavirus disease in fever clinics. Lancet Respir Med, Published Online February 13, 2020 https://doi.org/10.1016/ S2213-2600(20)30071-0.
[2] 武晓捷. 抗菌新药苹果酸奈诺沙星胶囊群体药代动力学及药代动力学/药效学研究 [D]. 复旦大学, 2012.
[3] 朱德妹, 吴培澄, 胡付品, 等. 奈诺沙星体外抗菌作用研究 [J]. 中国感染与化疗杂志, 2015(02): 97-112.
[4] Wang N., Liu W., Zhou Y., et al., In vitro activities of nemonoxacin and other antimicrobial agents against human Mycoplasma and Ureaplasmas isolates and their defined resistance mechanisms[J]. Front Microbiol. 2019, 10: 1890.
[5] 评价口服苹果酸奈诺沙星对比左氧氟沙星治疗成人社区获得性肺炎患者的有效性和安全性的多中心、随机、双盲双模拟、平行对照 III 期临床研究报告, 2012.
[6] Liu Y., Zhang Y., Wu J., et al., A randomized, double-blind, multicenter Phase II study comparing the efficacy and safety of oral nemonoxacin with oral levofloxacin in the treatment of community-acquired pneumonia[J]. J Microbiol Immunol Infect, 2017, 50(6): 811-820.
[7] Liang W., Chen Y., Cao Y., et al., Pharmacokinetics and pharmacodynamics of nemonoxacin against Streptococcus pneumoniae in an in vitro infection model[J]. Antimicrob Agents Chemother, 2013, 57(7):2942-2947.
[8] David H. W, Gigi H.B, Marnie L. P, et al. Application of fluoroquinolone pharmacodynamics[J]. J Antimicrob Chemother, 2000, 46:669-683.
[9] 陈渊成. 数学模型与计算机仿真技术在喹诺酮抗菌新药临床研究中的应用. 复旦大学. 博士后研究工作报告. 2013.
[10] Zhao C., Lv Y., Li X., et al., Effects of nemonoxacin on thorough ECG QT/QTc interval: a randomized, placebo- and positive-controlled crossover study in healthy Chinese adults[J]. Clin Ther, 2018. 40(6): 983-992.
[11] Yuan J., Mo B., Ma Z., et al., Safety and efficacy of oral nemonoxacin versus levofloxacin in treatment of community-acquired pneumonia: a phase 3, multicenter, randomized, double-blind, double-dummy, active-controlled, non- inferiority trial [J]. J Microbiol Immunol Infect, 2019. 52(1): 35-44.
[12] Cheng S., Wu R., Chuang Y., et al. Integrated safety summary of phase II and III studies comparing oral nemonoxacin and levofloxacin in community- acquired pneumonia[J]. J Microbiol Immunol Infect, 2019, 52(5): 743-751.
责任编辑:刘恩茂、苏越 题图来源:站酷海洛