抗体基本知识
一、免疫基础
1. 抗原(Ag)定义:能够刺激机体产生免疫应答的物质。即能够特异性结合T细胞表面受体TCR或B细胞表面受体BCR,并能够活化T细胞或B细胞,从而产生效应T细胞或浆细胞进而产生抗体,并且在体内能够和效应T细胞或抗体相互结合作用。
2. 抗体(Ab)定义:通过抗原刺激B细胞分化成浆细胞从而产生能够和抗原特异性结合的免疫球蛋白。(免疫球蛋白Ig=抗体Ab)
3. 抗体产生通路:简单来说,就是抗原呈递细胞(APC cells)将抗原呈递给辅助T细胞(T helper/Th cells), 再由Th细胞分泌刺激因子刺激B细胞成浆细胞,从而产生抗体。
二、抗体结构
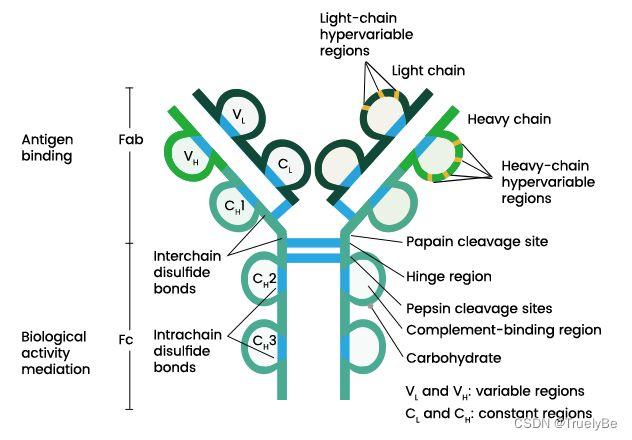
1. 抗体是由两条轻链和两条糖基化重链组成的同源多聚体。轻链和重链之间,以及重链和重链之间靠二硫键进行组装。
2. 轻链通常无糖基化修饰,分子量约为24 kD。有两个链内二硫键。分为κ型和λ型。轻链由可变区VL和恒定区CL组成。
3. 重链分子量约为55-75 kD。有4-5个链内二硫键。分为μ、γ、α、δ、ε五个亚型。重链由可变区VH、恒定区CH1、CH2、CH3组成。
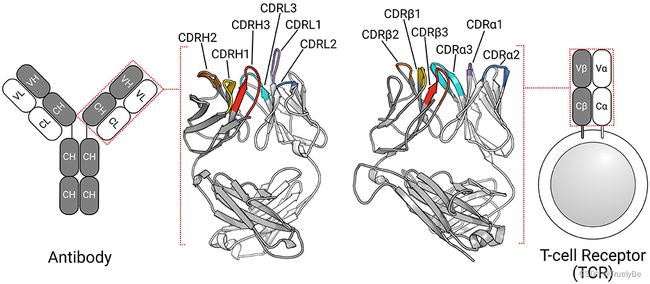
4. 可变区VH/VL又可分为互补决定区CDR(CDR1、CDR2、CDR)和骨架区FR。
5.关于Fc区的功能,后续会单独开一章来讲。
6. hinge为铰链区,木瓜蛋白酶切up-hinge可得到两个Fab和1个Fc;胃蛋白酶切down-hinge可得到一个F(ab')2和一个无活性pFc'
三、抗体分类
1. 最大的分类:可以把抗体分为膜型和分泌型。
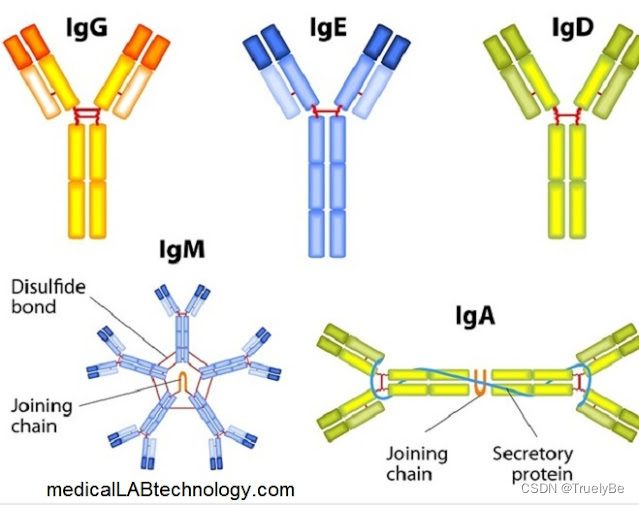
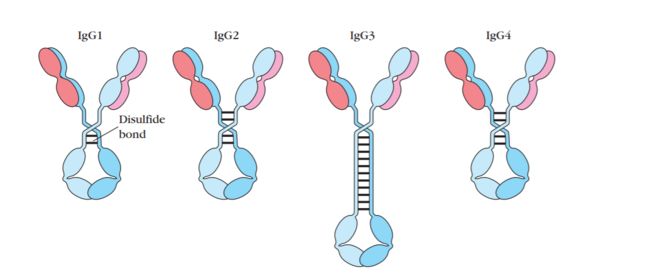
2. 按照结构分类:按照重链的不同,μ、γ、α、δ、ε分别对应IgM, IgG, IgA, IgD和IgE。其本质的区别是重链二硫键数量、铰链区长度以及重链Fc段恒定区长度的区别。
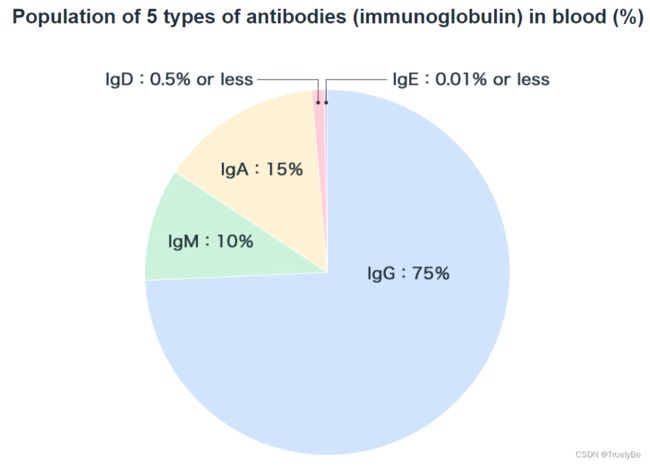
IgG:是血液中主要的抗体类型,具有很强的结合血液中细菌和毒素的能力。也是唯一能够穿透胎盘的抗体亚型,能够从母亲体内转移到新生儿体内并起到保护作用。因此通常所说的抗体/免疫球蛋白都是值得IgG。而IgG又根据重链二硫键数量的不同分为IgG1、IgG2、IgG3、IgG4。
- IgG1、IgG3、IgG4都可以容易穿过胎盘,但是IgG2穿过胎盘的效率较低。
- 补体激活能力IgG3>IgG1>IgG2>IgG4,IgG4完全没有补体激活能力。
- IgG1和IgG3对吞噬细胞上的Fc受体具有很高的亲和力,IgG4亲和力中等,而IgG2具有极低的亲和力。
- IgG1由于结构稳定,是最常使用的亚型,如曲妥珠单抗、贝伐珠单抗;IgG3结构不稳定,较少使用,如omodenbamab。
- IgG2存在二硫键错配(AA、AB、BB),与其它Fc受体结合力较低,如帕尼单抗。
- IgG4不能激活补体,且与其它Fc受体结合力较低,用于减弱Fc功能的抗体,如O/K药。
IgM:是由5格单位组成的5价抗体。是抗原刺激诱导免疫应答中最先产生的Ig,可结合补体,主要分布于血清中。由于IgM有较高的结合价,其杀菌、溶菌、促吞噬和凝集作用比IgG高500-1000倍,IgM在机体得早期防御中起着重要的作用。
IgA:分血清型和分泌型两种。在血液中,IgA主要是由单体形式存在;但是在分泌液中(如肠液、鼻涕和唾液)时,其是由二聚体形式存在。血清型IgA可起到调理吞噬ADCC作用,分泌型IgA是机体粘膜防御系统的主要成分,能抑制微生物再呼吸道上皮附着,减慢病毒繁殖,是粘膜的重要屏障,对某些病毒、细菌和一般抗原具有抗体活性,是防止病原体入侵机体的第一道防线。其也存在于乳汁中从而保护新生儿的消化道不受到细菌或病毒的感染。
IgD:在血清中含量很低,约占总Ig的1%。可作为膜受体存在于B细胞表面,有研究表明IgD可能参与启动B细胞产生抗体和防止呼吸道感染。
IgE:一种分泌型免疫球蛋白,是引起Ⅰ型变态反应的主要抗体,也是免疫球蛋白中对热最不稳定者,在5种免疫球蛋白中,IgE半衰期最短,并且具有最高的分解率和最低的合成率,因此在血清中含量最低。IgE被认为和寄生虫免疫反应以及参与过敏反应。如在摄入过敏原或自身免疫性疾病中,浆细胞产生的IgE抗体指引下,肥大细胞和嗜碱性粒细胞脱颗粒引发过敏反应,释放组胺、白三烯及其他炎症介质。如奥马珠单抗就是首个获批上市针对IgE的抗体来治疗哮喘。
3. 按照抗体产生的方法来分,可以分为多克隆抗体、单克隆抗体和基因工程抗体
- 首先是克隆的定义:是由单一的祖先细胞分裂繁殖而形成的一簇细胞纯系;克隆在这里指的是B细胞克隆,单克隆就是指由单个B细胞克隆产生的抗体,多克隆就是指多个B细胞克隆产生的抗体。
- 多克隆抗体(polyclonal antibody, pAb):用一种包含多种抗原决定簇的抗原免疫动物,可刺激机体多个B细胞克隆产生针对多种抗原表位的不同抗体。所获得的免疫血清实际上是含有多种抗体的混合物。制备:①制备抗原;②选择实验动物;③动物免疫;④试取血进行测试,看看是否成功免疫;⑤如果成功免疫,处死实验动物,采集全部血清;⑥纯化出抗体;⑦鉴定抗体,包括纯度以及特异性。
- 单克隆抗体(monoclonal antibodies, mAb):由一个识别一种抗原表位的B细胞克隆产生的同源抗体。高度均一、特异性强、效价高、少或无交叉反应性。制备(杂交瘤细胞法): 经过特定抗原处理过的B淋巴细胞与骨髓瘤细胞通过细胞融合的方法得到杂交瘤细胞,经HAT培养基筛选、ELISA检测效价后就得到阳性克隆株,最后进行细胞培养或将细胞注入到动物(一般为balb/c小鼠)腹腔中用腹水培养,收集上清/腹水纯化后就能得到单克隆抗体。
- 关于基因工程抗体,后面会单独开一章来讲。
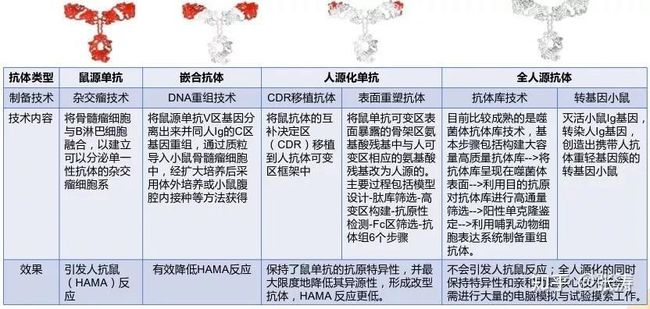
4. 根据人源化程度分类:具体人源化技术过程会在后面讲基因工程抗体的时候来讲,这里先简单谈谈其分类。
| 鼠源单抗 | 人鼠嵌合抗体 | 人源化抗体 | 全人源抗体 |
| 鼠源成分100% | 鼠源成分30-40% | 鼠源成分5-10% | 鼠源成分0% |
| -莫单抗 | -昔单抗 | -珠单抗 | 木单抗 |
| -momab | -ximab | -zumab | -mumab |
值得注意的是,2021年11月,WHO更新了抗体药通用名命名规则,抗体不再通称-mab。取而代之的4类后缀,未修饰的单抗后缀为“-tug”,抗体工程Fc引入突变的单抗后缀为“-bart”,双抗和多抗的后缀为“-mig”,抗体片段的后缀为“-ment”。抗体药的通用名的中缀也有部分变化,过敏抗体的中缀为“-ler-”,免疫刺激性抗体的中缀为“-sto-”,免疫抑制性抗体的中缀为“-pru-”。举例来说:
- 信达生物的PD-1抗体Sintilimab,采用了IgG4亚型,Fc引入S228P突变避免Fab exchange,应采用第二类后缀“-bart”,中缀则使用免疫抑制性的“-pru-”。综上,sintilimab应用新版命名规则应该叫做“sintiprubart”。
- 再以辉瑞/默克的Avelumab为例,采用IgG1亚型,Fc没有引入突变保留了ADCC效应。应采用第一类后缀“-tug”,中缀使用免疫抑制性的“-pru-”。综上,avelumab应用新版命名规则应该叫做“aveprutug”。
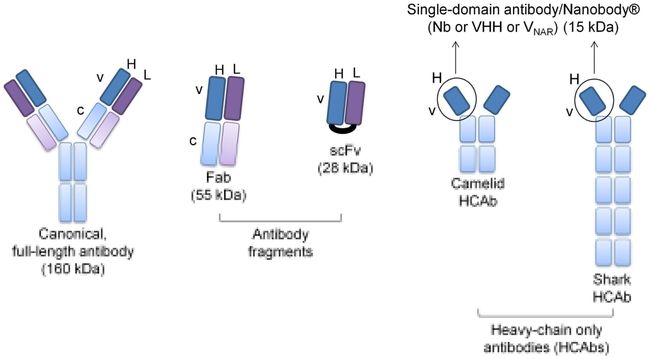
四、抗体片段
1. Fab和 F(ab')2: 相较于完整抗体而言,分子量大幅减小,分子量分别为50 kDa和110 kDa。Fab是能够结合抗原的单价片段,无Fc段,由木瓜蛋白酶酶切生成。可以在更简单的表达系统(如酵母)中表达。F(ab')2可以通过胃蛋白酶酶切得到,是能够结合抗原的二价片段,仍然保留了二硫键和铰链区。相较于完整片段,其能够去除Fc片段和细胞(如巨噬细胞,树突细胞,中性粒细胞,NK细胞以及B细胞)表面的Fc受体的非特异性结合,从而减少CDC、ADCC等杀伤效应,并在体内预防Fc相关的不良反应。另外,由于其具有更小的分子量,其能够在、在体内具有更好的穿透效果。此外,由于没有Fc段,它们不会对抗Fc的抗体的检测产生干扰。在应用上,如在治疗湿性黄斑变性患者方面,VEGF-a特异性Fab片段雷珠单抗比相应的全长单抗贝伐珠更有效,FDA已批准certolizumab-pegol(Cimzia®),一种聚乙二醇化和人源化的抗TNF-α Fab,用于治疗克罗恩病和类风湿性关节炎。NMPA批准了Metuximab-(131碘[131I]美妥昔单抗注射液),一种放射性碘[131I]标记的抗CD147 F(ab')2单抗,用于治疗肝癌。
2. scFv:scFv是一种重组抗体。其包含了有柔性linker(通常是15-20个甘氨酸和丝氨酸组成,能够改善其溶解性)链接的抗体的VL和VH片段,分子量约为25 kDa。scFv通常可由细菌表达系统表达。scFv主要的优势是其较小,且能够在成本更低的细菌中表达,并且可以通过噬菌体展示来筛选得到(有些抗体或片段通过体内免疫的方式可能无法得到,如自身免疫抗原和极具致命性抗原)。当然,由于scFv片段较小,有更好的穿透性,且体内半衰期较短,能很快被清除掉,因此在成像领域具有优势。此外,由于没有Fc片段。scFv的免疫原性较小。而scFv的主要缺点是其亲和力较完整抗体小,稳定性差,较容易聚集沉淀。其较短的半衰期也对长滞留的治疗效果有影响。在临床应用上,2019年FDA首次批准了Brolucizumab用于治疗与年龄相关的湿性黄斑变性(AMD)。
3. 纳米抗体:也叫单域抗体。由重链抗体衍生得到,分子量仅为15 kDa。VHH相比一般的VH,CDR1与CDR3之间多以一对二硫键,同时FR区的若干疏水氨基酸替换成了亲水氨基酸,使之更稳定、水溶性好。目前FDA和EMA批准的第一种VHH药物caplacizumab(Ablynx Inc),是一种用于治疗成人获得性血栓性血小板减少性紫癜的人源化抗VWF的纳米抗体。由于本课题组一直从事纳米抗体的相关研究,后面会单独开一章来谈一谈纳米抗体。
4. Darpin:通过蛋白质工程改造得到的抗体类似蛋白。来源自自然界中最常见的结合蛋白:锚蛋白。其分子量为14(四个重复构象)或者18 kDa(五个重复构象),重复构象少于三个时不稳定。其N端和C端的Cap能够将中心疏水区域包裹起来。可以通过对参与结合的位点氨基酸建库,从而采用核糖体或噬菌体展示筛选来获得能够和目标蛋白结合的Darpin。其能够在原核系统中高效表达,且具有极好的稳定性和溶解性。Darpin也能够很容易通过串联表达来获得多价、多特异性的蛋白。其亲和力能够达到pmol级。临床上,MP0112,一种针对湿性年龄相关性黄斑变性的VEGF抑制剂临床未通过FDA审批。
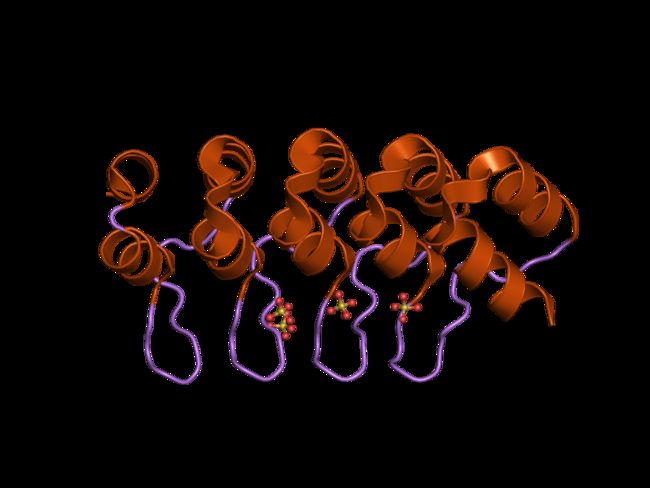
5. 亲和体affibody:通过蛋白质工程得到,能够进行原核表达。仅有58个氨基酸构成,分子量仅为6 kDa。最初affibody是基于protein A的Z domain的骨架设计的。通过序列替换和噬菌体展示筛选,可以获得能够和目标蛋白较高亲和力的蛋白。affibody由3个α螺旋构成,且分子内没有二硫键存在,能够极为快速的完成折叠(已知最快),且能和多种蛋白串联融合表达。affibody一般极为稳定,能够在高温(90°C) 、强酸(pH 2.5)、强碱(pH 11)下变性之后再在室温中恢复折叠。二代affibody,ABY-025,能够以pmol的亲和力结合HER2受体。因此,基于affibody的检测、成像技术大有潜力。
四、不同Format形式的抗体
1. 二/多价抗体:多价抗体在小抗体片段中较为常见,通常用来弥补单价抗体亲和力不足的缺点。如Ablynx的caplacizumab就是采用了二价纳米抗体。二价抗体也分为针对同一抗原表位和针对不同抗原表位的双表位(biparatopic)抗体。
2.二/多特异性抗体:目前较为火热,是将能够结合不同抗原的抗体融合在一起组成。目前在BiTE、CART领域十分常见。下图对双特异性抗体有一个较好的总结。目前全球已获批双特异性抗体共有5款,分别为Trion的Catumaxomab(Epcam×CD3,2017年退市)、Amgen的blinatumomab(CD3×CD19,2014年全球首次获批上市)、Roche的emicizumab(艾美赛珠单抗,FIX×FX,2017年全球首次获批)和faricimab(ANGPT2×VEGFA,2022年全球首次获批)、强生的amivantamab(EGFR×cMet,2021年全球首次获批),其中blinatumomab、emicizumab已分别于2020.12、2018.11在国内获批上市。关于双特异性抗体,后面也会单独开一章来讲一下。