初中化学知识点总结 基本概念和基本理论
(一)物质的变化和性质
1.物质的变化:物理变化:没有生成其他物质的变化。化学变化:生成了其他物质的变化。
化学变化和物理变化常常同时发生。物质发生化学变化时一定伴随物理变化;而发生物理变化,不一定同时发生化学变化。物质的三态变化(固、液、气)是物理变化。物质发生物理变化时只是分子间的间隔发生变化,而分子本身没有发生变化;发生化学变化时,分子被破坏,分子本身发生变化。化学变化的特征:生成了其他物质的变化。
2.物质的性质(描述性质的语句中常有“能……”“可以……”等字)
物理性质:颜色、状态、气味、熔点、沸点、硬度、密度、溶解性。
化学性质:通过化学变化表现出的性质。如还原性、氧化性、酸性、碱性、可燃性、热稳定性。
元素的化学性质跟原子的最外层电子数关系最密切。原子的最外层电子数决定元素的化学性质。
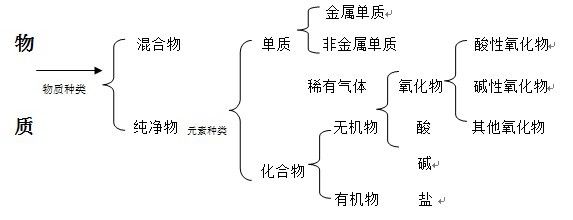
(二)物质的分类
3.混合物:是由两种或两种以上的物质混合而成(或由不同种物质组成) 例如,空气,溶液(盐酸、
澄清的石灰水、碘酒、矿泉水), 矿物(煤、石 油、天然气、铁矿石、石灰石),合金(生铁、钢)
注意:氧气和臭氧混合而成的物质是混合物,红磷和白磷混合也是混合物。
纯净物、混合物与组成元素的种类无关。即一种元素组成的物质可能是纯净物也可能是混合物,多种元素组成的物质可能是纯净或混合物。
4.纯净物:由一种物质组成的。 例如:水、 水银、 蓝矾(CuSO4 ·5H2 O)都是纯净物
冰与水混合是纯净物。名称中有“某化某”“某酸某”的都是纯净物,是化合物。
5.单质:由同种(或一种)元素组成的纯净物。例如:铁 氧气(液氧)、氢气、水银。
6.化合物:由不同种(两种或两种以上)元素组成的纯净物。
名称中有“某化某”“某酸某”的是化合物。
7.有机物(有机化合物):含碳元素的化合物(除CO、CO2 和含碳酸根化合物外)
无机物:不含碳元素的化合物以及CO、CO2 和含碳酸根的化合物
8.氧化物:由两种元素组成,其中一种是氧元素的化合物。
a.酸性氧化物:跟碱反应生成盐和水的氧化物。CO2 ,SO2 ,SO3 大部分非金属氧化物都是酸性氧化物,跟水反应生成同价的含氧酸。
CO2 + H2O= H2CO3 SO2 + H2O= H2SO3 SO3 + H2O= H2SO4
b.碱性氧化物:跟酸反应生成盐和水的氧化物。CaO Na2 O MgO Fe2 O3 CuO
大部分金属氧化物都是碱性氧化物, BaO K2 O CaO Na2 O溶于水立即跟水反应
生成相应的碱,其他碱性氧化物不溶于水,跟水不反应。
CaO+H2O=Ca(OH)2 BaO+H2O=Ca(OH)2 Na2O+H2O=2NaOH K2O+H2O=2KOH
c.注意:CO和H2 O既不是酸性氧化物也不是碱性氧化物,是不成盐氧化物。
9.酸:电离时生成的阳离子全部是氢离子的化合物。酸溶液的PH值小于7
酸的名称中最后一个字是“酸”,通常化学式的第一种元素是“H ”,酸由氢和酸根离子组成
紫色石蕊试液遇酸变红色,无色酚酞试液遇酸不变色
根据酸的组成,通常有以下两种分类方法:酸的电离方程式:酸=nH+ +酸根离子n-
a.根据酸分子电离所能生成的氢离子的个数分为:一元酸(HCl、HNO3 )、
二元酸(H2 SO4 、H2 S、H2 CO3 )和三元酸(H3 PO4 )
b.根据酸分子里有无氧原子分为:
含氧酸(H2 SO4 ,HNO3 , H3 PO4 名称为:某酸)
无氧酸(HCl, H2 S名称为:氢某酸 )
鉴定酸(鉴定H+ )的方法有:①加紫色石蕊试液变红色的是酸溶液;
②加活泼金属Mg、Fe、Zn等有氢气放出
10.碱:电离时生成的阴离子全部是氢氧根离子的化合物。碱通常由金属离子和氢氧根离子构成
溶碱有五种:钾钙钠钡氨(KOH,Ca(OH)2 ,NaOH Ba(OH)2 ,氨水)它们的溶液无色。
有颜色的碱(不溶于水):红褐色的氢氧化铁(Fe(OH)3 ↓)、蓝色的氢氧化铜(Cu(OH)2 ↓)
其他固体碱是白色。碱的名称通常有“氢氧化某”,化学式的最后面是“OH”
可溶性碱的溶液PH值大于7,紫色石蕊试液遇溶碱变蓝色,无色酚酞试液遇溶碱变红色
鉴定可溶性碱溶液(鉴定OH- )方法一:加紫色石蕊试液变蓝色,加无色酚酞试液变红色是碱.
方法二:加铁盐溶液有红褐色沉淀生成;加铜盐溶液有蓝色沉淀的是碱。
11.盐:电离时生成金属离子和酸根离子的化合物。
第一种分类方法:
a.正盐(酸碱完全中和的产物,没有可电离的氢离子或氢氧根离子),例如NaCl、Na2 S KNO3
无氧酸正盐叫 “某化某”Na2 S_______ MgCl2__________FeS__________
含氧酸盐叫“某酸某”KNO3_________ BaSO4______________Na2CO3______
b.酸式盐(多元酸里的氢部分被金属取代,H夹在中间)
NaHCO3____________ 、Ca(HCO3 )2_____________、NaH2 PO4 _____________
常见的酸式盐的酸根有:HCO3 - 、HSO4 - 、H2 PO4 - 、HPO4 2-
c.碱式盐(化学式的中间有“OH”):Cu2 (OH)2 CO3
第二种分类方法
按盐中相同部分的离子称为某类盐:含碳酸根离子的盐称为碳酸盐、含硫酸根离子的盐称为硫酸盐、含硝酸根离子的盐称为硝酸盐、含铁离子的盐称为铁盐,等等。
12.酸碱指示剂(石蕊试液、无色酚酞)和PH值:
酸溶液的PH值小于7(如盐酸、稀硫酸、硝酸),酸性越强PH值越小,酸性越弱PH值越大。水、中性的硫酸盐、硝酸盐和盐酸盐溶液不能使指示剂变色,PH值等于7。不能使指示剂变色;可溶的碱溶液PH值大于7。碱性越强PH值越大,碱性越弱PH越小
13.酸碱盐溶解性口诀:
钾钠硝铵溶 溶碱有五种 钡钾钙钠氨
不溶氯化物AgCl 不溶硫酸盐BaSO4 碳酸盐只溶钾钠铵
口诀的含义:含有钾、钠、硝酸根、铵根的物质都溶于水
溶于水的碱有:氢氧化钡、氢氧化钾、氢氧化钙、氢氧化钠和氨水,其他碱不溶于水
含Cl的化合物只有AgCl不溶于水,其他都溶于水;
含SO42-的化合物只有BaSO4 不溶于水,其他都溶于水
含CO32-的物质只有含K+ Na+ NH4+溶于水,其他都不溶于水
14.沉淀物中AgCl和BaSO4 不溶于稀硝酸,Fe(OH)3是红褐色沉淀,Cu(OH)2是蓝色沉淀
其他沉淀是白色(包括Fe(OH)2)有以下常见的沉淀:Mg(OH)2 Al(OH)3 CaCO3 BaCO3 Ag2 CO3
推断题中,往沉淀物加稀硝酸:若讲沉淀不溶解,则沉淀中一定有AgCl或BaSO4 ;若讲沉淀 全部溶解,则沉淀中一定没有AgCl或BaSO4 ;若讲沉淀部分溶解,则沉淀中一定有AgCl或BaSO4 中的一种,且还有另一种可溶于稀硝酸的沉淀。
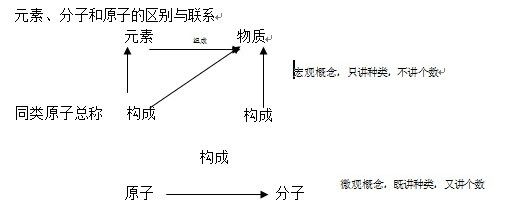
(三)分子、原子、离子、元素和化学式
15.元素:具有相同核电荷数(即核内质子数)的一类原子总称元素。
原子的核电荷数(即核内质子数)决定原子或离子的元素种类。
①大部分单个的元素符号表示:一种元素、该元素的一个原子、一种单质
但H N O Cl等符号不能表示单质,它们的单质是:H2 N2 O2 Cl2
②地壳中元素按质量分数由多至少前四位是:O氧 Si硅 Al铝 Fe铁。铝是地壳中含量最多的金属元素。
③化学的“语法”: “某分子”由“某原子构成”
“某物质”由“某元素组成”或“某某分子构成”(金属单质、稀有气体讲由某原子直接构成)
例:水由氢元素和氧元素组成,水由水分子构成。 1个水分子由2个氢原子和1个氧原子构成
元素、物质都是宏观概念,只表示种类,不表示个数。不能说“水是由二个氢元素和一个氧元素组成”
④具有相同核电荷数的粒子不一定是同种元素,下列粒子有相同的核电荷数:
⑴H2 和He ⑵CO、N2 和Si ⑶O2 、S和 S2- ⑷ OH- 和 F-
16.粒子:如原子、离子、分子、电子、质子等,它们都是微观概念,既表示种类又可表示个数。
分子、原子、离子都是构成物质的粒子。金属单质和稀有气体由原子直接构成;
非金属单质、非金属与非金属形成的共价化合物由分子构成,化合物中既有金属元素又有
非金属元素的离子化合物是由离子构成。
17.分子:分子是保持物质化学性质的最小粒子。分子由原子构成,
例:1个水分子由2个氢原子和1个氧原子构成
18.原子:原子是化学变化中的最小粒子。(注意:原子不是构成物质的最小粒子。)
原子的的构成:原子由核外带负电的电子和带正电的原子核构成,原子核由带正电的质子
和不带电的中子构成。 在不显电性的粒子里: 核电荷数=质子数=核外电子数
注意:原子不是构成物质的最小粒子。原子只是化学变化中的最小粒子;
普通氢原子核中只有质子无中子,氢原子的原子核就是一个质子。
分子和原子的区别:在化学变化中分子可分为更小的粒子---原子,原子不能再分。
物质发生物理变化时只是分子间的间隔发生变化,而分子本身没有发生变化;发生化学变化时,
分子被破坏,分子本身发生变化。
在一切化学反应中,反应前后元素的种类、原子的种类、原子的数目和原子的质量都不变。
19.原子团:由两种或两种以上元素的原子构成,在化学反应中通常以整体参加反应的原子集团
常见的原子团:SO42- CO32- NO3- OH- MnO4- MnO42- ClO3- PO43- HCO3- NH4+
碳酸氢根(HCO3-)硫酸氢根(HSO4-)磷酸氢根(HPO42-)磷酸二氢根(H2PO4-)
注意:原子团只是化合物中的一部分,不能脱离物质单独存在,因此含原子团的物质必定有
三种或三种以上元素,二种元素组成的物质不含原子团。原子团在化学反应中可再分为更小的粒子原子。
20.离子:带电的原子或原子团叫离子。带正电的离子叫阳离子;带负电的离子叫阴离子。
离子里:质子数=核电荷数=电子数±带电量
离子符号的写法:离子的电荷数标在右上角,电荷的数值等于它对应的化合价
阳离子:Na+ Mg2+ Al3+ 、H+ NH4+、Fe2+ Fe3+ Ca2+
阴离子:O2- 、OH- S2-、F- Cl- SO4 2- CO32- NO3- MnO4- PO43- MnO42- ClO3-
21.核外电子排布的规律:核外电子按能量由低到高从里往外排,第一层最多容纳2个电子,
第二、三层最多容纳8个电子。 按顺序背诵:质子数从1~18的元素符号和名称:
氢氦锂铍硼 碳氮氧氟氖 钠镁铝硅磷 硫氯氩
22.稳定结构:最外层电子数是8(只有一层的为2)的结构。
元素的化学性质跟原子的最外层电子数关系最密切,原子的最外层电子数决定元素的化学性质:
最外层电子数小于4时,易失去最外层所有电子,成为阳离子;(通常是金属元素)
最外层电子数多于4时,易得到电子使最外层电子数变为8,成为阴离子(通常是非金属元素)
最外层电子数与化合价的关系:(元素的最高正价等于原子的最外层电子数)
最外层电子数小于4时,最外层电子数就是元素的化合价(正价);
最外层电子数多于4时,最外层电子数-8=元素的化合价
23.化学式的写法:
① 单质的化学式:大部分单质的化学式只用单个的元素符号,
下面几种元素的单质不能只用单个的元素符号表示,须注意:
氢气H2 氧气O2 氮气N2 氯气Cl2 氟气F2 溴(Br2 ) 碘(I2 )臭氧O3
②化合物的化学式写法与读法的一般关系:“倒写倒读”。
化合价与化学式(交叉法确定化学式:正价在前负价在后,约简化合价,交叉)
NH3、有机物如CH4等化学式是负价在前正价在后。同种元素可以有不同的化合价
硝酸铵(NH4 NO3 )中氮元素的化合价分别为前N-3价 ,后N+5价。
24.元素的化合价:一种元素一定数目的原子与另一种元素一定数目的原子化合的性质。
标在元素符号的正上方
+2 -2 +1
Ca +2价的钙元素 O -2价的氧元素 H2O 水中氢元素化合价是+1价
背诵化合价口诀:
+1价钾钠银铵氢, +2价钡钙镁铜汞锌
二三铁、二四碳, 三铝四硅五价磷,
氟、氯、溴、碘-1价 氧硫-2要记清。
氢氧根、硝酸根(OH、NO3 )-1价, 硫酸根、碳酸根(SO4 、CO3 )-2价,
化合物各元素化合价代数和为零, 单质元素化合价是零。
注:铵是NH4原子团;+2价的铁叫“亚铁”; +1价的铜叫“亚铜”
无氧时S为-2价,跟氧结合时+4或+6价。SO32-原子团叫“亚硫酸根”
无氧时Cl为-1价,跟氧结合时+1、+3、+5或+7价
25.相对原子质量:以一种碳原子(碳-12)质量的1/12作为标准,其他原子的
质量跟它相比较所得的数值,是该种原子的相对原子质量。
26. 化学反应基本类型
①化合反应:A+B+...=C 两种或两种以上的物质生成另一种物质的反应
②分解反应:A=B+C+... 一种物质生成两种或两种以上其他物质的反应
③置换反应:一种单质跟一种化合物反应生成另一种单质和另一种化合物的反应
A+BC=AC+B 溶液里的置换反应必须符合金属活动性顺序:
金属活动性顺序由强至弱:Ba K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
(按顺序背诵) 钡 钾钙钠镁铝 锌铁锡铅(氢) 铜汞银铂金
金属位置越靠前的活动性越强,越易失去电子变为离子,反应速率越快
排在氢前面的金属能置换酸里的氢,排在氢后的金属不能置换酸里的氢,跟酸不反应;
排在前面的金属,能把排在后面的金属从它们的盐溶液里置换出来。排在后面的金属跟
排在前面的金属的盐溶液不反应。 注意:单质铁在置换反应中总是变为+2价的亚铁
等质量金属跟足量酸反应,放出氢气由多至少的顺序按相对原子质量/化合价由小到大排列:
Al(9) Mg(12) Ca(20) Na(23) Fe(28)Zn(32.5) K(39)
④复分解反应:两种化合物相互交换成分,生成另外两种化合物的反应,
复分解反应前后各元素和原子团的化合价都保持不变。
注意事项:复分解反应能否发生,要考虑是否有沉淀、气体或水生成。有沉淀生成的反应中,反应物和生成物中不能同时有难溶于水的物质。初中化学只有碳酸盐跟酸反应有气体生成
中和反应:酸跟碱作用生成盐和水的反应。中和反应属于复分解反应。
27.我国古代在化学方面的杰出贡献主要有:造纸术、火药、烧瓷器
28.氧化反应:物质跟氧发生的化学反应(或得到氧的化学反应),不是一种基本反应类型。
缓慢氧化:缓慢进行不易被人觉察的氧化反应。如铁生锈、呼吸作用、食物腐败
燃烧必备的二条件:①可燃物与氧气接触,②温度达到着火点
自燃:由缓慢氧化积聚的热量引发的自发燃烧。白磷着火点低,易自燃,要放在水中密封保存。
还原反应:物质失去氧的反应。(氧化反应和还原反应不是基本反应类型)
还原剂:在化学反应中得到氧的物质。常用的还原剂有H2 、CO、C等, 具有还原性。
29.催化剂(触媒): 在化学反应里能改变其他物质的化学反应速率,而本身的质量和化
学性质在化学反应前后都没有改变的物质。
催化作用:催化剂在化学反应里所起的作用叫催化作用。
注意:二氧化锰只是在氯酸钾分解的反应里作催化剂,在其他反应里可能不是催化剂
30. 书写化学方程式①依据:质量守恒定律:参加化学反应的各物质质量总和,等于反应后生成的各物质质量总和。(在一切化学反应中,反应前后元素的种类、原子的种类、各类原子的数目和原子的质量都不变)②书写化学方程式的步骤: 化学式写正确,方程式要配平,条件箭头要标明。
③遵守二原则:一是以客观事实为基础,不能随便臆造化学反应和化学式;
二是遵守质量守恒定律,等号两边的各种原子数目必须相等
(四)溶液、溶解度
31.溶液:一种或几种物质分散到另一种物质里,形成均一、稳定的混合物。
溶液由溶质和溶剂组成。(在溶液里的反应,一般是溶质参加反应)
32.溶质:被溶解的物质叫溶质(可以是气体、液体或固体),但没有溶解的物质
不是溶液的一部分,不能认为是溶质。
例:20℃时,50克食盐放入100水中,没有溶解的24克食盐不是溶质,不是溶液的一部分
33.溶剂:能溶解其他物质的物质叫溶剂。溶剂通常是液体,不指明溶剂的溶液其溶剂是水。
34.饱和溶液:在一定的温度下,一定量的溶剂里,不能再溶解某种溶质溶液叫做
这种溶质的饱和溶液。(蒸发溶剂有晶体析出,剩余溶液一定是饱和溶液)
35.不饱和溶液:在一定温度下,一定量的溶剂里,还能继续溶解某种溶质的溶液叫做
这种溶质的不饱和溶液。注意:饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液
同种溶质在同一温度下,饱和溶液比不饱和溶液的浓度大
36.饱和溶液与不饱和溶液的相互转化
一般情况下:向饱和溶液加溶剂或升高溶液温度可使饱和溶液变为不饱和溶液;
向不饱和溶液加溶质、降低溶液温度、蒸发溶剂可使不饱和溶液变为饱和溶。
37.固体的溶解度:在一定温度下,某固态物质在100克溶剂达到饱和状态时所溶解
的质量,叫做这种物质在这种溶剂里的溶解度。
(关键词:一定的温度 100克溶剂 达到饱和状态 溶质质量)
38.溶解度曲线:物质的溶解度随温度变化的曲线。
大部分固体的溶解度随温度升高 而增大,但NaCl的溶解度受温度影响很小,
熟石灰的溶解度随温度高而减小。气体的溶解度随温度降低、压强的增大而增大。
39.固体溶解度与溶解性的关系:
| 溶解性 |
易溶 |
可溶 |
微溶 |
难溶(或不溶) |
| 20℃的溶解度(克) |
>10 |
1~10 |
0.01~1 |
<0.01 |
常见难溶于水的物质有:大部分金属、金属氧化物、BaSO4、AgCl、CaCO3等碳酸盐
40.混合物的分离:把混合物里的各种物质分开,得到混合物中每一组分的纯净物。
常用的物理方法有:溶解、过滤、结晶等
化学方法是:通过化学反应,使某些组分变为与原物质不同状态的物质而分开
41.结晶:从溶液里得到有一定几何形状的晶体的过程叫结晶。
结晶方法:①蒸发溶剂结晶(适用于溶解度受温度影响小的固体,如NaCl)
从盐水中得NaCl固体可采用蒸发溶剂的方法。
②冷却热的饱和溶液结晶(适用于溶解度受温度影响大的固体,如硝酸钾)
此方法还可分离硝酸钾和氯化钠的混合物,得较纯的硝酸钾晶体。
(五)电离
42.溶液的导电性:物质溶于水发生电离使溶液能导电。(纯水、固体酸碱盐不导电)
43.电离:物质溶于水时,离解成可自由移动的离子的过程叫电离。
注意 ①电离是自发的过程,不须通电。②在溶液里所有阳离子所带的正电荷总数 和所有阴离子所带的负电荷总数相等,所以溶液不显电性。但阳离子的个数不一定等于阴离子的个数
44.电离方程式的书写注意:①离子电荷数等于它对应的化合价数值②原子团不能拆散
Ax By =xAy+ +yBx- Ax(ROn )y =xAy+ +yROn x-