肠道重要基石菌属——罗氏菌属(Roseburia)
谷禾健康
罗氏菌属是共生细菌的一部分,在世界各地的人群中都有代表,占健康肠道细菌总数的 2-31%(谷禾数据库)。产生短链脂肪酸,特别是丁酸,影响结肠运动,具抗炎特性。
罗氏菌属 の 基本特性
罗氏菌属(Roseburia),专性革兰氏阳性厌氧菌, 轻微弯曲,杆状,并通过多个亚末端鞭毛运动。
罗氏菌属包括5种:
- Roseburia intestinalis、 R.hominis、 R.inulinivorans、 R.faecis、 R.cecicola
罗氏菌属代谢膳食成分,刺激其增殖和代谢活动。
罗氏菌属可以分泌各种分子,与宿主和消化道的其他细菌相互作用。
罗氏菌属可以改善肠道生物多样性,提高葡萄糖耐受性,帮助减肥,使结肠细胞恢复活力。
罗氏菌属的失调(过少)可能影响多种代谢途径,并与多种疾病相关(包括肠易激综合征、肥胖、2型糖尿病、神经系统疾病、过敏、肝病等)。
Roseburia也可以作为症状性病理(如胆石形成)的生物标志物,或作为益生菌修复有益菌群。
罗氏菌属 の 定植
研究人员利用16S rRNA测序技术研究早产儿肠道菌群的多样性,并对早期肠道定植模式进行了监测。在新生儿中没有发现Roseburia,但在母乳中发现了,可能通过食用母乳获得。
Roseburia在老年人中降低,提示衰老可能导致肠道菌群的改变。 相反,与较年轻的老年人相比,百岁老人的肠道菌群中有更丰富的Roseburia。
罗氏菌属 ——丁酸生产者
罗氏菌产生短链脂肪酸(乙酸,丙酸,丁酸),分解不可消化的碳水化合物。短链脂肪酸在碳水化合物和脂肪等重要营养素的代谢中发挥重要作用。
典型的Roseburia菌株特别喜欢生产高水平的丁酸盐。这些化合物通常参与能量产生,可以保护肠道免受病原体和疾病的侵害。
目前,发现只有Roseburia inulinivorans产生丙酸,但不是从葡萄糖中产生的。在Roseburia中,乙酸辅酶a转移酶是进行丁酸合成最后一步的主要酶。丁酸盐的形成可通过底物水平的磷酸化和质子梯度导致肠上皮能量产生和细胞反应调节。丁酸是罗氏菌属与寄主相互作用的关键因子。
罗氏菌属是一种抗炎因子
前面小节我们知道,Roseburia从可发酵的膳食碳水化合物中产生了大量的丁酸盐。R. intestinalis主要寄生在粘蛋白层,并确保丁酸盐的生成。Roseburia作为一种高产丁酸菌,可能对控制炎症过程,尤其是肠道炎症过程具有重要作用。
从R. intestinalis菌体大量培养获得的鞭毛蛋白制剂,刺激人肠上皮细胞系分泌IL-8,提示鞭毛蛋白具有促炎作用。
矛盾的是,Roseburia还与肠道中抗炎调节T细胞的产生有关:持续的减少可能会对宿主修复上皮细胞和调节炎症的能力产生功能性影响。
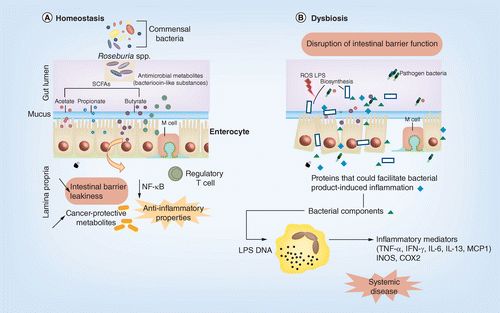
罗氏菌属在维持肠道内稳态和生态失调中的作用如下图所示。此外,焦磷酸测序实验揭示了丁酸产生物的存在,如Roseburia,对免疫系统的成熟是很重要的。
Zohreh et al., Future Microbiol 2017
罗氏菌属 の 失调与疾病
肠道疾病
Roseburia和肠道健康之间的联系,包括炎症性肠病,肠易激综合征和结直肠癌。
炎症性肠病(IBD)
溃疡性结肠炎中主要产丁酸菌(如Roseburia intestinalis)的减少与短链脂肪酸浓度的降低相关。
有研究认为,溃疡性结肠炎患者中,丁酸盐产生的减少可能与丁酸盐氧化相关基因的表达减少和/或与丁酸盐产生菌(罗氏菌属)的减少有关。
在回肠克罗恩病患者中,Roseburia的消失是肠道菌群的一种特殊变化。
在溃疡性结肠炎中,发现患者罗氏菌属丰度较低(P<0.0001),尤其是Roseburia hominis减少。
肠易激综合征(IBS)
在慢性便秘患者中,健康人与慢性便秘患者结肠黏膜和粪便微生物群的比较表明,Roseburia的存在与结肠运输更快相关。
假设肠易激综合征患者的肠道菌群中可能存在一种功能失调,导致碳水化合物代谢的改变,这是允许向宿主提供营养和能量的一个中心过程。
Roseburia相关细菌的丰度通常与IBS症状呈负相关。肠易激综合征有几种不同的亚型,包括以腹泻为主的和以便秘为主。
健康和腹泻为主的IBS儿童中Roseburia的丰度相似。
便秘患者中Roseburia丰度明显低于健康受试者,这减少了丁酸的产生。然而,这些结果在IBS缓解或利福昔明治疗后未观察到。
结直肠癌
结直肠癌的发生与可能与Roseburia失调有关。在这些患者中已经发现Faecalibacterium和罗氏菌属的减少。
来自中国结直肠癌患者的8对肿瘤/正常组织对,与正常部位相比,肿瘤部位的罗氏菌属显著增加。作者认为,肿瘤组织中这种“旅客细菌”的增加可能与样本类型有关(遗传和饮食的差异),因为他们在另一项研究中未能找到类似的结果。
前面我们了解罗氏菌属在肠道丁酸生成中的作用,值得注意的是肠道细菌丁酸生成的增加与结肠癌发病率的降低有关。丁酸盐通过降低c-Myc来抑制miR-92a转录,从而增加p57水平。
代谢类疾病
代谢综合征与心血管疾病和2型糖尿病等多种疾病风险增加有关。总体而言在代谢类疾病中,罗氏菌属丰度较低。
肥胖
对人类的研究表明,与瘦人相比,肥胖人群的双歧杆菌、罗氏菌属数量减少,肥胖微生物群从饮食中获取能量的效率更高。
这种益生元效应伴随着小鼠循环炎症标志物的降低和白色脂肪组织中紧密连接标记物和瘤胃酸的增加。在接受瘦供体粪便移植的一组中也发现了有益的代谢效应,伴随这种效应的是肠道微生物多样性的显著增加,以及丁酸盐产生菌(如Roseburia)水平的显著增加。
II型糖尿病
研究表明,II型糖尿病患者与健康人相比,肠道微生物组成有一些显著差异,肠道罗氏菌属与血糖呈负相关。
有人提出,Roseburia, Bifidobacterium和Akkermansia菌可以调节葡萄糖稳态,并可能从正常血糖发展为糖尿病前期和糖尿病。
维生素D缺乏可能会增加患糖尿病和肠道菌群失调的风险。一项针对糖尿病高风险人群的研究发现,补充维生素D后,Roseburia的相对丰度显著下降,而维生素D水平升高。这一结果提示,肠道通透性调节可能是与维生素D状态和菌群组成有关的致病机制。
动脉粥样硬化
动脉粥样硬化也是代谢综合征或疾病的常见并发症。它与动脉壁内的脂质积聚和炎症过程有关,与健康患者相比,症状性动脉粥样硬化患者的罗氏菌属和Eubacterium减少。
高血压
比较 60 名原发性高血压患者和 60 名性别、年龄和体重匹配的健康对照的粪便样本,在高血压患者中,罗氏菌属丰度较低。
多囊性卵巢综合征
对163名多囊性卵巢综合征患者分析发现,肠道中罗氏菌属丰度较低。
神经系统疾病
罗氏菌属在保护神经系统免受侵袭方面的作用也得到了重视。
帕金森病
在属水平上,rRNA扩增子测序显示,帕金森病患者比对照粪便中推定的“抗炎丁酸盐”细菌(如罗氏菌属)明显更少。
肌痛性脑脊髓炎/慢性疲劳综合征
这种肠道功能障碍也在肌痛性脑脊髓炎/慢性疲劳综合征中进行了评估,与挪威对照人群相比,患者中罗氏菌属的比例较低。然而,并没有在比利时人群中发现同样的结果。
免疫性疾病
许多研究表明,微生物失调与适应性免疫系统或炎症过程的紊乱有关,导致系统性炎症和自身免疫性疾病。
慢性风湿病
多项研究表明,慢性风湿病患者的肠道中罗氏菌属丰度降低。
幼年特发性关节炎
分析40 名幼年特发性关节炎患者和42名健康对照者的粪便微生物群,年龄 1 至 16 岁。患者Roseburia 的相对丰度显着降低。
此外,一些报告也探讨了肠道微生物群变化和过敏之间的关系,如婴儿和儿童时期的食物过敏。
哮喘
在3周龄时,罗氏菌属的粪便定植可能是日后哮喘发生的早期指标。
食物过敏
事实上,与健康儿童相比,食物过敏儿童的总菌群多样性较低,但罗氏菌属显著增加。
在广泛水解的配方中添加乳糖可以正向调节肠道菌群的组成,减少拟杆菌和梭状芽胞杆菌(包括罗氏菌属)的种类。
过敏性鼻炎
与健康对照相比,过敏性鼻炎患者罗氏菌属增加。
过敏性紫癜
过敏性紫癜患儿罗氏菌属显著减少(P < 0.0001)。
白塞氏综合征
比较22名白塞氏综合征患者和16名健康共居对照者的粪便微生物群,发现白塞氏患者的罗氏菌属显著减少。
肝胆类疾病
胆结石
胆结石患者的粪便胆汁酸总体浓度较高,同时微生物多样性降低,有益的罗氏菌属减少,其LOD较低,可作为症状性胆结石形成的生物标志物。
肝硬化及肝性脑病
肝硬化及其并发症的发病机制,特别是细菌易位、感染和肝性脑病(HE),也可能与肠道菌群的变化密切相关。
研究人员发现肝硬化合并和不合并HE患者的粪便微生物组与健康人群相比没有差异。然而,作者注意到粘膜微生物群中罗氏菌属的丰度较低。作者还报道了与有HE的肝硬化患者相比,没有HE的肝硬化患者有大量的Roseburia。
此外,在使用利福昔明治疗后,这些菌显著减少。作者认为,肝硬化患者(有和没有HE)的微生物群(粪便或结肠粘膜)的改变主要与周围炎症和脑病的改变有关。与HE患者相比,受影响较少的患者(对照组和非HE肝硬化患者)的Roseburia水平更高。
非酒精性脂肪肝
非酒精性脂肪性肝病、非酒精性脂肪性肝炎和肝硬化常使代谢综合征复杂化,并伴有较高的肠道通透性,允许促炎/抗原/有毒物质从肠腔转移到肝脏。肠道失调可能在非酒精性脂肪肝的发展中起重要作用。
罗氏菌属丰度与高脂肪诱导的体重增加、脂肪质量发育和肝脂沉积呈负相关。
酒精性脂肪肝
分析了来自212名韩国双胞胎的410份粪便样本的肠道微生物群。当给酒精性脂肪肝小鼠模型使用罗氏菌属时,不论细菌活力如何,肝脏脂肪变性和炎症均显著改善。
具体而言,肠毛杆菌鞭毛蛋白可能通过toll样受体5 (TLR5)的识别,通过上调紧密连接蛋白Occludin的表达,恢复肠道屏障的完整性,并通过上调IL-22和REG3γ的表达,帮助肠道菌群的恢复。
该研究表明,罗氏菌属改善肠道生态系统,防止肠道渗漏,从而改善酒精性脂肪肝。
以上大部分情况下,罗氏菌属发挥有益菌的作用,罗氏菌属的缺乏会导致疾病风险的增加,然而,不同的罗氏菌种可能具有不同的效果,偶尔也会在疾病中表现更高水平的罗氏菌属。
如何调节罗氏菌属?
许多因素都可能影响消化道中Roseburia的数量,包括饮食成分(如碳水化合物、盐、脂类)和抗菌剂或外源性物质(如金属、农药)的摄入。
饮 食
地中海饮食与肠道中Roseburia的增加有关。某些膳食中的碳水化合物可能会直接促进罗氏菌属的生长。一连串微生物酶,如水解酶、酯酶和裂解酶完全或部分地降解复杂的聚合物。
地中海饮食主要包括植物性食物(例如水果和蔬菜)、全谷物、豆类和坚果等。
肠道中的 pH 值也会影响肠道微生物群的组成。发酵膳食碳水化合物后在肠道中产生的酸性环境可能是有益的,因为酸性可以抑制有害微生物的生长。肠道环境更酸(~pH 5.5)时,丁酸盐水平也更高,这与微生物群的组成有关。肠道中更多的罗氏菌会诱导更多的碳水化合物发酵,从而降低 pH 值并促进丁酸盐的产生。
益生元
益生元是一种不可消化的化合物,是肠道细菌作为益生菌水解和发酵的潜在底物。它们可以调节肠道菌群的组成和/或功能活性,从而对宿主产生有益的生理作用。
许多已被确定为能够提高罗氏菌属:
- β-葡聚糖(蘑菇、燕麦)
- 几丁质
- 青香蕉粉
- 菊粉
- 膳食多酚
主要参考文献:
Zhu L, Xu F, Wan W, et al. Gut microbial characteristics of adult patients with allergy rhinitis [published correction appears in Microb Cell Fact. 2020 Oct 8;19(1):192]. Microb Cell Fact. 2020;19(1):171. Published 2020 Sep 1. doi:10.1186/s12934-020-01430-0
Salem F, Kindt N, Marchesi JR, et al. Gut microbiome in chronic rheumatic and inflammatory bowel diseases: Similarities and differences. United European Gastroenterol J. 2019;7(8):1008-1032. doi:10.1177/2050640619867555
Tamanai-Shacoori Z, Smida I, Bousarghin L, Loreal O, Meuric V, Fong SB, Bonnaure-Mallet M, Jolivet-Gougeon A. Roseburia spp.: a marker of health? Future Microbiol. 2017 Feb;12:157-170.
Carmen Haro, Miguel Montes-Borrego, Oriol A. Rangel-Zúñiga, Juan F. Alcalá-Díaz, et al. (2016). Two Healthy Diets Modulate Gut Microbial Community Improving Insulin Sensitivity in a Human Obese Population,The Journal of Clinical Endocrinology & Metabolism, 101( 1), 233–242.
Khemayanto H, Shi B.(2014).Role of Mediterranean diet in prevention and management of Type 2 diabetes. Med. J. (Engl.) 127(20), 3651–3656.
Claesson MJ, Jeffery IB, Conde Set al. Gut microbiota composition correlates with diet and health in the elderly. Nature 488(7410), 178–184 (2012).
Jason M. Ridlon, Spencer C. Harris, Shiva Bhowmik, Dae-Joong Kang & Phillip B. Hylemon (2016)Consequences of bile salt biotransformations by intestinal bacteria, Gut Microbes, 7(1), 22-39.
Vrieze A, Van Nood E, Holleman F et al. (2012) Transfer of intestinal microbiota from lean donors increases insulin sensitivity in individuals with metabolic syndrome. Gastroenterology143(4)
Chen, L., Wang, W., Zhou, R., Ng, S. C., Li, J., Huang, M., … Xia, B. (2014). Characteristics of fecal and mucosa-associated microbiota in Chinese patients with inflammatory bowel disease. Medicine, 93(8)
Jost, T. , Lacroix, C. , Braegger, C. P., Rochat, F. and Chassard, C. (2014), Mother–neonate bacterial transfer. Environ Microbiol, 16, 2891-2904
Van den Abbeele P, Belzer C, Goossens M, et al. Butyrate-producing Clostridium cluster XIVa species specifically colonize mucins in an in vitro gut model. ISME J. 2013;7(5):949-961.