此前,三位高中生引爆了医药圈,他们使用人工智能(AI)引擎进行靶点发现,确定了多形性胶质母细胞瘤(GBM)的新治疗靶点,多形性胶质母细胞瘤(GBM)是最具侵袭性和最常见的恶性脑肿瘤类型,占所有原发性脑肿瘤的16%。他们合作撰写的论文于4月26日发表在国际科学期刊《衰老》(aging)上,显示了人工智能系统辅助新药研发的广阔前景。
人工智能技术正在从成本、效率等方面重塑制药行业。近年来,相关专家认为,AI 制药将成国内医药产业弯道超车机遇,应以 AI 制药为切入点,对这一新兴领域加强前瞻性政策扶持,推动整个中国创新药行业的原始、自主创新,或许在制药领域,真正走向中国“智”造就在于人工智能技术的成熟应用。
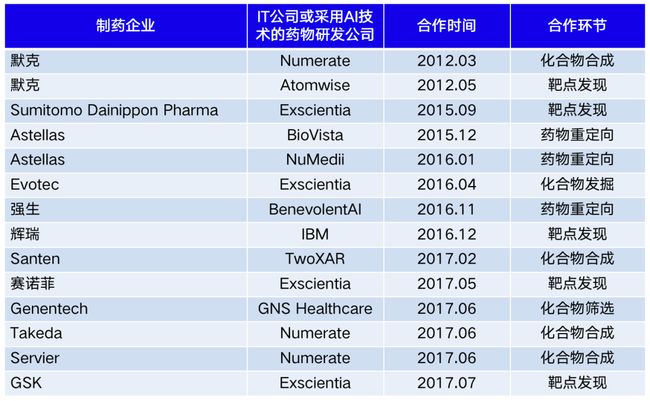
目前在制药领域,AI 制药主要由三大类公司进行相互协作共同推进药品研发进程,IT 技术公司、药物研发 CRO 公司以及大型药企。IT 公司利用自身的互联网基础与平台优势赋能行业应用,大型药企则拥有药物研发的相关数据、成熟的研发管线以及资深的药物专家,在优势互补的情况下,目前已经可以看到AI制药的很多成熟案例。
我国 AI 制药起步较欧美起步稍晚,但发展迅速,更具数据、算法等优势,在前段时间结束的百度飞桨中国行·上海站活动中,杭州立德百克生物医药总经理王紫壹博士讲述了他如何针对乳腺癌开展 CDK4/6 抑制剂的 AI 制药之路。
根据世卫组织发布的数据,早在2020年,乳腺癌就在全球新发病例上超过肺癌,成为世界第一大癌症。我国则是全球乳腺癌发病人数最多的国家,每年新发病例数接近42万。
而 CDK4/6 抑制剂是目前全球范围内治疗乳腺癌最为畅销的药物,用于治疗HR阳性/HER2阴性的乳腺癌患者。比如,恒瑞医药的达尔西利、美国辉瑞的哌柏西利和美国礼来的阿贝西利等三款药已在中国获批上市,其中阿贝西利还进入了国家医保目录。
但 CDK4/6 抑制剂在给广大患者带来福音的同时,也存在着“瑕疵”,比如难以避免的产生了不同程度的耐药性以及临床副作用,而且同质化竞争异常激烈。这就要求独辟蹊径,开发全新机制的 CDK4/6 抑制剂乳腺癌药物。
对此,王紫壹团队提出利用 CDK4/6 的激酶活性必须依赖于自身同 CCND(细胞周期素D)形成复合物这一关键特性,开发出能阻断 CDK4/6-CCND 蛋白-蛋白相互作用的小分子化合物,同样能够使 CDK4/6 激酶失去活性,进而达到抑制乳腺癌细胞生长的目的。
新药研发思路确定后,一个老大难问题再次浮现,即需要找到对应的目标分子。这一过程的快慢,在过去只能取决于运气。而王紫壹团队拒绝墨守成规,选择了一条新路径,采用百度飞桨螺旋桨生物计算平台提供的文心生物计算大模型能力来进行药物发现的工作,成效令他颇为惊艳,仅仅几个小时内,就在780万个化合物的虚拟筛选库中筛选出了110个打分较高的潜在候选分子。
立德百克构建了特异性的检测方法对筛选出的化合物进行活性检测,从110个分子中采购了40个进行湿实验检测,最后发现有6个高潜力分子,其中3个化合物能同时打断 CDK4/6-CCND 蛋白-蛋白相互作用,还有3个化合物能打断 CDK4-CCND 蛋白-蛋白相互作用。目前,双方团队正对这些化合物做更进一步的研究,有望在不久的将来将这种新型抑制剂推向临床。
据介绍,相比于现有 CDK4/6 抑制剂,新型药物属于机制创新的首创新药,具备更优的特异性,并在耐药性与潜在副作用上更有优势,这将为广大乳腺癌患者带来福音。得益于这些优势,新型药物有望打开可观的市场空间。
王紫壹博士介绍道,“百度拥有国内领先的AI+药物研发的技术能力,特别是文心生物计算大模型在国内是非常领先的,运用这些技术能力,飞桨螺旋桨帮助我们更高效的找到苗头化合物分子,这大大提升了我们药物发现的效率。”
百度飞桨螺旋桨(PaddleHelix)是基于飞桨深度学习框架打造的“AI+生物”计算平台,提供文心大模型-生物计算大模型能力,已开放多个算法模型,覆盖小分子药物筛选、多肽/蛋白药物设计、mRNA 疫苗/药物设计等技术,面向新药研发、疫苗设计、精准医疗等场景,为生物医药领域的创新药企、医药技术提供商、科研机构、生物科技公司等提供全面的算法工具和技术方案。
目前在华东区域,已有不少企业采用飞桨螺旋桨平台开展了相关药品研发。除杭州立德百克联合百度飞桨螺旋桨开发乳腺癌创新药之外,索智生物也在多个领域与飞桨螺旋桨合作,其中 ADMET 性质预测大模型 HelixADMET,已经整合到索智自身的AI药物发现平台(AIxMol®),并成功应用于其在研管线项目,有效地帮助索智提升合成测试湿实验成功率,进而提高整体研发效率,在短短的18个月中成功确定了3个 PCC 分子。
数据显示,40-45%临床试验的失败归结于药物的高毒性和低类药性。如果能够在药物研发的早期就排除性质不佳的分子,就可以省下大量的时间和资金投入。因此,化合物的成药性预测(简称ADMET)对新药研发的成功至关重要。ADMET 是药物代谢动力学所关注的化合物在体内的吸收、分布、代谢和排泄行为 (简称ADME) 与毒性 (Toxicity) 的合称,是衡量化合物成药性最重要的参考指标。
针对该问题,业界已经提出了很多解决方案,比如 admetSAR、ADMETlab、swissADME 等,但这些方法训练所使用的数据集量级普遍较小,故在对未知骨架结构的化合物进行性质预测时效果较差,同时无法基于用户需求做指标拓展。未知骨架结构的化合物进行性质预测泛化能力较差,药物设计成本较高,可拓展性存在一定阻力。
而飞桨螺旋桨的 HelixADMET 大模型可在60秒内计算1000个分子的 ADMET 相关指标。对比国内外多个知名的 ADMET 预测软件,在功能的完整度(预测52项指标)和指标上的精度上(超过其他对比平台4个百分点以上),都大大超过竞品。相应的研究已被收录在生物信息学领域的顶级期刊 Bioinformatics 上。
可以预见,在生物制药领域,HelixADMET 大模型可以应用于化合物优化/筛选阶段,辅助决策优先进入临床的化合物,规避后期的可能风险;还能指导学术/项目的研究计划制定,减少盲目实验的概率;同时模型可以用于验证新药/仿制药的成药性,评估新药/仿制药的风险,大大提高药效研究的效率,更快地评估和验证新药/仿制药的效果。
此外,在5月2日,国际顶级学术期刊《Nature》正刊发表了百度与合作单位在生物计算领域的突破性成果 ——《Algorithm for Optimized mRNA Design Improves Stability and Immunogenicity》,提出 mRNA 序列优化算法 LinearDesign,百度赫然以第一完成单位署名该研究。以新冠病毒Spike蛋白为例,该算法能在短短11分钟之内找到最稳定的 mRNA 候选序列。
实验数据证明,LinearDesign 算法设计序列将有助于生物医药公司快速研发更有效的 mRNA 疫苗,缩短研发周期,降低研发成本。这一算法的有效性已经在新冠 mRNA 疫苗和带状疱疹 mRNA 疫苗两种疫苗中得到验证。与传统基准相比,百度的设计显著改善了体外 mRNA 半衰期和蛋白质表达,使体内抗体反应增强了高达128倍。
结语
人工智能最广泛应用领域或在药物研究,一项新药物的研发,研究人员常需要通过设计、合成和评估多种化合物来创造潜在新型药物,将具有发展前景的化合物精制为候选药物的过程常常既昂贵又耗时。假如将人工智能与药物研究相结合,不仅投入资本将大大减少,效率也会大幅度提高。但是,就目前而言,我们仍然面临发展中的瓶颈,AI 制药未来是否能够快速发展应从体制上全面激发我国 AI 制药产业活力,在人才培养、监管审批、园区建设、数据管理多角度予以扶持,推动 AI 制药实现我国的创新药研发“革命”,最后让我们期待人工智能技术的“第四次科技革命”。