7+脂肪酸代谢+免疫,简单又高效,思路简单到让你怀疑人生
今天给同学们分享一篇生信文章“Prognosis and Dissection of Immunosuppressive Microenvironment in Breast Cancer Based on Fatty Acid Metabolism-Related Signature”,这篇文章发表在Front Immunol期刊上,影响因子为7.3。
结果解读:
癌症患者预后脂肪酸代谢相关基因的鉴定
最初,作者总结了TCGA-BRCA队列中269个FMG中CNV的发生率和DEG的鉴定。通过研究CNV的频率,作者注意到FMG存在普遍的CNV改变,并且显示了处于扩增或缺失CNV状态的前20个基因(图1A)。此外,作者通过使用|log2FC|>1和FDR<0.05的阈值将1082个BC样本与113个正常乳腺样本进行比较,检测到72个DEG。在DEG中,BC患者有40个FMG显著增强,而BC样本中有32个FMG基本减弱(图1B、C)。为了确定每种可用FMG的潜在预后价值,采用单变量Cox风险回归分析来筛选METABRIC和TCGA-BRCA数据集中与OS相关的FMG(图1D、E),分别检索到103和29个显著的OS相关FMG。将两个队列的结果交叉,11个交集的OS相关FMG(HCCS、CPT1A、CYP4F11、HMGCS1、SCD、ELOVL1、GSTZ1、CEL、RDH16、LTA4H和SDHA)有资格进行进一步分析(图1F)。此外,以上11个FMG的两个数据集中的染色体位置和表达水平通过circos图说明(图1G)。通过相关矩阵图揭示了这些基因之间的相关性特征(图1H)。
癌症患者脂肪酸代谢相关预后标志的构建
在TCGA-BRCA队列中对11个候选OS相关FMG进行Lasso-Cox回归,旨在挖掘最佳FMG以建立预后特征。最终,提取了六个关键的FMG来构建基因特征,其包含CPT1A、CYP4F11、HMGCS1、ELOVL1、GSTZ1和LTA4H(图2A、B)。此外,为了进一步挖掘包含FMG的每个特征的表达水平和独立预后能力,展示了训练集中表达水平的盒图(图2C)和OS的K-M曲线(图2D)。从结果中,作者发现在BC样品中HMGCS1、ELOVL1和GSTZ1的表达水平显著提高,而LTA4H的表达水平相对降低。然而,CPT1A和CYP4F11既没有显著增加也没有显著下降。在OS的分离K-M分析中,ELOVL1和CPT1A的高表达组以及LTA4H、CYP4F11和GSTZ1的低表达组表示OS比另一个比较组受损更多,而HMGCS1的表达水平对BC患者的OS的影响可忽略不计。此外,在人类BC细胞系中验证了ELOVL1和LTA4H的RNA表达水平,其结果表明,与乳腺上皮细胞系MCF10A相比,ELOVL1在包括BT549、MDA-MB-231、SK-BR-3和T47D在内的BC细胞系中显着促进,而LTA4H在除SK-BR--3以外的BC细胞株中减少。
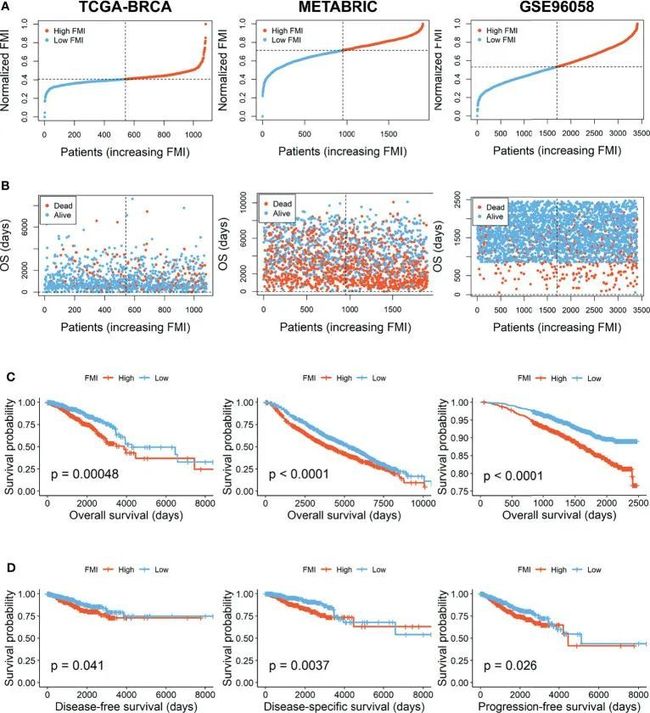
根据签名,每个患者的FMI计算如下:FMI=CPT1A*0.000952的表达−CYP4F11*0.003123的表达+HMGCS1*0.000327+ELOVL1*0.000245的表达−GSTZ1*0.002498的表达−LTA4H*0.000609的表达。此外,根据训练集中FMI的中值,BC患者可以分为高FMI组和低FMI组,并对FMI进行调整,使数据更加直观(图3A)。TCGA-BRCA数据集中,高FMI组的死亡患者比例大于低FMI组(图3B)。为了评估FMI的预后可行性,进行了K-M分析,以解读高FMI组的OS比低FMI组差得多(图3C),与训练集中DSS、DFS和PFS的评估相同(图3D)。
基于6个脂肪酸代谢相关基因的签名验证
为了进一步验证基于训练集中6个FMG建立的FMI的预后意义,在两个外部验证集METABRIC和GSE96058中进行了相同的研究。使用相同的FMI计算公式,BC患者被分为两个数据集中的高FMI组和低FMI组(图3A)。正如预期的那样,随着GSE96058中FMI的增加,具有死亡状态的BC患者的数量逐渐增加,但在METABRIC中没有(图3B)。与训练集一致,在验证集中,高FMI组比低FMI组涉及更多恶化的OS(图3C)。
癌症患者脂肪酸代谢指标与临床参数的综合评价
为了确定FMI在预测其他临床参数方面的可用性,作者进一步确定了FMI与临床特征之间的关系。在训练集中,在不同程度的不同临床参数(包括生存状态、临床病理T、临床病理N和AJCC分期)中,调整FMI存在显著差异(均p<0.05),FMI越高可能与上述临床特征的趋势越严重有关(图4A)。同样,除了GSE96058数据集中的阳性节点(图4C)外,在多样化临床参数的不同水平上再次确认了显著差异,包括METBRIC验证集中的PAM50亚型、肿瘤大小、阳性节点和AJCC阶段(图4B),以及PAM50子型、肿瘤尺寸和患者状态,这表明FMI升高越多与临床因素有关,意味着BC患者的生存能力受损越多。每个涉及FMI的FMG的表达水平与TCGA-BRCA和METBRIC数据集中可用的临床参数之间的综合相关性分析如图4D、E所示。
脂肪酸代谢相关临床病理诺模图的建立与评价
为了阐明FMI是否是BC的独立预后指标,在训练集中进行了单变量和多变量Cox回归分析(图5A、B),其结果表明,在单变量Cox分析中,年龄、T、N、AJCC分期和FMI与BC患者的OS显著相关(均p<0.001),在多变量Cox分析中,FMI是独立的预后预测因子(均p<0.01)。基于上述结果,开发了一个具有最佳一致性指数(C指数,0.76)的临床病理诺模图,该诺模图将FMI与另外两个临床特征(包括年龄和AJCC分期)相结合,以预测2年、3年和5年的个体OS(图5C)。为了证实列线图令人满意的预测判别,绘制了校准图,并发现其更接近理想曲线(图5D),这表明列线图具有完美的稳定性。随后,DCA得出诺模图比单一独立临床特征获得了更大的净效益(图5E)。简而言之,从多个方面阐明了预后列线图的有效性。
高、低脂肪酸代谢指标组间基因集富集分析
进行GSEA是为了破译训练集中高FMI组和低FMI组之间主要富集的信号通路和生物功能。如图6A、B所示,使用Hallmark数据库的结果表明,G2/M检查点、胆固醇稳态、PI3K–AKT–mTOR信号、TGF-β信号和mTORC1信号在高FMI组中基本富集,而细胞周期、ERBB信号通路、FCγR介导的吞噬作用、糖脂生物合成内酯和新内酯系列,通过KEGG数据库的GSEA结果,高FMI组中WNT信号通路丰富。
免疫治疗和肿瘤免疫微环境景观的潜在意义
用于免疫疗法和靶向治疗的新分子,如免疫检查点,目前在治疗BC患者的临床前或临床试验中进行了观察和评估。因此,对训练集中低FMI组和高FMI组之间8个候选免疫检查点的表达水平的比较表明,包括PDCD1(PD-1)、CD274(PD-L1)、CTLA4、IDO1、CD96、TIGIT、LAG3和PVR在内的靶标的表达水平在高FMI组中均显著放大(图6C)。在另外两个验证集中也存在类似的结果。这些结果表明,FMI较高的BC患者可能对针对上述检查点的治疗反应更强。
为了进一步揭示TME的前景,对训练集中FMI定义的BC TME中的免疫浸润细胞进行了分析,结果发现,在高FMI组的TME中,激活的记忆CD4+T细胞和巨噬细胞M0和M1显著增强,而激活的自然杀伤(NK)细胞、单核细胞、静息树突状细胞,而静息肥大细胞在低FMI组中被显著激活(图6D)。然后,作者还分别分析了LM22在基底亚型和非基底亚型BC中的分布。在基础亚型中,CD8+T细胞减弱,而巨噬细胞M0在高FMI组中显著增强。在非基础亚型中,在低FMI组中,幼稚B细胞、活化NK细胞、单核细胞、静息DC和静息肥大细胞富集,而活化记忆CD4+T细胞和巨噬细胞M0显著减弱。有趣的是,在基础亚型或非基础亚型中未检测到浸润性M1巨噬细胞富集的主要差异。
因此,作者进一步仔细研究了FMI特征与TME免疫抑制因子表达水平之间的相关性,这些因子包括免疫抑制性TME的关键细胞因子、IL-10和TGF-β、Treg标记物FOXP3、癌症相关脂肪细胞激活的标记物IL-6和CAF标记物FAP。在训练集中,上述五种细胞因子和标志物的表达水平在高FMI中增强(图7A)。除了METABRIC中的FOXP3和GSE96058中的FAP外,两个外部验证数据集中也出现了类似的趋势,这两个数据集的表达水平在两个比较FMI组中略有不同(图7B、C)。总之,上述结果表明,高FMI组的BC患者可能仍存在强烈的免疫抑制性TME,这种TME有助于肿瘤细胞的免疫逃逸和预后受阻。
癌症不同治疗方案脂肪酸代谢指标的预后研究
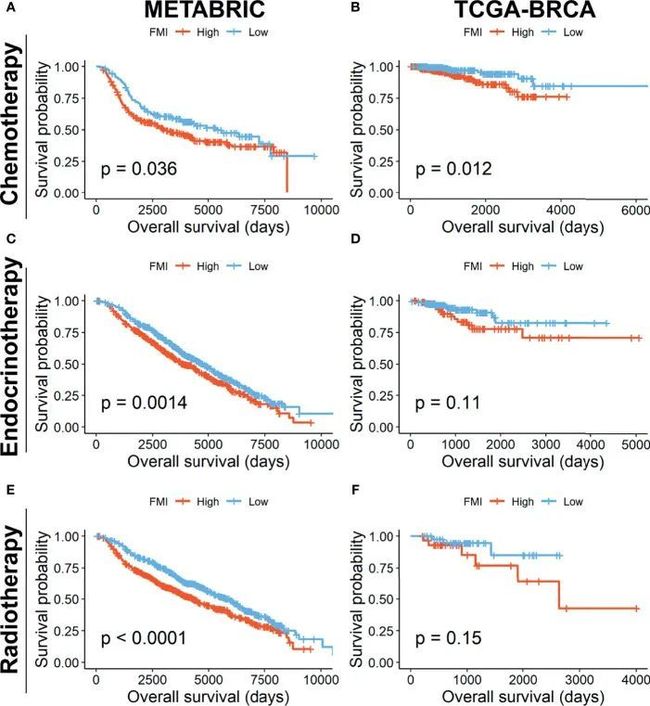
此外,作者还研究了接受不同治疗方案的BC患者的FMI特征对预后影响的可靠性。在METABRIC组中,高FMI组接受传统化疗的BC患者(n=412)的OS比低FMI组更差(图8A),接受内分泌治疗(n=1174)和放射治疗(n=1137)的患者也是如此(图8B,C)。同样,在TCGA-BRCA集合中,高FMI组中接受化疗的BC患者(n=499)获得了缩短的OS时间(图8D),而两个FMI组之间接受内分泌治疗(n=264)和放疗(n=72)的患者的意义有限(图8E,F),可能是由于缺乏样本。
总结
总之,作者的研究基于FA代谢相关基因构建了一个可靠的预测信号。签名被明确为一个独立的预后因素,并建立了一个由作者设计的签名组成的具有高度实用性的列线图。作者的特征与免疫抑制性TME之间的潜在相关性已被破译。由一个特征定义的治疗耐药性的含义被解开了。简言之,作者的研究支持FA代谢对癌症研究的关键临床前意义。