人工智能在老年痴呆疾病早期预警临床应用的研究
人工智能在老年痴呆疾病早期预警临床应用的研究
一, 研究背景
老年痴呆(seniledementia)是老年人发生的所有类型痴呆的统称,包括阿尔茨海默病(Alzheimer's disease,AD)、血管性痴呆(vascular dementia, VD)、混合性痴呆(AD 与VD的病理变化同时存在)以及其他原因所致的痴呆[1][q1] ,其中AD的患病率占老年痴呆的60%~70%[2][q2] 。阿尔茨海默病(Alzheimer's disease, AD),是一种隐匿起病的以进行性认知功能下降和行为损害为特征的中枢神经系统退行性疾病,其特征性病理变化为大脑皮层萎缩,并伴有β-淀粉样蛋白(β-amyloid, Aβ)沉积、神经元纤维缠结(neurofibrillary tangles, NFT)以及大量神经元数目减少[3-5][q3] 。随着老龄化社会的到来,AD患者逐年増多,国际老年痴呆协会发布的数据显示:2013年,全球老年痴呆人数为4400万,其中50%-75%为阿尔茨海默病患者。2015年,全球新增990万名痴呆患者,平均每3秒新增1人。在全球范围内,2015年护理老年痴呆产生的总费用预计为8180亿美元,与2010年相比,增加了2140亿美元。[6][q4]
据评估,在未来20年AD患者将达到目前的双倍,至2050年将有约11540万人患该病。AD是在癌症和心脏病之后的第3位花费最大的疾病,在老年人中,AD是继心脏病、肿瘤、脑猝死后的第四位死亡原因。自2000年以来,死于AD的患者较前增长了68%,AD逐渐成为全球主要死亡原因之一。经流行病学调查,发达国家65岁以上老年人患病率约4%-8%,在我国约3%-7%,据此,目前我国大约有AD患者600万-800万, 近几年每年新增30万。 2014年的调查数据显示,中国有90%的阿尔兹海默症患者未经过诊断治疗。阿尔茨海默病的患病率随年龄增高而增高,85岁以上老年人中平均每3-4位就有1位罹患AD。[7][q5]
AD的患病原因尚不明确,目前还没有有效逆转或阻止该病进展的特效方法。轻
度认知障碍(mild cognitiveimpairment, MCI)是老年人出现轻度记忆或认知障碍,介于正常老化和早期痴呆之间,但不符合痴但呆的诊断标准。MCI患者可呈现稳定的非进行性症状,但也可以观察到疾病的进展(通常渐变),发展到痴呆[8][q6] 。流行病学调查,MCI总发病率为20.8%[9][q7] ,每年约有10%~15% MCI老年人进展为AD[1][q8] 。目前AD发现时多为中、晚期,缺乏有效的治疗方法。如能准确预测MCI是否会进一步转化为AD,对疾病的认识和早期干预均有重要意义。如果疾病发现的早,阿尔茨海默症是可以通过药物治疗和控制的,能够帮助患者改善认知功能、延缓临床病程10-15年。发达国家中每位阿尔兹海默症患者平均每年耗用33000美元。早期的诊断和诊断介入,可使患者显著延后入住看护机构,平均每年可净节省10000美元的费用,因此对AD的早期诊断、早期干预尤为重要。
目前国内各大医院的神经内科、精神科、老年科的记忆障碍门诊均可对阿尔茨海默病进行诊断。其中,常规诊断程序包括病史回顾、体格检查、痴呆筛查测试(量表评估)、脑神经系统检查及实验室检查(如血生化及CT、MRI、PET/SPECT等脑部扫描检查)等。这些方法对疾病的诊断有作用,但是前提是需要有经验的医生,而且这些方法并不适用于大规模的早期筛查。
影像学检查在AD早期检测中发挥着重要作用,随着大数据+医疗时代的到来,人工智能在医学影像上的作用越来越凸显,利用深度学习技术来辅助医生诊断,可以大大提高医生的效率、减轻医生工作量,不仅可以挽救无数患者的生命,而且对于缓解医疗资源和医患矛盾也有重大意义。
二, 阿尔兹海默症的影像学检查
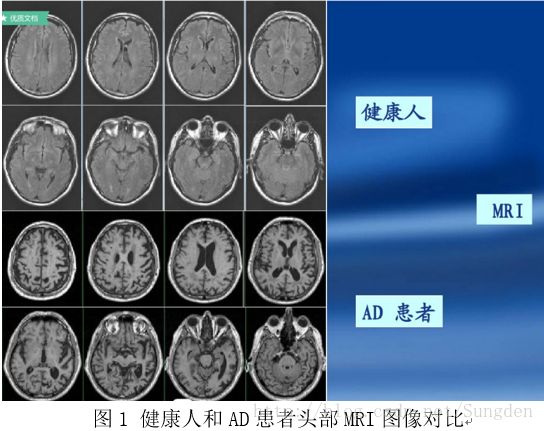
AD的检查主要有神经心理学测查(如MMSE、MOA等)和影像学检查(CT、PRT或MRI),其中影像学检查可提供痴呆的脑组织损害等异常情况,这是近年来医学的一个突破性进展,在现实的临床中,CT、MRI、PET/SPECT各种影像都可以用来诊断老年痴呆症,但MRI具有软组织分辨率高、能分辨灰白质界限、无损伤、无辐射及无骨伪影、可在任意方向直接断层,对脑内结构的线性、面积和体积进行测量等优点[10][q9] ,特别是在斜冠状面显示颞叶、海马的萎缩更准确可靠。同时MRI的结构性扫描在临床应用广泛,非常容易获得,获取成本低,时间短,通常情况下,患者拍MRI图像的成本在几百元左右,相比于PET\CT要便宜的多,另外拍摄时间短,不会对临床工作带来很多干扰。因此美国放射科学会也推荐结构MRI图像是诊断AD(阿尔兹海默症)的最佳影像学方式。从头部MRI影像中可以发现,AD患者的大脑皮层灰质萎缩更明显、颞叶、额叶、枕叶皮层相对容积较其他脑区减少明显、白质相对容积减少不明显。如图1所示:
图1 健康人和AD患者头部MRI图像对比
三, 国内外研究现状
随着卷积神经网络(CNN)在图像识别上取得重大突破,其在医疗图像处理上的应用已成为当下的一个研究热点。将深度学习方法应用于AD病的早期检测,正是在这种背景下应运而生。Saman Sarraf和Ghassem Tofighi[11-13][q10] 等运用LeNet-5网络模型在区分AD病MRI图像和正常MRI图像上取得了98.84%的准确率,他们又将LeNet-5网络分别用在fMRI图像和fMRI与MRI结合的图像区分上,取得了96.85%和97.77%的准确率;国内学者赵地等提出增强的AlexNet网络模型利用AD病MRI图像在早期诊断上得到了较好的测试结果;英国伦敦的一家公司Avalon AI宣称其开发的模型在AD病MRI图像上的预测准确率可以达到75%,但具体算法没有披露[14][q11] 。Ronghui Ju,Chenhui Hu等[15][q12] 利用脑网络深层学习和临床相关的文本信息对阿尔茨海默病进行早期诊断,准确率比传统的方法提高了31.21%;Jun Shi, Xiao Zheng等[16][q13] 利用多模态层叠多项式网络多模态神经影像特征学习诊断阿尔茨海默病。总的来说,目前用深度学习来诊断AD病有两种思路:一是利用医学软件先对MRI图像进行一部分预处理,分割出灰白质,然后送入神经网络进行分类;二是结合多种影像信息(比如MRI和PET,fMRI和PET)来进行判定。这两种思路都存在不足。第一种思路因为需要人工干预,耗时长,易造成疲劳误差;第二种思路需要结合多种影像信息,一般较难实现。
四, 方法
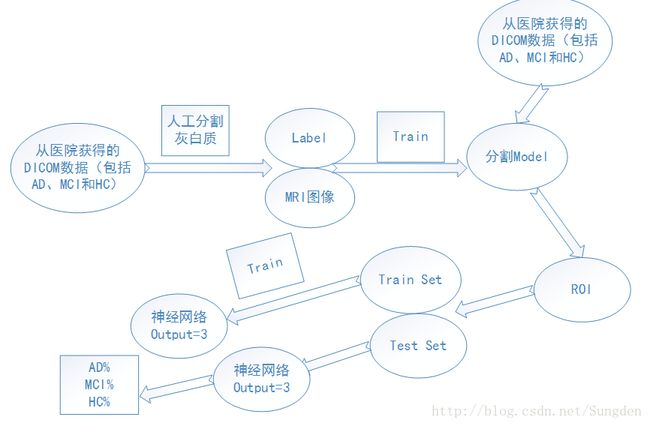
本文提出一种全自动诊断AD病的方法,即自动分割灰白质,送入神经网络,得到诊断结果。
创新点:1,自动分割灰白质;2,医院的临床数据(现有文献使用的都是公开数据库ADNI)。
流程图为:
[q1]影像学技术应用于阿尔茨海默病早期诊断的研究进展
[q2]Sadhu A, UpadhyayP, Agrawal A, et al. Management of cognitive determinants in senile dementia ofAlzheimer's type: therapeutic
potential of a novel polyherbal drug product [J]. Clin DrugInvestig, 2014, 34(12): 857- 869. doi: 10.1007/s40261-014-0235-9.
[q3]Cuttler JM, MooreER, Hosfeld VD, et al. Treatment of Alzheimer disease with CT scans: a casereport [J]. Dose Response,2016, 14(2):1559325816640073.doi:10.1177/1559325816640073.
Vemuri P, Lesnick TG, Przybelski SA, et al. Vascular andamyloid pathologies are independent predictors of cognitive decline
in normal elderly [J]. Brain, 2015, 138(Pt 3): 761-771.doi: 10.1093/brain/awu393.
Yanagisawa D, Amatsubo T, Morikawa S, et al. In vivodetectionof amyloid β deposition using 19F magnetic resonance imaging with a 19F- containingcurcumin derivative in a mouse model of Alzheimer's disease [J]. Neuroscience,2011, 184:120127.doi:10.1016/j.neuroscience.2011.03.071.
[q4]http://www.sohu.com/a/190336829_639566
[q5]武慧 阿尔茨海默病患者不同临床阶段颅脑磁共振和神经心理学对比研究
[q6]Cova I, Clerici F,Rossi A, et al. Weight loss predicts progression of mild cognitive impairmentto Alzheimer's disease [J].PLoS One, 2016,11(3):e0151710.doi:10.1371/journal.pone.0151710.
[q7]Jia J, Zhou A, WeiC, et al. The prevalence of mild cognitive impairment and its etiological subtypesin elderly Chinese [J].Alzheimers Dement, 2014, 10(4): 439- 47. doi: 10.1016/j.
jalz.2013.09.008.
[q8]Ganguli M, DodgeHH, Shen C, et al. Mild cognitive impairment,amnestic type:an epidemiologicstudy [J]. Neurology,2004, 63(1): 115-121.
[q9]Jin Z, Guan Y, YuG, et al. Magnetic resonance imaging of postoperative fracture healing processwithout metal artifact: a preliminary report of a novel animal model [J].Biomed Res Int, 2016, 2016: 1429892. doi: 10.1155/2016/1429892
[q10]Classificationof Alzheimer’s Disease Structural MRI Data by Deep Learning ConvolutionalNeural Networks
Classification of Alzheimer’s Disease Using fMRI Data and Deep
Learning Convolutional Neural Networks
DeepAD: Alzheimer’s Disease Classification viaDeep Convolutional Neural Networks using MRI and fMRI
[q11]可预测老年痴呆症患病概率Avalon AI 医学影像诊断玩出新花样
[q12]Early Diagnosis of Alzheimer’s Disease Based
on Resting-State BrainNetworks and Deep
Learning
[q13]Multimodal Neuroimaging Feature Learning
with Multimodal Stacked Deep Polynomial
Networks for Diagnosis of Alzheimer's Disease