- nodejs ,npm 发布包的一些问题
Batman_curry
开发npm前端node.js
你提到的问题非常实际,也是每个开发者在发布Node.js包时需要考虑的关键点。以下是逐步解答你的所有问题,并解释依赖管理、发布过程、依赖大小、冲突解决以及如何修改和托管到GitHub的具体细节。1.关于node-gyp和依赖问题:node-gyp是否会打包进我的库?当你运行npminstall-gnode-gyp时,-g表示全局安装,它不会安装在你的项目目录中,而是安装到全局环境中(如C:\Use
- AES加密解密CBC模式与ECB模式_aes cbc加解密
全栈_XzJ
python开发语言
一、概要AES(AdvancedEncryptionStandard)是一种对称加密算法,广泛应用于信息安全领域。AES支持多种密钥长度,包括128比特、192比特和256比特。在AES加密和解密中,同一个密钥用于两个过程。下面是一个简单的Python实例,演示如何使用AES加密和解密文本。这里使用的是Python标准库中的cryptography模块,确保你已经安装该模块:pipinstallc
- 第十一届蓝桥杯大赛软件赛省赛C/C++ 大学 A 组 子串分值
徽京人
蓝桥解析算法数据结构c语言c++蓝桥杯
题目描述对于一个字符串SS,我们定义SS的分值f(S)f(S)为SS中恰好出现一次的字符个数。例如f(aba)=1,f(abc)=3,f(aaa)=0f(aba)=1,f(abc)=3,f(aaa)=0。现在给定一个字符串S0⋯n−1S0⋯n−1(长度为nn,1≤n≤1051≤n≤105),请你计算对于所有SS的非空子串Si⋯j(0≤i≤jusingnamespacestd;intmain(){s
- C++容器string类
只有月亮知道
c++开发语言
C++中对于字符串的处理进行了特殊的封装,使得这个容器既具有普通容器的性质,又能对于字符串进行处理。下面对一些常用的string接口进行说明。1.构造函数首先来看string的构造函数。string()//构造空的string类对象string(constchar*s)//利用C-string来构造类对象string(conststring&s)//拷贝构造2.常用容量操作size_tsize()
- 蓝桥备赛指南(8):矩阵基础
神里流~霜灭
蓝桥备赛矩阵c++算法数据结构c语言排序算法
矩阵的乘法矩阵的乘法是《线性代数》中的基础内容。乘法规则:(行数和列数)只有当相乘的两个矩阵的左矩阵的列数等于右矩阵的行数时,才能相乘。(详细详看《线性代数》)矩阵的乘法的规则用一句话来描述就是第一个矩阵A的第i行和第二个矩阵B的第j列的各m个元素对应相乘再相加就得到新矩阵C[i][j]的值。如图:代码实现://代码实现//n行k列for(inti=1;i<=n;++i){for(intj=1;j
- Deepseek文生图、文生音乐、文生视频操作步骤(详细版)
SoulQuestor
Deepseek音视频人工智能deepseek
目录一、文生图方法一1.启动浏览器双击桌面上的浏览器图标,启动浏览器程序。2.访问DeepSeek官网3.进入对话界面4.输入图片生成代码方法二1.获取绘画提示词2.复制提示词3.使用AI绘画软件生成图4.优化和保存图片二、文生音乐1.启动浏览器并访问DeepSeek官网2.进入DeepSeek对话界面3.输入音乐主题并获取描述4.获取详细描述5.访问音疯平台6.进入音乐创作界面7.输入音乐描述并
- 贪心算法(11)(java)加油站
奋进的小暄
算法贪心算法算法
题目:在一条环路上有n个加油站,其中第i个加油站有汽油gas[i]升.。你有一辆油箱容量无限的的汽车,从第i个加油站开往第i+1个加油站需要消耗汽油cost[i]升。你从其中的一个加油站出发,开始时油箱为空。给定两个整数数组gas和cost,如果你可以按顺而环招行驶一周,则返回出发时加油站的编号,否则返回-1。如果存在解,则保证它是唯一的.示例1:输入:gas=[1,2,3,4,5],cost=[
- Kubernetes(K8S)学习笔记(2):Kubernetes架构
徐卷
分布式与并行计算kubernetes学习笔记云计算
注:该笔记整理自Kubernetes官方文档中的内容,笔记中使用的观点与资源均来源于官方文档以及我个人的理解,如果涵盖其它来源的观点,会额外标明引用。1、相关概念Kubernetes集群由一个控制平面与一组用于运行容器化应用的工作机器组成,我们把这些工作机器称之为节点(Node)。工作节点托管着组成工作负载的Pod,控制平面负责管理工作节点以及Pod,以下为Kubernetes集群组件的逻辑关系图
- SQLite Delete 语句详解
wjs2024
开发语言
SQLiteDelete语句详解SQLite是一种轻量级的数据库管理系统,广泛应用于移动设备、嵌入式系统和服务器端应用。在数据库管理中,删除数据是一项基本操作。SQLite提供了强大的删除功能,本文将详细介绍SQLite的Delete语句及其用法。1.Delete语句概述Delete语句用于从SQLite数据库中删除记录。其基本语法如下:DELETEFROMtable_nameWHEREcondi
- Python 爬虫实战:全球公司财报数据抓取与财务健康分析
西攻城狮北
python爬虫开发语言
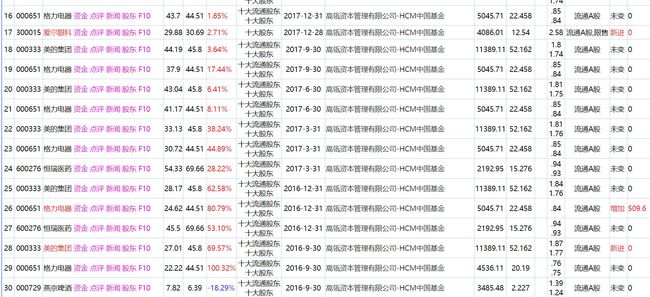
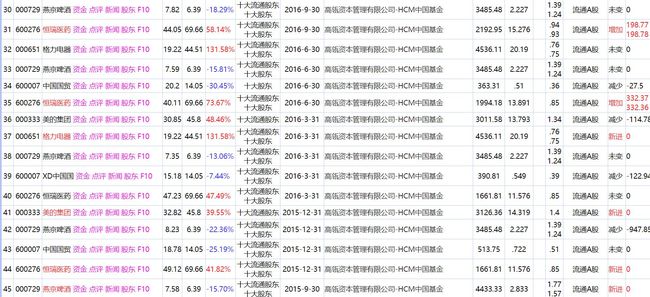
一、引言在当今数字化时代,数据已成为企业决策、投资分析和市场研究的关键要素。公司财报数据作为企业经营状况的重要反映,对于投资者、分析师以及企业管理者来说具有极高的价值。通过获取和分析全球公司的财报数据,我们可以深入了解企业的财务健康状况,为投资决策提供有力支持。本文将详细介绍如何使用Python爬虫技术抓取全球公司财报数据,并进行财务健康分析。二、爬虫环境搭建在开始爬取数据之前,我们需要先搭建好P
- 基于Matlab的大气湍流光束传输特性的研究
pk_xz123456
算法深度学习matlab开发语言
以下是一个基于Matlab实现大气湍流光束传输特性研究的详细代码及解释。%定义参数N=512;%网格点数L0=10;%外尺度(m)l0=0.01;%内尺度(m)Cn2=1e-14;%大气折射率结构常数(m^(-2/3))k=2*pi/0.6328e-6;%波数(m^(-1))z=1000;%传输距离(m)w0=0.1;%束腰半径(m)%生成随机相位屏[phase_screen]=generate_
- leetcode(1) 3.16-3.22
今天也要好好学习呀!
LeetCode算法
3.16–3.22刷题总结-LeetCode篇两数之和据说是leetcode入门必刷题,小菜鸡在遇到这种题第一反应:暴力!!!嗯,那肯定是不行的,所以,在众多资料中,成功使用HashMap完成了这个题呢。暴力法得时间复杂度为O(n2),在要求降低时间复杂度的情况下,则必须用空间来换。HashMap:建立数字与其坐标位置之间的映射,遍历一个数,另一个预先存储。思路:target-遍历到的数字=另一个
- Java中Scanner类应用详解
海边漫步者
Java基础java开发语言
Java中的Scanner类应用详解在java编程中,Scanner类是一个用于读取数据的常用工具,可以从文件、输入流、字符串中读取数据。本文从常用构造方法、常用方法两个方面讲解其功能并举例说明。该类尚有其他的构造方法与一般方法,有技术开发需求的读者可以从官网查看API文档学习应用。一、常用构造方法1.Scanner(InputStreamsource)功能:构造一个新的Scanner,它生成的值
- 在Springboot中集成unihttp后应用无法启动的解决办法
夜郎king
java集成Unihttp报错Java集成UnihttpSpring集成unihttp
目录前言一、最开始的应用集成1、使用unihttp定义第三方访问接口2、在SpringBoot应用中集成unihttp3、启动时发生的问题二、问题解决1、一种解决办法2、未来的优化三、总结前言在当今的软件开发领域,SpringBoot框架以其简洁、高效、灵活的特点,成为了众多开发者构建Java应用程序的首选。它能够帮助开发者快速搭建项目,简化繁琐的配置过程,让开发变得更加高效和便捷。而UniHtt
- 蓝桥杯 拔河
wuqingshun314159
蓝桥杯十五届蓝桥杯C/C++B组蓝桥杯职场和发展算法c++c语言数据结构
问题描述小明是学校里的一名老师,他带的班级共有n名同学,第i名同学的力量值为a_i。在闲暇之余,小明决定在班级里组织一场拔河比赛。为了保证比赛双方实力尽可能接近,需要在这n名同学中挑选出两个队伍:每个队伍内的同学编号连续,分别为:{a_l1,a_l1+1,...,a_r1}{a_l2,a_l2+1,...,a_r2}满足:l1≤r1#includeusingnamespacestd;typedef
- Java基础——常用运算符、scanner类介绍
咋说话呢?
java
目录一、.scanner类介绍1.使用方法2.next()方法与nextLine()方法二、常用运算符1.赋值运算符2.算术运算符3.关系运算符4.逻辑运算符5.位运算符6.条件运算符7.运算符的优先级一、.scanner类介绍Scanner类是一个用于Scanner指的是java.util包下的Scanner类,可以接收控制台输入的数据。位置:Java.util.Scanner;1.使用方法第一
- 刷题3.22
努力的小司仪
蓝桥杯专题蓝桥杯
1.算式900649fromitertoolsimport*s=['0','1','2','3','4','5','6','7','8','9']forpinpermutations(s,10):ifp[0]!=0andp[4]!=0andp[8]!=0:s=''.join(p)a=int(s[0:4])b=int(s[4:8])c=int(s[8:10])if(a-b)*c==900:print
- Linux的权限
巷子里的童年ya
linux运维服务器centos
基本权限与归属读取:允许查看内容-readr写入:允许修改内容-writew可执行:允许运行和切换-excutex1、对于文本文件:r读取权限:cat、less、grep、head、tailw写入权限:vim、>、>>x可执行权限:Shell与Python\Go2、对于目录:r读取权限:ls命令查看目录内容w写入权限:能够创建、删除、修改等目录的内容x执行权限:能够cd切换到此目录下(进入此目录)
- Java项目设计文档:架构、模块与实现策略详解
体制教科书
本文还有配套的精品资源,点击获取简介:Java项目设计文档是项目规划、实施和维护的重要指导工具,包含系统架构、模块划分、接口定义、类设计、数据库设计、异常处理、测试计划、性能优化以及部署运维等方面。本设计文档集合对于理解Java项目的架构设计和提升项目开发质量具有极高的参考价值。1.项目背景阐述在当今数字化转型的大潮中,企业对于IT系统的依赖日益加重。项目背景阐述这一章,将为您揭示本次项目的发起缘
- java调用自己写的类型_Java基础——自定义类的使用
跑马溜溜
java调用自己写的类型
自定义类我们可以把类分为两种:1.一种是java中已经定义好的类,如之前用过的Scanner类、Random类,这些我们直接拿过来用就可以了。2.另一种是需要我们自己去定义的类,我们可以在类中定义多个方法和属性来供我们实际的使用。什么是类呢?在java中,我们可以将现实生活中的事物通过描述来写成代码,我们可以自定义类来描述生活中的事物。比如我们可以将人进行描述,人的姓名,年龄,性别都是人的特有属性
- Java 程序员必读书单
AI天才研究院
DeepSeekR1&大数据AI人工智能大模型Java实战深度学习实战自然语言处理人工智能语言模型编程实践开发语言架构设计
作者:禅与计算机程序设计艺术1.简介Java是一门高级、新兴的静态面向对象编程语言,在互联网、移动互联网、大数据、云计算、人工智能、物联网等领域都有广泛应用。作为Java程序员的你是否也经常被面试官或者HR问到有关Java的知识点呢?如果你最近在准备面试或阅读相关技术文档,则本文正是适合你。在本文中,我将给你一些你可能不知道的关于Java的重要概念和知识,并通过具体的代码示例和图表来帮助你理解这些
- SvelteKit 最新中文文档教程(9)—— 部署静态站点与单页应用
前言Svelte,一个语法简洁、入门容易,面向未来的前端框架。从Svelte诞生之初,就备受开发者的喜爱,根据统计,从2019年到2024年,连续6年一直是开发者最感兴趣的前端框架No.1:Svelte以其独特的编译时优化机制著称,具有轻量级、高性能、易上手等特性,非常适合构建轻量级Web项目。为了帮助大家学习Svelte,我同时搭建了Svelte最新的中文文档站点。如果需要进阶学习,也可以入手我
- mysql外键设置
moxiaoran5753
mysql数据库
在mysql表设计时,如果巧用外键设置,可以给我们的开发带有很大的便利。应用场景:子表依赖于父表,或父子表存在某种关联;那么就存在父表或子表数据发生变化时,对应的子表或父表的数据应该作何改变;主要涉及以下处理:CASCADE,NOACTION,RESTRICT,SETNULL;下面简要概括下这4个设置适用的场景:1.CASCADE(级联操作)ONDELETECASCADE:当父表中的某条记录被删除
- html大学生网站开发实践作业:传统文化网页设计题材【绒花6页】HTML+CSS+JavaScript (1)
@码出未来-web网页设计
htmlcssjavascript
精彩专栏推荐文末获取联系✍️作者简介:一个热爱把逻辑思维转变为代码的技术博主作者主页:【主页——获取更多优质源码】web前端期末大作业:【毕设项目精品实战案例(1000套)】程序员有趣的告白方式:【HTML七夕情人节表白网页制作(110套)】超炫酷的Echarts大屏可视化源码:【Echarts大屏展示大数据平台可视化(150套)】HTML+CSS+JS实例代码:【️HTML+CSS+JS实例代码
- 大模型微调方法之Delta-tuning
空 白II
大语言模型论文解读微调方法介绍微调方法delta-tuning论文解读大语言模型
大模型微调方法之Delta-tuning大模型微调方法自从23年之后可谓是百花齐放,浙大有团队在8月将关于大模型微调方法的综述上传了ArXiv。论文将微调方法总结为等几个类别。本次讨论的1大模型业务分类当前的大模型行业可谓百花齐放,自然语言处理(naturallanguageprocessing,NLP)、计算机视觉(computervision,CV)、音频处理(audioprocessing,
- Python 学习笔记1 - 认识Python
Scora_liu
Python学习笔记python
一、什么是Python1989年圣诞节期间,荷兰数学和计算机科学研究学会的GuidovanRossum(吉多.范罗苏姆)决心开发一个新的解释程序,作为ABC语言的替代品。这门ABC语言的替代语言被取名为Python,命名来自Guido爱看的的电视剧MontyPython'sFlyingCircus(蟒蛇马戏团)。二、什么是Python(⭐⭐)Python是一门解释型语言。计算机不能识别任何除了机器
- C# SerialPort 类中 Handshake 属性的作用
鲤籽鲲
上位机c#开发语言上位机
总目录前言在C#的SerialPort类中,Handshake属性用于指定串口通信中的流量控制(FlowControl)方案,以协调发送方和接收方的数据传输速率,防止数据溢出或丢失。一、Handshake属性基本信息1.作用C#中SerialPort.Handshake属性的核心作用是通过硬件或软件流控制协议,管理串口通信中的数据流,防止缓冲区溢出并确保数据传输的可靠性。System.IO.Por
- HarmonyOS NEXT 基于原生能力获取视频缩略图
大家好,我是V哥。不得不佩服HarmonyOSNEXT原生能力的强大,如果你想在鸿蒙APP开发中获取视频缩略图,不用依赖第三方库,就可以高效和稳定的实现,AVMetadataHelper就是一个好帮手,下面V哥整理实现步骤的代码,帮助你快速理解,开整。想要学习鸿蒙开发,一定绕不开学习ArkTS语言,V哥写了三本鸿蒙开发之路的书,第一本《鸿蒙HarmonyOSNEXT开发之路卷1ArkTS篇》已上市
- 灵活运用HarmonyOS NEXT布局管理器,实现完美的自适应布局
harmonyos
灵活运用HarmonyOSNEXT布局管理器,实现完美的自适应布局在多设备和多样化的屏幕尺寸环境中开发应用时,创建一个既能适应不同屏幕尺寸又能保持良好视觉效果的布局至关重要。本文将深入探讨HarmonyOSNEXT提供的几种布局管理器及其工作原理,指导开发者如何利用这些工具实现高效的自适应布局,并提供API12版本的具体示例代码。Flex布局:沿主轴和交叉轴排列子元素Flex布局是一种强大的布局模
- 鸿蒙开发:正则中的match和matchAll
前言本文基于Api13关于正则表达式,其实之前也撰写过相关文章,但没有对match和matchAll做过详细的分析,虽然都是用于常见的字符串匹配,但是在使用方式上还是具有一定的区别;大家记住一点,正则表达式适用于所有的编程语言,可能有些语法和使用方式有些不同,但基本的原理是一样的。我们先看下源码:match:将字符串与正则表达式匹配,并返回一个包含该搜索结果的数组。/***Matchesastri
- HttpClient 4.3与4.3版本以下版本比较
spjich
javahttpclient
网上利用java发送http请求的代码很多,一搜一大把,有的利用的是java.net.*下的HttpURLConnection,有的用httpclient,而且发送的代码也分门别类。今天我们主要来说的是利用httpclient发送请求。
httpclient又可分为
httpclient3.x
httpclient4.x到httpclient4.3以下
httpclient4.3
- Essential Studio Enterprise Edition 2015 v1新功能体验
Axiba
.net
概述:Essential Studio已全线升级至2015 v1版本了!新版本为JavaScript和ASP.NET MVC添加了新的文件资源管理器控件,还有其他一些控件功能升级,精彩不容错过,让我们一起来看看吧!
syncfusion公司是世界领先的Windows开发组件提供商,该公司正式对外发布Essential Studio Enterprise Edition 2015 v1版本。新版本
- [宇宙与天文]微波背景辐射值与地球温度
comsci
背景
宇宙这个庞大,无边无际的空间是否存在某种确定的,变化的温度呢?
如果宇宙微波背景辐射值是表示宇宙空间温度的参数之一,那么测量这些数值,并观测周围的恒星能量输出值,我们是否获得地球的长期气候变化的情况呢?
&nbs
- lvs-server
男人50
server
#!/bin/bash
#
# LVS script for VS/DR
#
#./etc/rc.d/init.d/functions
#
VIP=10.10.6.252
RIP1=10.10.6.101
RIP2=10.10.6.13
PORT=80
case $1 in
start)
/sbin/ifconfig eth2:0 $VIP broadca
- java的WebCollector爬虫框架
oloz
爬虫
WebCollector主页:
https://github.com/CrawlScript/WebCollector
下载:webcollector-版本号-bin.zip将解压后文件夹中的所有jar包添加到工程既可。
接下来看demo
package org.spider.myspider;
import cn.edu.hfut.dmic.webcollector.cra
- jQuery append 与 after 的区别
小猪猪08
1、after函数
定义和用法:
after() 方法在被选元素后插入指定的内容。
语法:
$(selector).after(content)
实例:
<html>
<head>
<script type="text/javascript" src="/jquery/jquery.js"></scr
- mysql知识充电
香水浓
mysql
索引
索引是在存储引擎中实现的,因此每种存储引擎的索引都不一定完全相同,并且每种存储引擎也不一定支持所有索引类型。
根据存储引擎定义每个表的最大索引数和最大索引长度。所有存储引擎支持每个表至少16个索引,总索引长度至少为256字节。
大多数存储引擎有更高的限制。MYSQL中索引的存储类型有两种:BTREE和HASH,具体和表的存储引擎相关;
MYISAM和InnoDB存储引擎
- 我的架构经验系列文章索引
agevs
架构
下面是一些个人架构上的总结,本来想只在公司内部进行共享的,因此内容写的口语化一点,也没什么图示,所有内容没有查任何资料是脑子里面的东西吐出来的因此可能会不准确不全,希望抛砖引玉,大家互相讨论。
要注意,我这些文章是一个总体的架构经验不针对具体的语言和平台,因此也不一定是适用所有的语言和平台的。
(内容是前几天写的,现附上索引)
前端架构 http://www.
- Android so lib库远程http下载和动态注册
aijuans
andorid
一、背景
在开发Android应用程序的实现,有时候需要引入第三方so lib库,但第三方so库比较大,例如开源第三方播放组件ffmpeg库, 如果直接打包的apk包里面, 整个应用程序会大很多.经过查阅资料和实验,发现通过远程下载so文件,然后再动态注册so文件时可行的。主要需要解决下载so文件存放位置以及文件读写权限问题。
二、主要
- linux中svn配置出错 conf/svnserve.conf:12: Option expected 解决方法
baalwolf
option
在客户端访问subversion版本库时出现这个错误:
svnserve.conf:12: Option expected
为什么会出现这个错误呢,就是因为subversion读取配置文件svnserve.conf时,无法识别有前置空格的配置文件,如### This file controls the configuration of the svnserve daemon, if you##
- MongoDB的连接池和连接管理
BigCat2013
mongodb
在关系型数据库中,我们总是需要关闭使用的数据库连接,不然大量的创建连接会导致资源的浪费甚至于数据库宕机。这篇文章主要想解释一下mongoDB的连接池以及连接管理机制,如果正对此有疑惑的朋友可以看一下。
通常我们习惯于new 一个connection并且通常在finally语句中调用connection的close()方法将其关闭。正巧,mongoDB中当我们new一个Mongo的时候,会发现它也
- AngularJS使用Socket.IO
bijian1013
JavaScriptAngularJSSocket.IO
目前,web应用普遍被要求是实时web应用,即服务端的数据更新之后,应用能立即更新。以前使用的技术(例如polling)存在一些局限性,而且有时我们需要在客户端打开一个socket,然后进行通信。
Socket.IO(http://socket.io/)是一个非常优秀的库,它可以帮你实
- [Maven学习笔记四]Maven依赖特性
bit1129
maven
三个模块
为了说明问题,以用户登陆小web应用为例。通常一个web应用分为三个模块,模型和数据持久化层user-core, 业务逻辑层user-service以及web展现层user-web,
user-service依赖于user-core
user-web依赖于user-core和user-service
依赖作用范围
Maven的dependency定义
- 【Akka一】Akka入门
bit1129
akka
什么是Akka
Message-Driven Runtime is the Foundation to Reactive Applications
In Akka, your business logic is driven through message-based communication patterns that are independent of physical locatio
- zabbix_api之perl语言写法
ronin47
zabbix_api之perl
zabbix_api网上比较多的写法是python或curl。上次我用java--http://bossr.iteye.com/blog/2195679,这次用perl。for example: #!/usr/bin/perl
use 5.010 ;
use strict ;
use warnings ;
use JSON :: RPC :: Client ;
use
- 比优衣库跟牛掰的视频流出了,兄弟连Linux运维工程师课堂实录,更加刺激,更加实在!
brotherlamp
linux运维工程师linux运维工程师教程linux运维工程师视频linux运维工程师资料linux运维工程师自学
比优衣库跟牛掰的视频流出了,兄弟连Linux运维工程师课堂实录,更加刺激,更加实在!
-----------------------------------------------------
兄弟连Linux运维工程师课堂实录-计算机基础-1-课程体系介绍1
链接:http://pan.baidu.com/s/1i3GQtGL 密码:bl65
兄弟连Lin
- bitmap求哈密顿距离-给定N(1<=N<=100000)个五维的点A(x1,x2,x3,x4,x5),求两个点X(x1,x2,x3,x4,x5)和Y(
bylijinnan
java
import java.util.Random;
/**
* 题目:
* 给定N(1<=N<=100000)个五维的点A(x1,x2,x3,x4,x5),求两个点X(x1,x2,x3,x4,x5)和Y(y1,y2,y3,y4,y5),
* 使得他们的哈密顿距离(d=|x1-y1| + |x2-y2| + |x3-y3| + |x4-y4| + |x5-y5|)最大
- map的三种遍历方法
chicony
map
package com.test;
import java.util.Collection;
import java.util.HashMap;
import java.util.Iterator;
import java.util.Map;
import java.util.Set;
public class TestMap {
public static v
- Linux安装mysql的一些坑
chenchao051
linux
1、mysql不建议在root用户下运行
2、出现服务启动不了,111错误,注意要用chown来赋予权限, 我在root用户下装的mysql,我就把usr/share/mysql/mysql.server复制到/etc/init.d/mysqld, (同时把my-huge.cnf复制/etc/my.cnf)
chown -R cc /etc/init.d/mysql
- Sublime Text 3 配置
daizj
配置Sublime Text
Sublime Text 3 配置解释(默认){// 设置主题文件“color_scheme”: “Packages/Color Scheme – Default/Monokai.tmTheme”,// 设置字体和大小“font_face”: “Consolas”,“font_size”: 12,// 字体选项:no_bold不显示粗体字,no_italic不显示斜体字,no_antialias和
- MySQL server has gone away 问题的解决方法
dcj3sjt126com
SQL Server
MySQL server has gone away 问题解决方法,需要的朋友可以参考下。
应用程序(比如PHP)长时间的执行批量的MYSQL语句。执行一个SQL,但SQL语句过大或者语句中含有BLOB或者longblob字段。比如,图片数据的处理。都容易引起MySQL server has gone away。 今天遇到类似的情景,MySQL只是冷冷的说:MySQL server h
- javascript/dom:固定居中效果
dcj3sjt126com
JavaScript
<!DOCTYPE html PUBLIC "-//W3C//DTD XHTML 1.0 Transitional//EN" "http://www.w3.org/TR/xhtml1/DTD/xhtml1-transitional.dtd">
<html xmlns="http://www.w3.org/1999/xhtml&
- 使用 Spring 2.5 注释驱动的 IoC 功能
e200702084
springbean配置管理IOCOffice
使用 Spring 2.5 注释驱动的 IoC 功能
developerWorks
文档选项
将打印机的版面设置成横向打印模式
打印本页
将此页作为电子邮件发送
将此页作为电子邮件发送
级别: 初级
陈 雄华 (
[email protected]), 技术总监, 宝宝淘网络科技有限公司
2008 年 2 月 28 日
&nb
- MongoDB常用操作命令
geeksun
mongodb
1. 基本操作
db.AddUser(username,password) 添加用户
db.auth(usrename,password) 设置数据库连接验证
db.cloneDataBase(fromhost)
- php写守护进程(Daemon)
hongtoushizi
PHP
转载自: http://blog.csdn.net/tengzhaorong/article/details/9764655
守护进程(Daemon)是运行在后台的一种特殊进程。它独立于控制终端并且周期性地执行某种任务或等待处理某些发生的事件。守护进程是一种很有用的进程。php也可以实现守护进程的功能。
1、基本概念
&nbs
- spring整合mybatis,关于注入Dao对象出错问题
jonsvien
DAOspringbeanmybatisprototype
今天在公司测试功能时发现一问题:
先进行代码说明:
1,controller配置了Scope="prototype"(表明每一次请求都是原子型)
@resource/@autowired service对象都可以(两种注解都可以)。
2,service 配置了Scope="prototype"(表明每一次请求都是原子型)
- 对象关系行为模式之标识映射
home198979
PHP架构企业应用对象关系标识映射
HELLO!架构
一、概念
identity Map:通过在映射中保存每个已经加载的对象,确保每个对象只加载一次,当要访问对象的时候,通过映射来查找它们。其实在数据源架构模式之数据映射器代码中有提及到标识映射,Mapper类的getFromMap方法就是实现标识映射的实现。
二、为什么要使用标识映射?
在数据源架构模式之数据映射器中
//c
- Linux下hosts文件详解
pda158
linux
1、主机名: 无论在局域网还是INTERNET上,每台主机都有一个IP地址,是为了区分此台主机和彼台主机,也就是说IP地址就是主机的门牌号。 公网:IP地址不方便记忆,所以又有了域名。域名只是在公网(INtERNET)中存在,每个域名都对应一个IP地址,但一个IP地址可有对应多个域名。 局域网:每台机器都有一个主机名,用于主机与主机之间的便于区分,就可以为每台机器设置主机
- nginx配置文件粗解
spjich
javanginx
#运行用户#user nobody;#启动进程,通常设置成和cpu的数量相等worker_processes 2;#全局错误日志及PID文件#error_log logs/error.log;#error_log logs/error.log notice;#error_log logs/error.log inf
- 数学函数
w54653520
java
public
class
S {
// 传入两个整数,进行比较,返回两个数中的最大值的方法。
public
int
get(
int
num1,
int
nu