Original montreal 生信人 2020-01-29
日前,武汉肺炎病毒已经有了一个暂时的正式名字:新型冠状病毒,英文叫做2019-nCoV。很多人都会将它拿来与03年横行全国的SARS作比较。按理说,03年以后,SARS已经被彻底消灭了。但有没有这样一个可能,SARS当年的一小股残余势力遁出江湖,销声匿迹十余年,在最近“化身”2019-nCoV再度肆虐人间?
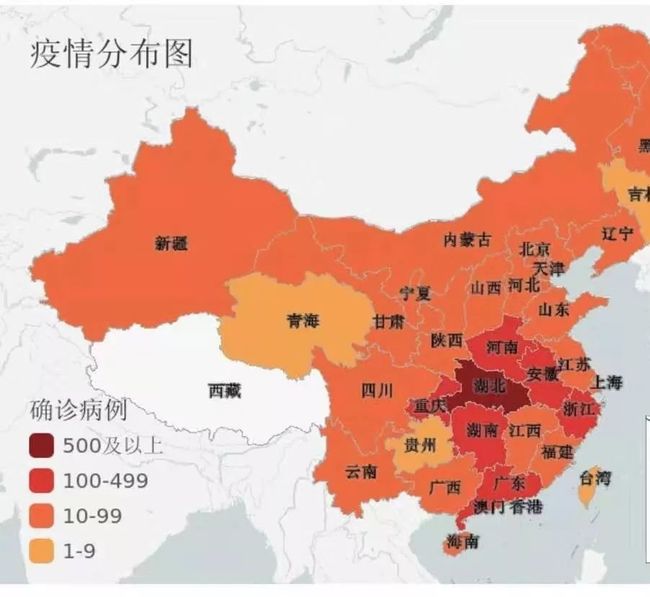
实时疫情最新情况(1月28日5点)
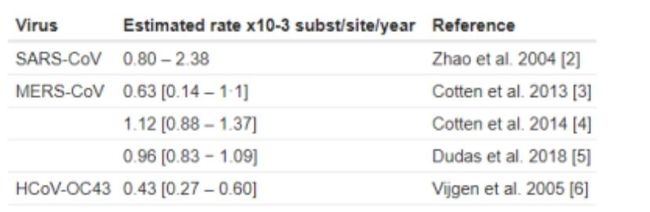
我们可以做一个简单的时间上的计算。假定SARS的后裔自03年以来一直活着,且在到20年的这17年里其DNA序列以0.001替换次数/位点/年的进化速率进化着(在下表的多种冠状病毒DNA的进化速率可以看出,这是一个对进化速率的合理估计)。
一些已知的冠状病毒的进化速度【1】
我们假设所有位点都以相等的速度突变,且认为每个位点最多只突变一次。那么,如果17年之后的2020,SARS的后裔存在,它与03年测到SARS的DNA的差异大概为0.001 * 17 = 1.7%。换言之相似度的期望是 1 – 1.7% = 98.3%。而我们知道,SARS与2019-nCoV的DNA identity(全同率,下文为简便称相似度)为80%,这与98.3%的差距是相当大的,我们可以很简单地排除2019-nCoV是SARS的可能性。
前不久,中科院武汉病毒所的石正丽实验室及合作者在biorxiv上po文,报道了2019-ncoro与他们在一种蝙蝠(中菊头蝠Rhinolophus affinis)身上分离得到的冠状病毒序列相似度达到了96.2%【2】。这听上去一个非常高的数字,且是现已知病毒里同2019-nCoV序列相似度最高的!显然,蝙蝠身上的病毒与2019-nCoV有一个共同祖先。那么,这个共同祖先的时间距今大概有多久呢?最简单的方法是先计算出差异 1-96.2%=3.8%,然后3.8% ÷ 0.001 ÷ 2 = 19(年)。最后除以2是因为蝙蝠采集到的病毒和都可以进化,这一点与前面SARS的例子不同,因为SARS的DNA序列是03年采集的样本,不能再变了,而被石正丽团队测序的蝙蝠病毒是03年后在云南采集的【2】。因此SARS的基因组序列应被视为来自“古代”,17年前就停止了变化,而石正丽团队采集到的蝙蝠身上的冠状病毒和2019-nCoV一样,它们的序列都是在最近(假设蝙蝠病毒也是近期采样,实际上可能是早前几年)才停止了变化。
如果再稍稍复杂一点,可以用JC69模型,它是Jukes和Cantor在1969年提出的【3】:2*r*t=-3/4*ln(1-4/3*p)。上式中,p为两条DNA序列差异的比例,r为速率,t为时间。上式左侧的2*r*t是distance的期望(由于是两条序列所以乘以2)。我们将r=0.001和p=3.8%代入上式,可得t=19.25(年),结果和上面最简单方法计算得到的结果十分接近。其实,当序列相似度较高时,用什么方法结果大差不差。
上面的计算都是在进化速率为0.001替代次数/年/位点的假设下进行的。如果我们假设一个更快的进化速率,0.002替代次数/年/位点(接近表1中的最高值),那么大概需要19÷2=9.5年。
再来看SARS。03年在人中分离到的SARS病毒与在果子狸中分离到的SARS病毒的DNA序列相似度为99.8%【4】。如果以0.001为替代速率做一简单估算,可得两者从最近共同祖先分道扬镳大概是在疫情爆发的0.2%÷0.001=1年之前。看上去,考虑其他各种误差(除了前面提及的假设外还包括:与SAR4更接近的果子狸病毒已无从查找),这对于从果子狸传给人到疫情爆发,时间算是足够近了,表明果子狸很可能是SARS的直接宿主。另一边,2017年,石正丽团队报道了云南一个山洞内发现的与SARS序列最接近的病毒,序列相似度为93%-96.2%【5】。再考虑此前分离到的蝙蝠身上的类SARS冠状病毒序列(SARS-related coronaviruses,SARSr-CoV),学界普遍认可蝙蝠是SARS天然宿主的结论。请注意,果子狸身上的病毒只有在广东养殖场养殖的果子狸才有找到,自然环境下生存的果子狸身上并未分离到,所以果子狸不是SARS的自然宿主,其携带的SARS应该是被天然宿主蝙蝠偶然传入,石正丽推测这一“传入”发生在云南【6】。
那么蝙蝠是否是本次爆发的新型冠状病毒的直接来源?参考03年非典的情况,可见前文提到的与2019-nCoV的96.2%的相似度,与当年果子狸与SARS的99.8%的相似度相比还是有不小差距。另外,前面估计从蝙蝠到人大概需要19年(最短也需要9.5年),对于病毒而言,这样的时间间隔也许意味着太多的可能——这其中当然包括存在中间宿主(intermediate host)的可能【7】。此外,有学者也认为,针对冠状病毒的研究,03年后很多病毒学家专注于对蝙蝠的研究,也会导致偏颇【8】。这一偏颇在一定程度上可以被宏基因组学纠正,不过,17年一项宏基因组学研究还是显示bats as the major evolutionary reservoirs and ecological drivers of CoV diversity【9】。纵使如此,仍需留意尽管每种蝙蝠所携带的冠状病毒最多,啮齿类动物(rodents)由于总数庞大,其作为一个整体所携带的病毒(不限于冠状病毒)总数要超过蝙蝠【10】。
引文
1. Rambaut, Andrew. “Preliminary phylogenetic analysis of 11 nCoV2019 genomes, 2020-01-19”
2. Zhou P, et al. (2020). "Discovery of a novel coronavirus associated with the recent pneumonia outbreak in humans and its potential bat origin". bioRxiv. doi:10.1101/2020.01.22.914952. Retrieved 24 January 2020.
3. Jukes TH, Cantor CR (1969). Evolution of Protein Molecules. New York: Academic Press. pp. 21–132.
4. Guan Y, Zheng BJ, He YQ, Liu XL, Zhuang ZX, Cheung CL, et al. Isolation and characterization of viruses related to the SARS coronavirus from animals in southern China. Science. 2003;302:276–8 10.1126/science.1087139
5. Hu B, Zeng L-P, Yang X-L, Ge X-Y, Zhang W, Li B, et al. (2017) Discovery of a rich gene pool of bat SARS-related coronaviruses provides new insights into the origin of SARS coronavirus. PLoS Pathog 13(11): e1006698.
6. 石正丽(2018)这些野生动物的病毒怎么就到了人类社会?一席
7. 徐鑫 (2020) 如何找到武汉肺炎病毒的源头 科学网
8. Banerjee, Arinjay, et al. "Bats and coronaviruses." Viruses 11.1 (2019): 41.
9. Anthony, Simon J., et al. "Global patterns in coronavirus diversity." Virus evolution 3.1 (2017).
10. Luis, Angela D., et al. "A comparison of bats and rodents as reservoirs of zoonotic viruses: are bats special?." Proceedings of the Royal Society B: Biological Sciences 280.1756 (2013): 20122753.
往期文章
1. 武汉肺炎病毒的时间生物信息学分析
2. R0是什么