转发自http://crickcollege.com/news/220.html
上一篇小编跟大伙儿聊了几种主要的质谱仪的原理及特点,错过的小伙伴请戳:
听课笔记之蛋白质谱的原理及使用(一)
接着上次的听课内容,今天我们来了解一下如何对一台质谱仪的性能进行评估,另外,小编还会分享一下串联质谱是如何工作的。
授课老师
这次课程的授课老师是来自中国农业大学生物学院的李溱老师。李老师于1999年本科毕业于北京师范大学,2007年于美国德克萨斯州Texas A&M大学获得博士学位,2008年-2009年在University of Illinois at Urbana-Champaign从事博士后研究。于2011年加入中国农业大学生物学院,任副教授,在植物生理学与生物化学国家重点实验室及中国农业大学“985”功能基因组中心生物质谱实验室工作,负责生物质谱实验室日常运行,对外提供蛋白质组学和代谢组学技术服务,并开展基于高分辨质谱技术的植物代谢组学和蛋白质组学研究工作。李老师对各种质谱仪器的原理、特点及运行维护有着非常丰富的理论积累和实践经验,很有幸能邀请到他为我们介绍蛋白质谱的原理和操作。
(文中所有图片均来自李溱老师的讲义,并获得发表授权。)
质谱仪性能参数
我们作为质谱仪的使用者,怎么来评估一台质谱仪的性能呢?或者说,我们如何选择质谱仪呢?质谱仪主要的性能参数如下图,就让小编来依次为大伙儿解释一下这些高大上的参数名称到底是啥意思吧。
检测限
“官方”的定义是,与三倍噪音相当的物质的量,我们可以理解为这是质谱仪能够检测到的最低含量化合物的浓度,或者量。比这个值再低的化合物,这台质谱仪就无能为力了。
我怎么知道我的质谱仪的检测限是多少呢?通常,我们会用利血平来作为一个标准的化合物测定质谱仪的检测限。比如,当我们在质谱仪中注入50 fg(飞克)利血平,如果我们获得的信噪比能达到100-1000,那么可以认为这台质谱仪的检测限是不错的。50 fg(飞克)利血平中大概只包含了几万个利血平分子,也就是说,如果能实现对含有几万个小分子的化合物进行检测,那么这台质谱仪的灵敏度是挺高的了。大家可以认为,灵敏度与检测限评估的是同一种性能。
线性范围
这个性能参数也是挺重要的。它表示在什么样的浓度范围之内,质谱仪检测到的信号与样品浓度之间成线性的关系。说得简单点,就是这个浓度范围内的样品,用这台质谱仪检测是比较合适的,高于或低于这个浓度范围的样品,需要浓缩或者稀释后才能用这台质谱仪检测。
通常情况下,质谱仪的线性范围是在3-6个数量级,也就是1,000 – 1,000,000这个范围之内。大部分质谱仪是在1,000 – 10,000这个范围内。
这个参数之所以重要,是因为当我们分析的样品含量分布非常广的时候,比如有的样品含量只有几十μg/ml,而有的样品含量可以达到几mg/ml。在这个比较宽的浓度范围内,如果质谱仪的线性范围非常好,我们不需要浓缩低浓度的样品,也不需要稀释高浓度的样品,可以直接进样,这样可以大大减少样品前处理的复杂程度,很好地节省时间,节省实验步骤。
分辨率和质量准确度
这是两个非常重要的参数,我们常说的高分辨质谱,指的就是分辨率特别高,且质量准确度特别高。这两个参数怎么理解呢?我们先来看看下面这个图:
分辨率
就是质谱仪可以分辨的最近两个质谱峰的质量差值。
这是啥意思呢?假设我有两个强度相同的质谱峰,当这两个峰很靠近的时候,我在什么情况下可以明确地判断出这是两个峰,而不是一个呢?基本准则就是,这两峰的重叠部分的高度,不超过任何一个质谱峰峰高10%的时候,我们认为这是两个可分离的峰。反之,如果这两个峰重叠的部分超过10%,就认为是不可分离的,也就是说,在处理质谱图时,是没办法按照两个峰值来处理的。
当两个峰实现10%基线分离时,我们来测定任何一个质谱峰的半峰宽(就是峰高一半处的峰宽),然后用任何一个峰的质荷比除以半峰宽,就可以得到分辨率。目前来讲,高分辨质谱仪的分辨率可以达到50,000-100,000的数量级,一般的四级杆可以达到5,000-10,000。
那么,高分辨质谱的优点如何体现呢?以上面的右图为例,当我们用低分辨质谱仪检测某种物质时,只能得到最外面蓝色的一个质谱峰,当我们不断提高分辨率,会慢慢发现,这一个质谱峰里面,其实包含了若干小的质谱峰,高分辨质谱仪得到的质荷比与低分辨获得的质荷比是有非常明显的差异。这对化合物鉴定来讲,是很重要的信息。如果我们把质荷比都算错了,我们是很难鉴定到正确的蛋白的。
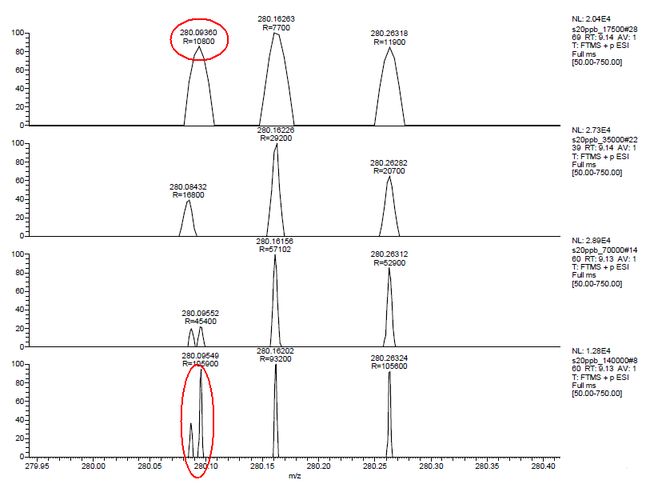
下面这个图也能很直观地告诉我们质谱检测高分辨率的优势。
比如说,我们用17,500的分辨率来对一个化合物进行扫描,会发现在质荷比在280.09的这个位置,有一个非常胖的质谱峰(第一张谱图红色圆圈标记),我们可能会认为这是一个化合物,于是就开始对这个化合物进行鉴定。可是,当我们不断提高质谱仪的分辨率,到一定程度时,我们会发现,这其实是两个不同的峰(第四张谱图红色圆圈标记)。
也就是说,用低分辨率质谱里得到的质荷比来鉴定化合物,得到的信息其实是不完全的(不一定是错的),而通过高分辨质谱,我们就能获得更全面的化合物信息,帮助我们做出正确的判断。
质量准确度
是指质谱仪测到的质荷比与它实际的质荷比的差值,除以它真实的质荷比与1,000,000的乘积。所以它是以ppm为单位的(百万分之一),这个数值看起来更方便。目前高分辨质谱仪质量准确度在2-5个ppm的范围之内。
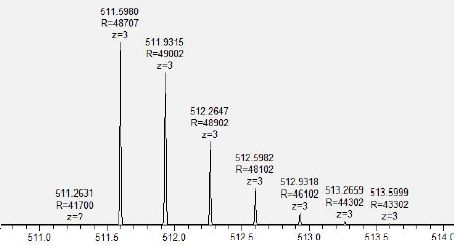
那么,我们怎么来测定一个质谱仪的实际分辨率及质量准确性呢?以李溱老师的一个实验数据为例:
比如,我们选质荷比是511.6这个峰,计算出它的半峰宽为0.012,于是它的分辨率就是511.6除以0.012,得到的值为42,500,而软件给出的分辨率是48,700,是很接近的。
同样的例子,我们来计算质量准确性。测到的质荷比是511.5978,而这个峰实际的质荷比是511.5995,于是计算出质量偏差为3.3ppm,也就是说此次实验的误差就是3.3ppm,这么一个质量偏差范围通常是可以接受的。
分辨率的重要性可能大伙儿容易理解,那质量准确性的高低到底对化合物鉴定会有怎样的影响呢?我们还是以利血平为例。
利血平分子,在质谱图中的609.28066处会有一个质谱峰。当我们用单四级杆来分析利血平的时候,单四级杆的质量准确性大约是在0.1个质量单位(165ppm)。也就是说,当把利血平注入一个四级杆质谱中,四级杆质谱会告诉我们,这个化合物的质荷比大概是在609.2-609.4这个范围之内。
那么问题就来了!在609.2-609.4范围内,我们用C、H、O和N四种元素可以组合出多少种在化学上可以存在的化合物呢?答案是:209种!也就是说,我们要判断这个化合物是不是利血平,得出正确结果的可能性只有1/209!
当我们将质量准确性不断提高,可以组合出来的可能的化合物就会越来越少。当质量准确性达到3 ppm的时候,只有4种可能的化合物。当达到2 ppm的时候,得到的可能的化合物就只剩下2种了。这时候我们再来判断化合物是不是利血平,那么准确性就会高很多很多。这就是为什么高分辨质谱仪对于化合物鉴定来说非常重要,它可以大大减少候选化合物的数量,提高鉴定的成功率。
可以这么说,分辨率与质量偏差分别评估了质谱仪的精密度与准确性。就像我们打靶,比如我每次都能打到右上角一个点上,说明打靶的精密度非常高,但如果我的目标是靶心,那说明准确性却比较差。另一种情况,比如我打靶很多次,打中的点很分散,东一枪西一枪,但平均起来的位置刚好在靶心上,可以认为质量准确性还可以,但精密度比较差。所以我们希望的是,质谱仪的精密度和准确性都非常高。
目前我们能用到的高分辨质谱仪,不管是QTOF或者Orbitrap系列,都可以达到50,000以上的分辨率,同时也可以达到2-3ppm的质量准确性。所以说,如今做蛋白质组学研究的童鞋们,比起以前,真是幸福了很多!
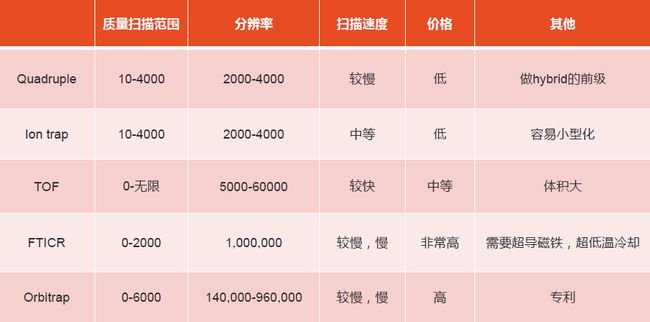
前面给大伙儿分享了评估质谱仪的几个重要参数。那接下来我们就针对不同质谱的性能做一个粗略的总结。
1、 四级杆和离子阱:它们的质量扫描范围是有限的,通常情况下是在10-4,000。超过4,000,四级杆和离子阱就只能作为离子传输用,而不能用于离子检测了。它们的分辨率通常是2,000-4,000,好一点的离子阱可以达到10,000-20,000。扫描速度都不是很快,它们的优势是价格非常低,而且整个仪器可以做得非常小。
2、 TOF:它最大的优势是可以测量的质量范围理论上可以无限大和无限小。如果待检测的离子没有质量,那么它的飞行时间将是0,于是可以测到质荷比是0的离子。同理,如果离子的质量是无限大的,那么它的飞行时间也是无限长的,理论上也是可以检测的。TOF的分辨率是5,000-60,000,扫描速度非常快,它的缺点是,TOF需要一个非常长的离子跑道,所以仪器的体积会很大。
3、 FTICR:优势是分辨率非常高,可以达到1,000,000甚至更高,缺点是扫描速度比较慢,而且它需要一个超导磁铁,运行费用非常高,而且FTICR质谱仪本身的价格也很高,通常都在100万美元以上。
4、 Orbitrap:克服了FTICR必须要使用超导磁铁的缺点,它的分辨率可以达到100,000到1,000,000万,扫描速度不是很快,价格比FTICR要低一些。它受专利保护,目前只有Thermo公司可以生产。
对于蛋白质组学研究来讲,我们对质谱仪器性能的最低要求是:分辨率至少在40,000-50,000,质量准确性应该优于5ppm,质量扫描范围应该在100-3,000,扫描速度是每秒至少获得一张高分辨的一级谱图和十张高分辨的二级谱图。达到以上条件的话,就算是满足了我们做蛋白质组学最基本的要求。
串联质谱
上面讲到各种质谱仪的优缺点,那么我们这里引入串联质谱的概念:将相同或者不同的质谱仪串联起来,实现串联或者并联工作。这样做的目的有两个:产生二级碎片离子(为什么要产生二级碎片离子我们后来会讲),以及实现不同质谱仪性能的优势互补。
我们知道,不同的质谱仪性能是不同的。比如说,四级杆质谱可以实现离子选择,但它的分辨率比较差,而TOF不能实现离子的选择,但分辨率比较高。那么我们能不能把不同性能的质谱仪串到一起,让它们协同工作呢?我们通常会利用串联质谱或者MS-MS来实现这个需求。它们的结合方式有很多种:
第一种:三重四级杆(Triple Quadrupole),或者串联四级杆,就是把三个四级杆串联起来,这样做的主要目的是为了实现二级质谱的扫描。
第二种:四级杆和飞行时间质谱仪串联到一起,就是我们经常听到的Q-TOF,它实际上是为了提高二级质谱的分辨率。
第三种:Orbitrap与四级杆组合,比如Orbitrap Fusion,或者Orbitrap与离子阱组合到一起,比如说Orbitrap Elite等,就是这样的组合。
首先,我们聊一聊怎么通过串联质谱仪获得二级碎片离子。
上面是一个串联四级杆结构的示意图。串联四级杆,或者叫三重四级杆,它是由三个四级杆串联起来。通常,第二个四级杆是由六级杆或八级杆来代替,但我们还是叫它四级杆。这个四级杆不是一个质量选择系统,而是一个collision cell,即碰撞池,用来碎裂离子。
当串联四级杆工作的时候,第一个四级杆是开启了质量选择的模式,它让特定质荷比的离子穿过质谱仪,而把其它的离子都甩掉(甩到四级杆上,或者甩到四级杆的空间当中去)。然后,当特定的离子被选择好后(称为母离子),会进入碰撞池。
在碰撞池里有这样一个结构,就是入口和出口存在电压差,通常入口电压会高于出口电压,当母离子进来以后,通过电压差的作用,就会被加速。而且碰撞池里会充上氦气或氮气,当离子被加速以后,它就会与碰撞池里的氦气或氮气分子发生碰撞、碎裂,形成一些碎片,叫做fragment ions,也就是碎片离子,或者子离子。这些碎片离子会进到第三个四级杆中,进行二级的扫描,得到二级质谱图。
下图就是一个串联四级杆质谱仪,我们可以看到,它仍然是一个非常紧凑的结构。
三重四级杆
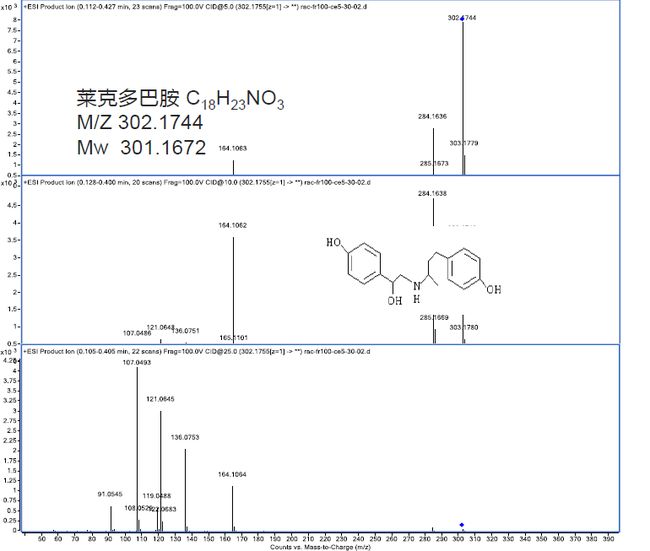
我们以莱克多巴胺为例,来看看它的分子通过串联质谱仪,会发生哪些变化,得到怎样的谱图。
莱克多巴胺这是一种兽药。它的分子量是301.1672,结构式见上图。第一张图,测出来的质荷比为302.1744,这是一个一级质谱的扫描图,在302.1744处有一个莱克多巴胺的质谱峰。
然后呢,我们告诉质谱仪,把302.1744处的这个离子挑出来,将CID(碰撞诱导解离)电压设为10伏,即在碰撞池的入口与出口处增加一个10V的电压差,让离子以10V的碰撞能来进行碰撞。碰撞以后,在第二张图里,我们看到302处的信号强度变弱了,同时284和164的信号强度变强了,原来没有看到的107、121、136信号也出现了。
接下来,我们把碰撞电压从10V增加到25V,增加以后我们会发现,302处的信号完全消失了,表明原来在第一个四级杆中被选择出来的这个离子,经过高能量的碰撞后,完全碎裂了,碎成了91、107、121、136和164这样一些碎片离子。那么这些碎片离子都是什么呢?
我们通过分析结构会发现,它们分别对应着莱克多巴胺的不同的碎片结构,比如164其实对应着莱克多巴胺右端的局部,136对应的是左半部分,等等。
通过分析碎片的化学结构,我们就可以把它们拼装起来,拼成一个完整的莱克多巴胺分子。这就是我们如何通过二级质谱图,来实现对化合物的结构鉴定。而实际的鉴定过程常常会更复杂更伤脑筋一些,上面只是一个简单的示例。
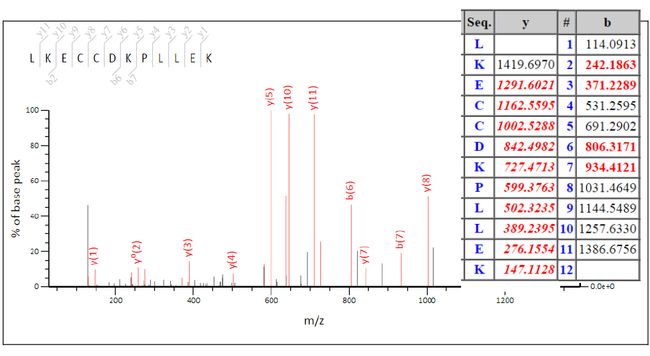
那么对于多肽,或者说对于蛋白酶解后的多肽片段来说,我们可以通过同样的过程,通过分析一个多肽理论上可以得到哪些碎片,然后与谱图进行对比,就可以实现对多肽序列的鉴定。这部分后面会详细再讲。我们先来看个简单的例子,如下图:
比如说我们有左上角这样一个肽段,理论上可以得到灰色标记出的各种b-y离子,通过分析质谱图,可以从中找到对应的碎片离子(右边表格里红色标记的都是可以从质谱图中找到的碎片离子),通过将这些信息拼装起来,我们就可以知道多肽的序列是什么。
上面通过以三重四级杆为例,跟大伙儿分享了串联质谱仪是如何获取二级碎片离子及二级谱图的。那么,其它一些串联质谱仪也是类似的过程。
Q-TOF
Q-TOF与串联四级杆其实是非常像的,只不过它把第三个四级杆换成了一个飞行时间质谱仪。也就是说,一个四级杆,接一个碰撞池,然后接一个飞行时间质谱仪。为了增加飞行的距离,我们会让离子拐个弯再飞回来,这种叫反射模式飞行,让离子在更短的空间内可以飞得更远一些。
下面这个图就是一个Q-TOF质谱仪,是Bruker生产的。它的飞行时间管(flight tube)的长度可以达到3.6米,离子飞一个来回是7.2米。这个数字大伙儿可以留意一下,后面在讲真空度的时候,还会再次提到。
Orbitrap系列
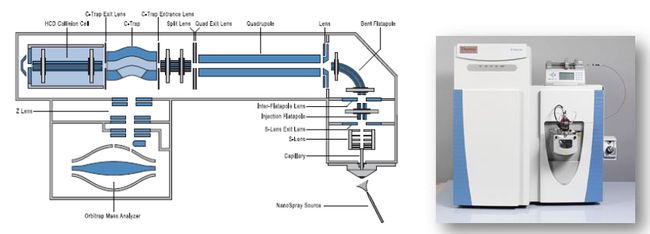
Orbitrap系列比一般的串联质谱仪要复杂一些,大伙儿可以通过下面这个示意图感受一下。
这个系列有好几种串联质谱仪,比如Q Exactive质谱仪,它的Q1也是一个四级杆,Q2是碰撞池,Q3是被一个Orbitrap所取代。
再比如Orbitrap Elite,它的Q1是一个离子阱,Q2是一个碰撞池,Q3为一个Orbitrap,也就是说,Orbitrap Elite里面是没有四级杆的,它用一个离子阱代替了四级杆。
还有一款是Orbitrap Fusion(见下图),它是三种质谱仪混在一些的组合,它的第一级是四级杆,第二级是一个离子阱,第三级是一个Orbitrap,同时它还有一个碰撞池,整体是一个非常复杂的结构。它的特点是,Orbitrap与离子阱可以同步进行扫描。
一般的质谱仪里,两个质量检测量是不能同时扫描的,只能是一个作为质量检测的功能,另外一个作为过滤用。而Orbitrap Fusion里的离子阱和Orbitrap是同时可以进行扫描的,也就是说,它是一个并列的结构,而不仅仅是串联的,所以它的扫描速度会更快,性能也更好。Fusion的分辨率可以达到240,000 – 960,000。
上面小编分享了几种常用的质谱仪,那么以Q-TOF为例,我们再来学习一下质谱仪的基本构造。
对于质谱仪来说,最核心的部分就是质量分析器,它包括两个部分,就是前面我们详细介绍的质量过滤器和质量检测器。质谱仪所有其它部分都是为这个核心部分来服务的。
除了这个核心的组件以外,质谱仪还需要以下几个部分辅助:
质谱辅助系统
真空系统:为什么需要有真空系统呢?我们知道,质谱仪是一台检测气态离子质荷比的仪器,当一个气态离子在空气中飞行时,它会与空气分子发生碰撞,它带的电荷可能就会被撞没了,而成为一个不带电荷的气态分子,那么质谱仪就无法再测量它的质荷比了。所以我们希望得到的这个气态离子能够在质谱仪中稳定存在,所以质谱仪需要一个真空系统,让离子可以稳定地飞行,不受其它空气分子的干扰。
真空系统通常需要有两级,一级是低真空,由机械泵或油泵来提供,它可以大概1-3个mbar,也就是千分之一个大气压的压力环境,低真空的目的是为了给高真空提供一个后备压力环境。高真空是用涡轮泵来提供的,它的真空程度是-1E-5~-1E-10 mbar,在这样一个真空环境里,空气分子基本上都被抽干净了。
可能你想问,为什么要求这个数量级的真空条件呢?
我们先引出一个概念,叫离子的平均自由程(mean free path),它的意思是,一个离子在一个真空环境中飞行多长的距离会碰到下一个空气分子。这就决定了离子在真空中可以稳定存在多久。
以串联四级杆为例,串联四级杆质谱仪大概有1米长左右,所以我们希望离子在飞行1米的过程中,不要碰到其它的空气分子。那么对于串联四级杆来讲,只要维持的真空度能保证1米距离内不会碰到空气分子就可以了。所以串联四级杆通常只需要-1E5 mbar的真空度。
而对于Q-TOF来说,离子的飞行距离大概是在5-7米(大伙儿还记得吗?前面介绍Q-TOF时专门提到了7米这个飞行距离),比串联四级杆的飞行距离长了将近一个数据级,所以Q-TOF质谱仪要求的真空度大约在-1E-6 ~ -1E-7 mbar,才能保证离子在飞行这么长的过程中,不会碰撞到其它空气分子。
而对于Orbitrap质谱仪,离子在里面飞行的时间可以达到1秒钟,会飞行非常远的距离,所以Orbitrap要求-1E-10 mbar这样的真空度。
离子源系统:我们需要把样品从外界大气压的非电离环境中导入质谱仪,变成一个气态的离子,所以需要一个离子源来实现这个功能。
计算机系统:实现质谱仪的控制和数据的采集。
气体系统:气体供应和废气处理(氮气、氩气)
电力供应:UPS不间断电源系统
加上核心组件质量分析器,以上就是组成质谱仪的六大系统。后面我们还会讨论每一部分的结构、使用以及维护。
安装好这六大组件的质谱仪可以用下面的示意图来表示。通常情况下,质量分析器和高真空的涡轮泵都会装在一个大盒子里,这个模块叫主机,而低真空泵(油泵)会放在主机的外面,因为这部分会产生很多的震动、噪音和热量,需要分开放置,从而防止震动对质谱仪产生的影响。质谱仪前面会有一个离子源,侧面会有一个废气口,质谱仪和泵产生的废气,通过这个排气管排到室外。尤其是泵产生的废气,通常是致癌的,所以排气尤其重要。
今天小编分享了课程中学习到的如何评估质谱仪的性能、串联质谱仪的工作原理,以及组成质谱仪的六大组件,大伙儿是否都清楚了呢?如果有什么问题,请给我们留言吧。下一篇小编将会聊聊液相色谱仪的构成,以及液质联用设备的工作原理