- GenVisR 基因组数据可视化实战(三)
11的雾
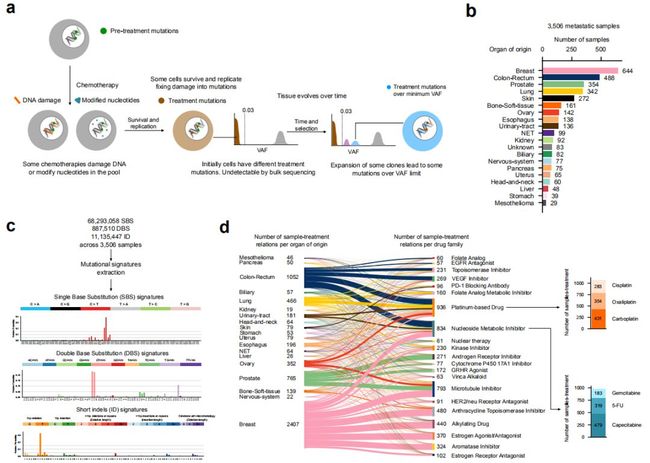
3.genCov画每个突变位点附件的coverage,跟igv有点相似。这个操作起来很复杂,但是图还是挺有用的。可以考虑。由于我的referencegenomebuild是hg38BiocManager::install(c("TxDb.Hsapiens.UCSC.hg38.knownGene","BSgenome.Hsapiens.UCSC.hg38"))library(TxDb.Hsapien
- 李克富 | 咨询师推荐阅读书目
李克富
最重要的书籍不是别人的推荐,而是自己学过的教材,不论当初使用的是哪个版本,它都是我们专业的底层代码,具有不可替代性。前不久,中国心理咨询师筹委会的一位老师邀请我罗列一个推荐书目清单作为咨询师工具包的内容,并要求“说明一下简单的分类或者作三言两语的说明”。斟酌后,我觉得自己推荐的书目大体可以分为普及类书籍、心理学书籍和心理咨询与治疗专业书籍,第三类又分为适合于咨询师新手的和有经验咨询师的。经过严格筛
- 儿童沙盘游戏为什么治疗有效?
静待花开_602f
图片发自App运华日记第197篇(2018.4.15)儿童沙盘游戏为什么治疗有效?首先是孩子们喜欢。其次它做为一种“语言”表现孩子们“问题”,通过沙具可以和孩子起到交流与沟通的作用。人最怕的被迫生活学习,那么在沙盘中,一切都由孩子们自由创造,发挥孩子们自己的主观能动性。他们可以任意摆放自己喜欢的沙具,呈现着他们的情绪与心理,表达着他们所遇到问题以及应付问题的方式。而治疗师为儿童提供一个助于他们通过
- 抑郁症
汝汝吾吾
我是一个一事无成的废物,厌倦活着感觉一切都是无意义的,和家里的关系也不好,朋友很多但真的了解我的基本没有,出门都是带着一个傻子的面具,回到家摘下面具才发现自己一无所有,我还特地去看了医生说是抑郁症,我当时感觉不可能身边的人也觉得不可能,我一直在配合治疗,只不过医生不知道我一直在圆一个天大的谎言,一步错步步错,可能我这个人命大吃安眠药吃了很多,都没用,跳楼怕疼割腕怕自己没胆量,一切都不敢做,好在我在
- 《拖延心理学》(一)你为什么会拖延?|木盒笔记
纯se蓝调
《拖延心理学》是帮助你向拖延症宣战的一本书,作者简·博克和莱诺拉·袁是全球知名的拖延症治疗专家。大概每个人或多或少总会有一点拖延症的行为。比如明天要叫论文了,今天你还没有写好,你一边在焦虑症怎么办,一边又拿着手机漫无目的的刷新闻;比如你想了很久准备减肥,但是迟迟又没有行动,想着今天晚上少吃一点吧、明天我就开始运动。今天分析的笔记来告诉你“你为什么会拖延?”,解读人杨坚。有人说拖延就像巨大的泥沼,让
- 【杨爽微习惯日更41/101】
杨爽_e105
沟通小课堂---治疗“愤世嫉俗”的最佳良方是什么?12月28日,钢琴家傅聪因感染新冠肺炎在英国去世了,傅聪先生被世人广泛熟知,除了他是优秀的钢琴家,更因为他是《傅雷家书》中享受父母深深关爱殷殷教诲的青年,这本书影响了一代又一代人。今天想和你分享傅雷先生时常会在家书中强调的,要坚持“大我”,抛弃“小我”,不要对个人的名利得失太过计较。当我们热衷于个人名利,而又得不到名利的时候,必然会因为嫉妒和仇恨变
- 第九章 肿瘤放射治疗
晨翕
放射物理学:主要研究各种放射源的性能特点、治疗剂量学、质量控制、质量保证及辐射防护等放射生物学:主要研究机体正常组织和肿瘤组织对射线对反应及如何人为地改变这些反应对质和量。放射技术学:主要研究具体运用各种放射源及设备治疗肿瘤患者,包括射野设置、体位固定、定位、摆位操作等技术实施。临床放射肿瘤学:在临床肿瘤学的基础上,研究肿瘤放射治疗的适应证,根据病理、分期、预后确定治疗策略,综合运用放射物理、放射
- Post teen
达米安曾
提起绵阳这个城市,你会想起什么?可能是那碗味道淡得让人骂娘的绵阳米线,这种把粉扔碗里拿热汤一冲就给你端上来的敷衍食物如今会在某个无聊的夜晚缓慢地折磨你的味蕾。可能是凯德广场的扶梯,去隔壁沃尔玛买几瓶劣质黑啤后慢悠悠地站在扶梯上打量上上下下的人,情侣家人老人年轻人女人男人,他们是一本本或者无聊或者生动的小说。可能是学校的情人坡,其实情人坡没有多少情人,大三的时候学校放弃治疗没再打理这个地方,杂草长得
- 平凡日记|壬寅虎年,继续康复治疗第31天
杨涛看评
2月7日,正月初七,阴,冷,早上小雨。早上起来的有点晚,护士就开始查房了才醒过来,确实太冷了,不想起床。最让人欣慰的是,主管护士看我房间没有空调,又一个薄被子,主动给我加了一床被子,感动至极,天下还是有好人。后来主管医生也来房间查房了,交流了一下,感觉“前途”一片光明,一起努力。昨天写了今天可以做手法治疗,早上去做手法的时候,医生说假期手肘状态还保持的可以,继续加油,是一个好的苗头,努力吧,争取早
- 尹吭【谦虚组】精进打卡2018.06.12
老黑1983
内容:【日精进打卡第171天】【知~学习】《六项精进》2遍共330遍《大学》2遍共346遍••••••【经典名句分享】人不知而不愠不亦君子乎【行~实践】一、修身:(对自己个人)俯卧撑20个五组修身:(利他:告知中医的一些治疗项目)修身:(帮扶:帮扶对象离职)二、齐家:(对家庭和家人)1、送女儿上学三、建功:(对工作)1、湿疹和疣案例页调整{积善}:发愿从2017年12月25日起1年内365善事。今
- 小儿咳嗽治疗
毋梦
家有小女,4岁,前段时间穿了一不透气的衣服跳床,出来后吹了阵风,当晚就嗓子哑了,第二天带她去古镇玩,嗓子哑加重,于是买了一杯暖和和的冰糖雪梨粥,想润润嗓子,没有大的效果。观察她的舌苔,有些白,稍有点腻,再加上没有大便,前一天吃得有点多,想起家里还有午时茶颗粒,给吃了些。无效,且开始发烧,38度以上,睡着时喉咙不干净,有呼哧呼哧的声音,而且开始咳嗽,有点像小儿喉炎的症状,因为之前得过,知道这个疾病的
- 2023-10-16呼建荣,中原焦点团队,网络中级第33期,坚持分享734天
呼建荣
筑基课团体心理咨询技能第一讲。团体辅导、咨询、治疗的异同。1.相同:工作原理、技术、方法相似,都认为人的困惑与障碍是人与外部环境的关系出了问题,都认为可以通过团体中人际互动来解决。2.区别:①团体辅导,起源于学校,有主题,重在信息和知识的传递。人数一般在25至45人。②团体咨询,针对心理咨询,少则三五人,多则十几人到几十人。更关心团体之间的互动。重视团体动力和问题解决。③团体治疗起源于医院,6-1
- 治疗失眠的食疗法
和友育儿
科学的食疗方法,不但有效对抗失眠,且无副作用,安全可靠。小米粥食材:莲子,桂圆,百合,小米;做法:将以上几种食材混合煮粥。功效:缓解习惯性失眠。2.莲藕食材:莲藕;做法:可食用藕粉,或以莲藕加蜂蜜煮熟食用;功效:适用于因身体虚弱而失眠者。3.猪心药膳食材:猪心,党参,当归;做法:将党参,当归2味中药,装入切开的猪心,炖后,食肉饮汤;功效:对多汗,心悸而睡眠不佳者有较好作用。4.芭蕉根猪肉汤食材:芭
- 【周总结】第六期第7周29叮当
29_叮当
时间:2019.6.24——2019.6.30【本周计划/总结】一、职业发展注会复习备考。计划一天八小时复习。二、财务状况收支正常,还有账未收回,等段时间再催。三、健康每日1万步,7天完成;治疗白发,6天;平板支撑最近没坚持;每天锻炼完后拉伸,疏通经络;体重下降。图片发自App四、娱乐没什么娱乐活动。五、朋友与重要他人哥哥和侄子都回来了,家人团聚,老人很开心。一家人难得相聚六、家庭做好每周的清洁,
- 用内心励志故事传递力量!扫雷英雄战士杜富国播音员上线啦。
斧惜山人
杜富国在执行扫雷任务时,失去了手和眼睛,但他没有自暴自弃,他还有梦想,要用嘴去,用声音,用故事传递正能量。他经过康复治疗,坚持练习吐字发声,成为了一名播音员。“播音员杜富国”系列节目上线啦。用声音传递力量!把扫雷故事讲给更多的人听,让更多的人了解扫雷战士。杜家四兄妹,在哥哥杜富国的垂范表率下,演绎着什么是家国大义,什么叫“大疫当前有大义,小家当中有大爱”。妹妹杜富佳作为护士,两次请战前往抗疫前线,
- 杏子
玩玉玩心情
文心儿时的杏树长在屋后一颗苦核杏一颗甜核杏一颗苦核杏记忆深处的杏子是那颗甜核杏奶奶说这是她种的杏树很久了麦黄六月瓜也被车子从县城拉到了农村杀开一个瓜一家人都可以尝到对于瓜没有太多记忆依稀记得拿锯条打磨的小刃刀杀瓜利器同样也在唇上留下了印记那颗甜核杏枝丫超过了屋檐小小的我们站在院中央等待着半红半黄的掉落奶奶用推耙摇晃着树枝我们几个在院子里撑开衣服捡拾一个又一个的塞进小小的口袋一捡就是一天一捡就是一个
- 淋巴结肿大会导致癌症吗?引起淋巴结肿大的原因,早知道早预防
20a6fc3e70ac
作为医生,在接诊过程中我经常会碰见这样的患者,体检中发现淋巴结肿大或者是感冒发热,在消炎治疗的过程中突然发现颈部两侧淋巴结肿大,以至于会变得越来越大。淋巴结是人体重要的免疫器官之一,但是淋巴结肿大是一种非常常见的疾病,淋巴结的肿大分为局部淋巴结肿大和全身淋巴结肿大,意义各不一样,一般局部淋巴结肿大都代表局部有炎症或者非特异性淋巴结炎,以及有癌转移等疾病。如果是两个区域以上淋巴结肿大就称为全身淋巴结
- 2022-11-23
聊癫痫
什么方式治疗癫痫病好?医生介绍,对于癫痫这种疾病的话,我们是不必过于害怕的,因为这种疾病虽然是难以治疗的,但是这种疾病仍然是可以治疗好的。患有癫痫病的话,我们就要对癫痫病的治疗方式做一个了解。这样的话不仅可以帮助我们在治疗癫痫病的时候根据病情选择方式,而且还可以对癫痫治疗方式的一些差异有个了解。很多治疗癫痫的方式效果都是不错的,但是具体治疗癫痫病的方式有哪些呢?目前最常见的治疗方法有药物治疗,手术
- 当野鸡“心理学”变成赚钱的工具
Z小姐不吐不快
今日乘车闲来无事便听起了电台(可在网易云音乐搜索「报刊选读」,点击20180212那一期),听罢,不禁感叹,怪不得「洗稿惯犯」周冲说,“与其教育傻逼,不如赚傻逼点钱。”哎,如果我没啥良心,估计也能赚这钱了。▲图片摘自六神磊磊读金庸《今儿就从头彻底扒一下周冲,看是什么成色》头痛、脚痛,不管是哪里痛,家排疗法总会告诉你,身体的每一处疼痛都喻示着你的“心事”影响身体健康,只要找出病因,无论疼痛还是癌症都
- 第一次尝试魔幻现实主义。
海子典当记
经历过朝生暮死的痛苦,才会懂存在的意义。许多年后,于雪夜的街头,我见过一位步履蹒跚的老人,他的头颅满被白丝缠绕,雪飘落在他的发梢便瞬间消失,他的目光浑浊,似是看遍了人间每个无光的角落。他的额头尽是皱纹,眨一下眼,眉毛便堆聚在了一起。岁月在他脸上狠狠的留下印记,我猜他一定从未使用过镜子,不然他一定也惊讶于造物主的神力--将一生的故事写在脸上。他自称"达摩流浪者”。我继续看他。他披着一件长款古铜色风衣
- 《中国特殊教育》
专注知识产权服务13937636601
职称评审知网期刊核心期刊核心期刊职称评审
刊物名称《中国特殊教育》刊号国内CN11-3826/G4国际ISSN1007-3728投稿须知1.征稿范围及各类稿件的要求特殊教育与心理学研究各领域的实证研究、综述、教学改革研究等,具体研究领域包括全纳教育、特殊教育理论、听力障碍、视力障碍、智力障碍、学习障碍、自闭症、情绪与行为障碍、康复与治疗、超常儿童教育、特殊群体教育(留守儿童、流动儿童、孤儿、小团伙、网络成瘾儿童、工读学生)等1.1实证类稿
- 十款青少年钙片产品排行榜 学生生长发育钙片推荐
优惠券高省
第一名:钙尔奇钙尔奇,首个进入中国的国际知名钙补充剂品牌,被众多中国医学专家和营养学专家推荐用于预防和治疗骨质疏松症,也是全球医生推荐比较多的钙制剂品牌。钙尔奇,国际知名钙补充剂品牌。来自于辉瑞中国健康药物部,前身为惠氏中国健康药物部,成立于1991年。辉瑞公司创建于1849年,是世界领先的以研发为基础的生物医学和制药公司。目前,分布于90个国家的大约80,000名辉瑞员工,致力于为全球带来更多健
- 癌症来了,她走了。
倾城小酒馆
作者:倾城小酒馆1清晨时分,带着一丝温暖的阳光悄悄地洒进了屋内,打开窗户,有些清凉的微风吹在身上,随手煮上一壶新鲜的茉莉花茶,淡淡的茉莉香气瞬间布满了整个屋子。蒋晓华和女友陈云锦相恋至今已经将近五年了,两人从青葱的学生年代走到了现在,恋情一直很稳定,最近已经在筹备婚礼,打算携手走进婚姻的殿堂。婚房选在昆城新城区最大的小区里,两房一厅,面积虽然不算大,但总算是有真正属于自己的小窝了。购房、采购、装修
- 2023-01-13
成长_3a8a
2023年1月13日中原焦点团队刘永利分享1201天。中原焦点团队第6期读书打卡第52天:今天阅读《最想说的话被自己听见》——叙事实践的15堂课。叙事治疗最核心的概念就是一个人之所以会受困,常不是因为这个人有问题,而是他活在充满问题的故事版本里,所以助人者最重要的工作就是陪着当事人找出与问题故事不同的新版本,要跳出旧有的问题故事框架,发展出新的故事版本,靠的就是一种不同于问题版本的视野,这样的视野
- 每天按摩或艾灸三个穴位,解决失眠问题
健康育儿心理
失眠常表现为:睡眠时间不足,睡眠不深,在睡眠中易惊醒,醒后入睡困难,严重的甚至出现彻夜不眠。长期失眠会导致疲劳感、不安、全身不适、无精打采、反应迟缓、头痛、注意力不能集中,严重者对人的精神状态会造成恶劣的影响。艾灸对于治疗失眠见效快,养心安神效果非常好。一是神门穴:在小指侧的腕横纹处可门六摸到一条筋,神门穴就在这条筋外侧的处左右各有凹陷穴。【施灸方法】神门穴可以自行施负,施负时取坐姿,一手执点燃的
- 《也许你该找个人聊聊》读书记录(第二部分19)
古灵精怪
19、当我们做梦这不仅是一个梦境中常见的主题,而且在心理治疗中也是再常见不过的主题了——那就是”排斥“。我们都会害怕被冷落、被忽视、被回避,最后变得丧失去爱的能力而孤独一生。——害怕孤独一生,但又好像无法躲避孤独,只是这种孤独伴随着热闹和温暖,没有绝对的孤独,只有孤独感~我们害怕受伤。我们害怕被羞辱。我们害怕失败,也害怕成功。我们害怕孤单,也害怕牵绊。我们害怕倾听内心的诉说。我们害怕不快乐,又害怕
- 读书笔记《焦虑自救手册》
如雪般飞舞
各位好,今天我们讲一本非常实用的小书,叫作《焦虑自救手册》。昨天我见到一个朋友,他就有焦虑症。他说你们不是讲过两本关于焦虑症的书了吗,而且讲得都很好,为什么还要再讲一本?我说因为大部分读者的焦虑症还没有缓解,只要有读者的焦虑症还没有缓解,我们其实就应该继续地探索这方面的话题。为什么呢?因为这本书的作者告诉我们,对于焦虑的治疗来说,一个非常重要的原理就是不断地重复。就是我们要一而再、再而三的重复,直
- 心情日记(6月16日)
陪你今生来世
早上不是太忙,送了小宝顺便去医院取检查报告。没有拿到结果之前,心里是有那么一点忐忑的。拿到之后,反而镇定了许多。医生再次给我做了检查,说是好多了。报告显示有点病毒感染,需要继续用药治疗一段时间。医生叮嘱其间要多运动,增强免疫力。回来的路上,心里充满了庆幸和感恩。庆幸机缘巧合,让我做到了早发现,早治疗。更庆幸一直以来,自己的良善,感恩之心换来了老天的眷顾,让我总是有惊无险。感恩老天的庇护,感恩国家先
- D83转载转载转载!
雨墨2021
点鼻子请帮手晃动手指,然后用自己的食指点对方的手指。再来回点自己的鼻子,只要都能顺利点到对方的手指,就表示没有问题!如果来回几次都点空,甚至当手指停下不动的时候都无法点中,就一定要去医院检查了!当然这个只是我们自己检测的一个手段,因为有的时候脑梗出现的位置不同,导致的症状也不同,从而自测只能作为参考,如果有很明显的身体症状,可以迅速的去医院,做相关的检查。疾病的预防永远大于治疗,如果你不想脑梗到来
- 《心理治疗师的刻意练习》读后记
海涛心理咨询
读后记:这本书主要是写一位心理咨询师从小白到合格咨询师的刻意练习。开篇写了自己初做心理咨询师的美好体验与尴尬——50%的来访者没有变好(而这居然是行业平均水平);希望自己的咨询水平能够提高而查阅了相关论文,请教了相关专家,开始了刻意练习之路;刻意练习如何降低了自己的焦虑,最终提高了自己的咨询表现,并且要和读者分享自己的成功之路。书中也提供了一些科学研究和统计调查:资深咨询师的来访者反馈与新手咨询师
- 多线程编程之卫生间
周凡杨
java并发卫生间线程厕所
如大家所知,火车上车厢的卫生间很小,每次只能容纳一个人,一个车厢只有一个卫生间,这个卫生间会被多个人同时使用,在实际使用时,当一个人进入卫生间时则会把卫生间锁上,等出来时打开门,下一个人进去把门锁上,如果有一个人在卫生间内部则别人的人发现门是锁的则只能在外面等待。问题分析:首先问题中有两个实体,一个是人,一个是厕所,所以设计程序时就可以设计两个类。人是多数的,厕所只有一个(暂且模拟的是一个车厢)。
- How to Install GUI to Centos Minimal
sunjing
linuxInstallDesktopGUI
http://www.namhuy.net/475/how-to-install-gui-to-centos-minimal.html
I have centos 6.3 minimal running as web server. I’m looking to install gui to my server to vnc to my server. You can insta
- Shell 函数
daizj
shell函数
Shell 函数
linux shell 可以用户定义函数,然后在shell脚本中可以随便调用。
shell中函数的定义格式如下:
[function] funname [()]{
action;
[return int;]
}
说明:
1、可以带function fun() 定义,也可以直接fun() 定义,不带任何参数。
2、参数返回
- Linux服务器新手操作之一
周凡杨
Linux 简单 操作
1.whoami
当一个用户登录Linux系统之后,也许他想知道自己是发哪个用户登录的。
此时可以使用whoami命令。
[ecuser@HA5-DZ05 ~]$ whoami
e
- 浅谈Socket通信(一)
朱辉辉33
socket
在java中ServerSocket用于服务器端,用来监听端口。通过服务器监听,客户端发送请求,双方建立链接后才能通信。当服务器和客户端建立链接后,两边都会产生一个Socket实例,我们可以通过操作Socket来建立通信。
首先我建立一个ServerSocket对象。当然要导入java.net.ServerSocket包
ServerSock
- 关于框架的简单认识
西蜀石兰
框架
入职两个月多,依然是一个不会写代码的小白,每天的工作就是看代码,写wiki。
前端接触CSS、HTML、JS等语言,一直在用的CS模型,自然免不了数据库的链接及使用,真心涉及框架,项目中用到的BootStrap算一个吧,哦,JQuery只能算半个框架吧,我更觉得它是另外一种语言。
后台一直是纯Java代码,涉及的框架是Quzrtz和log4j。
都说学前端的要知道三大框架,目前node.
- You have an error in your SQL syntax; check the manual that corresponds to your
林鹤霄
You have an error in your SQL syntax; check the manual that corresponds to your MySQL server version for the right syntax to use near 'option,changed_ids ) values('0ac91f167f754c8cbac00e9e3dc372
- MySQL5.6的my.ini配置
aigo
mysql
注意:以下配置的服务器硬件是:8核16G内存
[client]
port=3306
[mysql]
default-character-set=utf8
[mysqld]
port=3306
basedir=D:/mysql-5.6.21-win
- mysql 全文模糊查找 便捷解决方案
alxw4616
mysql
mysql 全文模糊查找 便捷解决方案
2013/6/14 by 半仙
[email protected]
目的: 项目需求实现模糊查找.
原则: 查询不能超过 1秒.
问题: 目标表中有超过1千万条记录. 使用like '%str%' 进行模糊查询无法达到性能需求.
解决方案: 使用mysql全文索引.
1.全文索引 : MySQL支持全文索引和搜索功能。MySQL中的全文索
- 自定义数据结构 链表(单项 ,双向,环形)
百合不是茶
单项链表双向链表
链表与动态数组的实现方式差不多, 数组适合快速删除某个元素 链表则可以快速的保存数组并且可以是不连续的
单项链表;数据从第一个指向最后一个
实现代码:
//定义动态链表
clas
- threadLocal实例
bijian1013
javathreadjava多线程threadLocal
实例1:
package com.bijian.thread;
public class MyThread extends Thread {
private static ThreadLocal tl = new ThreadLocal() {
protected synchronized Object initialValue() {
return new Inte
- activemq安全设置—设置admin的用户名和密码
bijian1013
javaactivemq
ActiveMQ使用的是jetty服务器, 打开conf/jetty.xml文件,找到
<bean id="adminSecurityConstraint" class="org.eclipse.jetty.util.security.Constraint">
<p
- 【Java范型一】Java范型详解之范型集合和自定义范型类
bit1129
java
本文详细介绍Java的范型,写一篇关于范型的博客原因有两个,前几天要写个范型方法(返回值根据传入的类型而定),竟然想了半天,最后还是从网上找了个范型方法的写法;再者,前一段时间在看Gson, Gson这个JSON包的精华就在于对范型的优雅简单的处理,看它的源代码就比较迷糊,只其然不知其所以然。所以,还是花点时间系统的整理总结下范型吧。
范型内容
范型集合类
范型类
- 【HBase十二】HFile存储的是一个列族的数据
bit1129
hbase
在HBase中,每个HFile存储的是一个表中一个列族的数据,也就是说,当一个表中有多个列簇时,针对每个列簇插入数据,最后产生的数据是多个HFile,每个对应一个列族,通过如下操作验证
1. 建立一个有两个列族的表
create 'members','colfam1','colfam2'
2. 在members表中的colfam1中插入50*5
- Nginx 官方一个配置实例
ronin47
nginx 配置实例
user www www;
worker_processes 5;
error_log logs/error.log;
pid logs/nginx.pid;
worker_rlimit_nofile 8192;
events {
worker_connections 4096;}
http {
include conf/mim
- java-15.输入一颗二元查找树,将该树转换为它的镜像, 即在转换后的二元查找树中,左子树的结点都大于右子树的结点。 用递归和循环
bylijinnan
java
//use recursion
public static void mirrorHelp1(Node node){
if(node==null)return;
swapChild(node);
mirrorHelp1(node.getLeft());
mirrorHelp1(node.getRight());
}
//use no recursion bu
- 返回null还是empty
bylijinnan
javaapachespring编程
第一个问题,函数是应当返回null还是长度为0的数组(或集合)?
第二个问题,函数输入参数不当时,是异常还是返回null?
先看第一个问题
有两个约定我觉得应当遵守:
1.返回零长度的数组或集合而不是null(详见《Effective Java》)
理由就是,如果返回empty,就可以少了很多not-null判断:
List<Person> list
- [科技与项目]工作流厂商的战略机遇期
comsci
工作流
在新的战略平衡形成之前,这里有一个短暂的战略机遇期,只有大概最短6年,最长14年的时间,这段时间就好像我们森林里面的小动物,在秋天中,必须抓紧一切时间存储坚果一样,否则无法熬过漫长的冬季。。。。
在微软,甲骨文,谷歌,IBM,SONY
- 过度设计-举例
cuityang
过度设计
过度设计,需要更多设计时间和测试成本,如无必要,还是尽量简洁一些好。
未来的事情,比如 访问量,比如数据库的容量,比如是否需要改成分布式 都是无法预料的
再举一个例子,对闰年的判断逻辑:
1、 if($Year%4==0) return True; else return Fasle;
2、if ( ($Year%4==0 &am
- java进阶,《Java性能优化权威指南》试读
darkblue086
java性能优化
记得当年随意读了微软出版社的.NET 2.0应用程序调试,才发现调试器如此强大,应用程序开发调试其实真的简单了很多,不仅仅是因为里面介绍了很多调试器工具的使用,更是因为里面寻找问题并重现问题的思想让我震撼,时隔多年,Java已经如日中天,成为许多大型企业应用的首选,而今天,这本《Java性能优化权威指南》让我再次找到了这种感觉,从不经意的开发过程让我刮目相看,原来性能调优不是简单地看看热点在哪里,
- 网络学习笔记初识OSI七层模型与TCP协议
dcj3sjt126com
学习笔记
协议:在计算机网络中通信各方面所达成的、共同遵守和执行的一系列约定 计算机网络的体系结构:计算机网络的层次结构和各层协议的集合。 两类服务: 面向连接的服务通信双方在通信之前先建立某种状态,并在通信过程中维持这种状态的变化,同时为服务对象预先分配一定的资源。这种服务叫做面向连接的服务。 面向无连接的服务通信双方在通信前后不建立和维持状态,不为服务对象
- mac中用命令行运行mysql
dcj3sjt126com
mysqllinuxmac
参考这篇博客:http://www.cnblogs.com/macro-cheng/archive/2011/10/25/mysql-001.html 感觉workbench不好用(有点先入为主了)。
1,安装mysql
在mysql的官方网站下载 mysql 5.5.23 http://www.mysql.com/downloads/mysql/,根据我的机器的配置情况选择了64
- MongDB查询(1)——基本查询[五]
eksliang
mongodbmongodb 查询mongodb find
MongDB查询
转载请出自出处:http://eksliang.iteye.com/blog/2174452 一、find简介
MongoDB中使用find来进行查询。
API:如下
function ( query , fields , limit , skip, batchSize, options ){.....}
参数含义:
query:查询参数
fie
- base64,加密解密 经融加密,对接
y806839048
经融加密对接
String data0 = new String(Base64.encode(bo.getPaymentResult().getBytes(("GBK"))));
String data1 = new String(Base64.decode(data0.toCharArray()),"GBK");
// 注意编码格式,注意用于加密,解密的要是同
- JavaWeb之JSP概述
ihuning
javaweb
什么是JSP?为什么使用JSP?
JSP表示Java Server Page,即嵌有Java代码的HTML页面。使用JSP是因为在HTML中嵌入Java代码比在Java代码中拼接字符串更容易、更方便和更高效。
JSP起源
在很多动态网页中,绝大部分内容都是固定不变的,只有局部内容需要动态产生和改变。
如果使用Servl
- apple watch 指南
啸笑天
apple
1. 文档
WatchKit Programming Guide(中译在线版 By @CocoaChina) 译文 译者 原文 概览 - 开始为 Apple Watch 进行开发 @星夜暮晨 Overview - Developing for Apple Watch 概览 - 配置 Xcode 项目 - Overview - Configuring Yo
- java经典的基础题目
macroli
java编程
1.列举出 10个JAVA语言的优势 a:免费,开源,跨平台(平台独立性),简单易用,功能完善,面向对象,健壮性,多线程,结构中立,企业应用的成熟平台, 无线应用 2.列举出JAVA中10个面向对象编程的术语 a:包,类,接口,对象,属性,方法,构造器,继承,封装,多态,抽象,范型 3.列举出JAVA中6个比较常用的包 Java.lang;java.util;java.io;java.sql;ja
- 你所不知道神奇的js replace正则表达式
qiaolevip
每天进步一点点学习永无止境纵观千象regex
var v = 'C9CFBAA3CAD0';
console.log(v);
var arr = v.split('');
for (var i = 0; i < arr.length; i ++) {
if (i % 2 == 0) arr[i] = '%' + arr[i];
}
console.log(arr.join(''));
console.log(v.r
- [一起学Hive]之十五-分析Hive表和分区的统计信息(Statistics)
superlxw1234
hivehive分析表hive统计信息hive Statistics
关键字:Hive统计信息、分析Hive表、Hive Statistics
类似于Oracle的分析表,Hive中也提供了分析表和分区的功能,通过自动和手动分析Hive表,将Hive表的一些统计信息存储到元数据中。
表和分区的统计信息主要包括:行数、文件数、原始数据大小、所占存储大小、最后一次操作时间等;
14.1 新表的统计信息
对于一个新创建
- Spring Boot 1.2.5 发布
wiselyman
spring boot
Spring Boot 1.2.5已在7月2日发布,现在可以从spring的maven库和maven中心库下载。
这个版本是一个维护的发布版,主要是一些修复以及将Spring的依赖提升至4.1.7(包含重要的安全修复)。
官方建议所有的Spring Boot用户升级这个版本。
项目首页 | 源