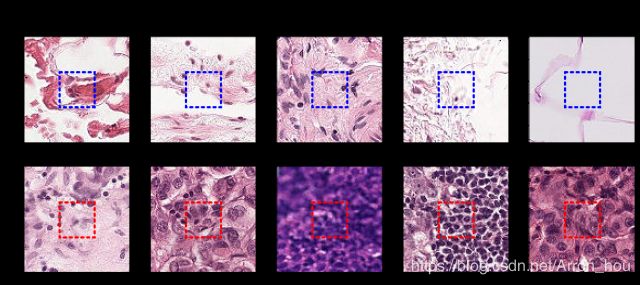
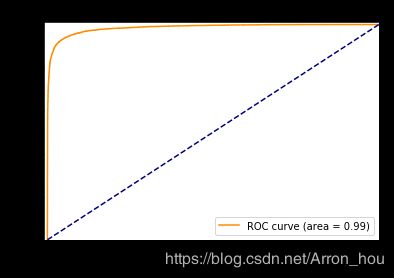
- 在NLP深层语义分析中,深度学习和机器学习的区别与联系
在自然语言处理(NLP)的深层语义分析任务中,深度学习与机器学习的区别和联系主要体现在以下方面:一、核心区别特征提取方式机器学习:依赖人工设计特征(如词频、句法规则、TF-IDF等),需要领域专家对文本进行结构化处理。例如,传统情感分析需人工定义“情感词库”或通过词性标注提取关键成分。深度学习:通过神经网络自动学习多层次特征。例如,BERT等模型可从原始文本中捕获词向量、句法关系甚至篇章级语义,无
- 深度学习--利用梯度下降法进行多变量的二分类(感知机)
白话学生nit
深度学习分类人工智能
其实这一节涉及到了感知机的相关知识,就把这一节当作是学习感知机的引子吧。什么是二分类我们先来说一下什么是二分类,二分类指的是将结果分为两个互斥的类别,通常用来表示问题的两种可能。为什么用感知机学习二分类常见的解决问题的模型有很多,这里我们使用感知机模型。至于为什么,因为感知机模型很多地方用起来比较简便,就拿我们这一节的问题举一下例子,我们需要依照房子的价格对房子进行分类。在感知机模型中,我们可以使
- 智能喷洒机器人目标识别系统:基于NanoDet的目标检测与UI界面实现
YOLO实战营
机器人目标检测uiNanoDet计算机视觉目标跟踪深度学习
在现代农业生产中,自动化喷洒系统是实现精准农业的重要组成部分。智能喷洒机器人通过图像识别和自动控制技术,能够高效识别并精确喷洒农药、肥料等,提高农业生产效率,降低化学品使用量,减少环境污染。目标识别是智能喷洒机器人中至关重要的部分,它涉及到精准的作物和病虫害识别,确保喷洒操作的准确性。在本篇博客中,我们将构建一个基于NanoDet深度学习目标检测模型的智能喷洒机器人目标识别系统。我们将介绍如何使用
- 对标ChatGPT,「文心一言」今日亮相!AI人机时代来临,未来在何方?
AI医学
本文由「AI医学er」提供医海无涯,AI同舟。关注我们,助力高效科研。3月15日,OpenAI公布了其大型语言模型的最新版本——GPT-4。3月16日,百度文心一言人工智能聊天机器人正式上线。一个时代开始了。OpenAI在官网表示,GPT-4是一个能接受图像和文本输入,并输出文本的多模态模型,是OpenAI在扩展深度学习方面的最新成果。此前的ChatGPT,只能通过向其输入文字提问才能生成文字回答
- 【深度学习新浪潮】什么是system 1和system 2?
小米玄戒Andrew
深度学习新浪潮深度学习人工智能大模型推理模型COT模型蒸馏动态推理
在大模型研究中,System1和System2的概念源于心理学家DanielKahneman的双系统理论,用于描述人类思维的两种模式。System1代表快速、直觉、自动化的思维(如模式识别),而System2代表慢速、有意识、需要努力的逻辑推理(如复杂数学计算)。这一理论被引入AI领域后,成为理解大模型能力边界和优化方向的重要框架。一、大模型中的System1与System2的定义System1(
- 学习人工智能开发的详细指南
Ws_
学习人工智能python
一、引言人工智能(AI)开发是一个充满挑战与机遇的领域,它融合了数学、计算机科学、统计学、认知科学等多个学科的知识。随着大数据、云计算和深度学习技术的快速发展,AI已经成为推动社会进步和产业升级的关键力量。本文将为初学者提供一份详细的学习指南,帮助大家逐步掌握AI开发的核心技能。二、基础知识准备数学基础:线性代数:理解向量、矩阵、线性变换等基本概念,掌握矩阵运算和特征值分解等技巧。概率论与统计学:
- AI人工智能领域知识图谱在文本分类中的应用技巧
AI天才研究院
AI大模型企业级应用开发实战人工智能知识图谱分类ai
AI人工智能领域知识图谱在文本分类中的应用技巧关键词:知识图谱、文本分类、图神经网络、实体关系抽取、深度学习、自然语言处理、特征融合摘要:本文深入探讨了知识图谱在文本分类任务中的应用技巧。我们将从知识图谱的基本概念出发,详细分析如何将结构化知识融入传统文本分类流程,介绍最新的图神经网络方法,并通过实际案例展示知识增强型文本分类系统的构建过程。文章特别关注知识表示学习与文本特征的融合策略,以及在不同
- 解读一个大学专业——信号与图像处理
专业定义与核心内容维度内容定义研究如何采集、处理、分析和理解一维信号(语音、雷达、脑电)和二维/三维图像(医学、遥感、工业视觉)。关键词数字信号处理(DSP)、图像处理、计算机视觉、模式识别、压缩感知、深度学习、GPU加速、嵌入式系统。技术栈MATLAB/Python+OpenCV/PyTorch+DSP/FPGA+GPU(CUDA)第五届先进算法与信号、图像处理国际学术会议(AASIP2025)
- Pad Token技术原理与实现指南
Takoony
AI
目录概述理论基础:第一性原理分析技术实现机制工程最佳实践性能优化策略常见问题与解决方案技术发展趋势附录1.概述1.1文档目的本文档旨在深入阐述深度学习中PadToken的技术原理、实现机制及工程应用,为算法工程师提供全面的理论指导和实践参考。1.2适用范围自然语言处理模型开发序列数据批处理优化深度学习系统架构设计高性能计算资源管理1.3核心问题研究问题:为什么深度学习模型需要将变长序列统一到固定长
- 深度学习分布式训练:并行策略与通信机制的系统性分析
Takoony
深度学习分布式人工智能
1.引言随着深度学习模型规模的指数级增长,单一计算设备已无法满足训练需求。以GPT-3为例,其1750亿参数在FP16精度下需要约350GB存储空间(每个参数2字节),远超当前主流GPU的显存容量(如NVIDIAA100的80GB)。根据OpenAI的技术报告[1],即使使用最先进的硬件,单卡训练GPT-3需要355年。这一计算瓶颈催生了分布式训练技术的快速发展。本文将从理论基础出发,系统性地分析
- TensorFlow为AI人工智能航空航天领域带来变革
AI原生应用开发
人工智能tensorflowpythonai
TensorFlow为AI人工智能航空航天领域带来变革关键词:TensorFlow、人工智能、航空航天、机器学习、深度学习、神经网络、自主系统摘要:本文探讨了TensorFlow这一强大的机器学习框架如何推动航空航天领域的创新。我们将从基础概念入手,逐步深入分析TensorFlow在航天器导航、卫星图像处理、飞行器自主决策等关键应用场景中的实现原理。通过实际代码示例和架构图解,展示TensorFl
- 多语言文本分类在AI应用中的实践
AI原生应用开发
人工智能分类数据挖掘ai
多语言文本分类在AI应用中的实践关键词:多语言文本分类、自然语言处理、机器学习、深度学习、BERT、迁移学习、跨语言模型摘要:本文深入探讨多语言文本分类在AI领域的应用实践。我们将从基础概念出发,逐步讲解其核心原理、技术架构和实现方法,并通过实际案例展示如何构建一个高效的多语言文本分类系统。文章将涵盖从传统机器学习方法到最先进的深度学习技术,特别关注跨语言迁移学习在实际业务场景中的应用。背景介绍目
- Orange3实战教程:图像分析---图像嵌入
err2008
Orange3实战教程数据挖掘神经网络自然语言处理机器学习计算机视觉深度学习orange3中文版
图像嵌入通过深度神经网络实现图像嵌入。输入图像:图像列表。输出嵌入向量:用数字向量表示的图像。跳过的图像:未计算嵌入向量的图像列表。图像嵌入功能读取图像并将其上传至远程服务器或本地计算。深度学习模型用于为每张图像计算特征向量。该功能返回一个增强的数据表,包含额外的列(图像描述符)。图像可以通过导入图像小部件导入,也可以通过电子表格中的图像路径导入。在这种情况下,包含图像路径的列需要一个三行表头,第
- 基于Paillier同态加密算法的金融数据安全共享机制研究【附数据】
金融数据分析与建模专家金融科研助手|论文指导|模型构建✨专业领域:金融数据处理与分析量化交易策略研究金融风险建模投资组合优化金融预测模型开发深度学习在金融中的应用擅长工具:Python/R/MATLAB量化分析机器学习模型构建金融时间序列分析蒙特卡洛模拟风险度量模型金融论文指导内容:金融数据挖掘与处理量化策略开发与回测投资组合构建与优化金融风险评估模型期刊论文✅具体问题可以私信或查看文章底部二维码
- YOLOv8实现手写数字识别系统:从MNIST到实时摄像头检测
在深度学习领域,手写数字识别是一个经典问题,也是入门计算机视觉的重要案例。本文将介绍一个基于YOLOv8和MNIST数据集的手写数字识别系统,该系统不仅能识别静态图像中的数字,还能通过摄像头实时检测手写数字。个人博客:YOLOv8实现手写数字识别系统:从MNIST到实时摄像头检测-iDing's博客项目概述这个项目结合了传统的MNIST数据集和现代的目标检测算法YOLOv8,实现了以下功能:将MN
- 基于深度学习的手写数字和符号识别系统:YOLOv5/v6/v7/v8/v10模型实现与UI界面集成
YOLO实战营
深度学习YOLOui人工智能目标检测计算机视觉
1.引言随着人工智能和深度学习技术的发展,手写数字和符号识别已经成为计算机视觉领域的重要研究方向。手写识别在很多实际应用中扮演着关键角色,例如邮政编码识别、表单自动处理和智能教育系统等。传统的手写识别方法通常依赖于复杂的特征工程,而深度学习则能够自动从数据中学习到特征,极大地提高了识别精度和速度。本文将介绍如何构建一个基于YOLO系列模型(YOLOv5、YOLOv6、YOLOv7、YOLOv8、Y
- AI作画:AI人工智能激发艺术创作灵感
AGI大模型与大数据研究院
AI作画人工智能ai
AI作画:AI人工智能激发艺术创作灵感关键词:AI作画、生成艺术、深度学习、神经网络、艺术创作、人工智能、创意工具摘要:本文深入探讨AI作画技术如何激发艺术创作灵感。我们将从基础概念出发,解释AI如何"学习"艺术风格并生成新作品,分析核心技术原理,提供实际应用案例,并展望这一领域的未来发展趋势。通过通俗易懂的讲解和实际代码示例,帮助读者理解这项融合科技与艺术的创新技术。背景介绍目的和范围本文旨在向
- Jetson平台编译Tengine
space01
AIoTJetson人工智能深度学习计算机视觉
1.Tengine简介Tengine于2017年在GitHub(https://github.com/OAID/Tengine)开源,是OPENAILAB(开放智能)推出的自主知识产权的边缘AI计算框架,致力于解决AIoT产业链碎片化问题,加速AI产业化落地。Tengine兼容多种操作系统和深度学习算法框架,简化和加速面向场景的AI算法在嵌入式边缘设备上快速迁移,以及实际应用部署落地,可以十倍提升
- 机器人-组成结构-感知 - 决策 - 执行
具身智能-查布嘎
具身智能机器人人工智能
目录一、感知系统内部传感器:外部传感器:二、智能决策系统机器学习家族1.1机器学习2.1深度学习2.2深度学习模型(主要属于监督/强化学习范畴,但结构通用):3.1监督学习3.2监督学习模型4.1半监督学习4.2无/半监督学习模型:5.1无监督学习5.2生成模型(可属于监督/无监督):6.1强化学习7.1其他学习三、控制系统(运控)①对应小脑和脊柱一、感知系统①对应人体的五官。由具有不同功能的各种
- 深度学习篇---矩阵
Atticus-Orion
嵌入式知识篇上位机知识篇嵌入式硬件篇深度学习矩阵人工智能
在机械臂解算、深度学习网络等硬件和软件领域中,矩阵运算作为核心数学工具,承担着数据表示、变换、映射和优化的关键作用。以下从具体领域出发,详细总结涉及的矩阵运算及对应的核心知识:一、机械臂解算领域机械臂解算(运动学、动力学分析)的核心是描述“关节空间”与“操作空间”的映射关系,矩阵运算用于精准刻画坐标系转换、运动传递和力/力矩分析。1.运动学解算(正/逆运动学)核心目标:通过矩阵描述关节角度与末端执
- Python深度学习实践:LSTM与GRU在序列数据预测中的应用
AI智能应用
Python入门实战计算科学神经计算深度学习神经网络大数据人工智能大型语言模型AIAGILLMJavaPython架构设计AgentRPA
Python深度学习实践:LSTM与GRU在序列数据预测中的应用作者:禅与计算机程序设计艺术/ZenandtheArtofComputerProgramming1.背景介绍1.1问题的由来序列数据预测是机器学习领域的一个重要研究方向,涉及时间序列分析、自然语言处理、语音识别等多个领域。序列数据具有时间依赖性,即序列中每个元素都受到前面元素的影响。传统的机器学习算法难以捕捉这种时间依赖性,而深度学习
- Baumer工业相机堡盟工业相机如何通过YoloV8深度学习模型实现打架检测(C#代码,UI界面版)
格林威
工业相机机器视觉数码相机YOLO深度学习计算机视觉人工智能
Baumer工业相机堡盟工业相机如何通过YoloV8深度学习模型实现打架检测(C#代码,UI界面版)工业相机使用YoloV8模型实现打架检测工业相机通过YoloV8模型实现打架检测的技术背景在相机SDK中获取图像转换图像的代码分析工业相机图像转换Bitmap图像格式和Mat图像重要核心代码本地文件图像转换Bitmap图像格式和Mat图像重要核心代码Mat图像导入YoloV8模型重要核心代码代码实现
- Baumer工业相机堡盟工业相机如何通过YoloV8深度学习模型实现人脸识别检测(C#代码,UI界面版)
格林威
机器视觉工业相机数码相机YOLO深度学习人工智能视觉检测c#
Baumer工业相机堡盟工业相机如何通过YoloV8深度学习模型实现人脸识别检测(C#代码,UI界面版)工业相机使用YoloV8模型实现人脸的检测工业相机通过YoloV8模型实现人脸识别检测的技术背景在相机SDK中获取图像转换图像的代码分析工业相机图像转换Bitmap图像格式和Mat图像重要核心代码本地文件图像转换Bitmap图像格式和Mat图像重要核心代码Mat图像导入YoloV8模型重要核心代
- Baumer工业相机堡盟工业相机如何通过YoloV8深度学习模型实现人物识别(C#代码,UI界面版)
格林威
工业相机机器视觉数码相机YOLOc#人工智能计算机视觉开发语言
Baumer工业相机堡盟工业相机如何通过YoloV8深度学习模型实现人物识别(C#代码,UI界面版)工业相机使用YoloV8模型实现人物识别工业相机实现YoloV8模型实现人物识别的技术背景在相机SDK中获取图像转换图像的代码分析工业相机图像转换Bitmap图像格式和Mat图像重要核心代码本地文件图像转换Bitmap图像格式和Mat图像重要核心代码Mat图像导入YoloV8模型重要核心代码代码实现
- Baumer工业相机堡盟工业相机如何通过YoloV8深度学习模型实现动物分类(C#源码,UI界面版)
格林威
机器视觉工业相机数码相机YOLO深度学习计算机视觉人工智能视觉检测c#
Baumer工业相机堡盟工业相机如何通过YoloV8深度学习模型实现动物分类(C#源码,UI界面版))工业相机使用YoloV8模型实现动物分类工业相机实现YoloV8模型实现动物分类的技术背景在相机SDK中获取图像转换图像的代码分析工业相机图像转换Bitmap图像格式和Mat图像重要核心代码本地文件图像转换Bitmap图像格式和Mat图像重要核心代码Mat图像导入YoloV8模型重要核心代码代码实
- AI 大模型重塑软件开发流程
万花丛中一抹绿
人工智能
一、AI大模型的定义与发展历史AI大模型是基于海量数据训练的深度学习模型,具备强大的自然语言理解、逻辑推理和知识生成能力。在软件开发领域,以GPT-4、CodeLlama、GitHubCopilotX为代表的大模型,能理解代码语法、语义及业务逻辑,实现代码生成、漏洞检测等复杂任务。其发展可追溯至2017年,谷歌提出Transformer架构,为大模型奠定了核心基础。2018年,GPT-1问世,参数
- 在 Conda 中删除环境及所有安装的库
Studying 开龙wu
conda
注意事项1.删除环境前确保你没有在该环境中运行任何程序。2.删除操作是不可逆的,所有该环境中的包和配置都会被永久删除。3.如果你想保留环境的配置信息,可以在删除前使用condaenvexport>environment.yml导出环境配置。关于requirements.txt和environment.yaml文件使用介绍详情可参考以往文章,争对机器学习和深度学习里Python项目开发管理项目依赖的
- OpenCV学习(二)-二维、三维识别
香蕉可乐荷包蛋
#OpenCVopencv学习人工智能
OpenCV是一个功能强大的计算机视觉库,可以用于识别和处理二维图像和三维图像。以下是关于二维图像和三维图像识别的基础知识和示例代码。1.二维图像识别二维图像识别通常包括图像分类、对象检测、特征提取等任务。以下是一些常见的操作:1.1图像分类使用预训练模型对图像进行分类,例如使用深度学习模型(如ResNet、MobileNet等)。importcv2#加载预训练的深度学习模型net=cv2.dnn
- 【人工智能之深度学习】6. 卷积核工作原理:从边缘检测到特征抽象的逐层演进(附可视化工具与行业实战代码)
AI_DL_CODE
人工智能深度学习卷积核特征提取卷积神经网络边缘检测特征可视化
摘要:卷积核是卷积神经网络(CNN)的核心组件,其通过局部感受野与参数共享机制实现高效特征提取。本文从数学本质出发,揭示卷积操作的空域-频域对偶性:空域卷积等价于频域乘积(F{f∗g}=F{f}⋅F{g}F\{f*g\}=F\{f\}⋅F\{g\}F{f∗g}=F{f}⋅F{g}),解释边缘检测核(Sobel、Laplacian)的频域响应特性。通过特征可视化实验表明,CNN特征呈现逐层抽象规律:
- 颠覆未来:创新代码引领人工智能与量子计算深度融合
金枝玉叶9
程序员知识储备1程序员知识储备2程序员知识储备3人工智能量子计算
摘要在信息时代飞速演进的背景下,人工智能与量子计算正以前所未有的速度互相融合,推动着科技边界的不断拓展。本文回顾了经典算法的智慧,展示了前沿深度学习模型的构建,并通过量子电路设计探讨了创新代码的可能性,为探索未来科技变革提供了全新视角。1.引言当前,科技创新正处于高速迭代的关键阶段,传统计算方法与新型技术的交汇处正成为研究热点。人工智能的发展已渗透到各行各业,而量子计算的崛起则为解决复杂计算问题提
- 集合框架
天子之骄
java数据结构集合框架
集合框架
集合框架可以理解为一个容器,该容器主要指映射(map)、集合(set)、数组(array)和列表(list)等抽象数据结构。
从本质上来说,Java集合框架的主要组成是用来操作对象的接口。不同接口描述不同的数据类型。
简单介绍:
Collection接口是最基本的接口,它定义了List和Set,List又定义了LinkLi
- Table Driven(表驱动)方法实例
bijian1013
javaenumTable Driven表驱动
实例一:
/**
* 驾驶人年龄段
* 保险行业,会对驾驶人的年龄做年龄段的区分判断
* 驾驶人年龄段:01-[18,25);02-[25,30);03-[30-35);04-[35,40);05-[40,45);06-[45,50);07-[50-55);08-[55,+∞)
*/
public class AgePeriodTest {
//if...el
- Jquery 总结
cuishikuan
javajqueryAjaxWebjquery方法
1.$.trim方法用于移除字符串头部和尾部多余的空格。如:$.trim(' Hello ') // Hello2.$.contains方法返回一个布尔值,表示某个DOM元素(第二个参数)是否为另一个DOM元素(第一个参数)的下级元素。如:$.contains(document.documentElement, document.body); 3.$
- 面向对象概念的提出
麦田的设计者
java面向对象面向过程
面向对象中,一切都是由对象展开的,组织代码,封装数据。
在台湾面向对象被翻译为了面向物件编程,这充分说明了,这种编程强调实体。
下面就结合编程语言的发展史,聊一聊面向过程和面向对象。
c语言由贝尔实
- linux网口绑定
被触发
linux
刚在一台IBM Xserver服务器上装了RedHat Linux Enterprise AS 4,为了提高网络的可靠性配置双网卡绑定。
一、环境描述
我的RedHat Linux Enterprise AS 4安装双口的Intel千兆网卡,通过ifconfig -a命令看到eth0和eth1两张网卡。
二、双网卡绑定步骤:
2.1 修改/etc/sysconfig/network
- XML基础语法
肆无忌惮_
xml
一、什么是XML?
XML全称是Extensible Markup Language,可扩展标记语言。很类似HTML。XML的目的是传输数据而非显示数据。XML的标签没有被预定义,你需要自行定义标签。XML被设计为具有自我描述性。是W3C的推荐标准。
二、为什么学习XML?
用来解决程序间数据传输的格式问题
做配置文件
充当小型数据库
三、XML与HTM
- 为网页添加自己喜欢的字体
知了ing
字体 秒表 css
@font-face {
font-family: miaobiao;//定义字体名字
font-style: normal;
font-weight: 400;
src: url('font/DS-DIGI-e.eot');//字体文件
}
使用:
<label style="font-size:18px;font-famil
- redis范围查询应用-查找IP所在城市
矮蛋蛋
redis
原文地址:
http://www.tuicool.com/articles/BrURbqV
需求
根据IP找到对应的城市
原来的解决方案
oracle表(ip_country):
查询IP对应的城市:
1.把a.b.c.d这样格式的IP转为一个数字,例如为把210.21.224.34转为3524648994
2. select city from ip_
- 输入两个整数, 计算百分比
alleni123
java
public static String getPercent(int x, int total){
double result=(x*1.0)/(total*1.0);
System.out.println(result);
DecimalFormat df1=new DecimalFormat("0.0000%");
- 百合——————>怎么学习计算机语言
百合不是茶
java 移动开发
对于一个从没有接触过计算机语言的人来说,一上来就学面向对象,就算是心里上面接受的了,灵魂我觉得也应该是跟不上的,学不好是很正常的现象,计算机语言老师讲的再多,你在课堂上面跟着老师听的再多,我觉得你应该还是学不会的,最主要的原因是你根本没有想过该怎么来学习计算机编程语言,记得大一的时候金山网络公司在湖大招聘我们学校一个才来大学几天的被金山网络录取,一个刚到大学的就能够去和
- linux下tomcat开机自启动
bijian1013
tomcat
方法一:
修改Tomcat/bin/startup.sh 为:
export JAVA_HOME=/home/java1.6.0_27
export CLASSPATH=$CLASSPATH:$JAVA_HOME/lib/tools.jar:$JAVA_HOME/lib/dt.jar:.
export PATH=$JAVA_HOME/bin:$PATH
export CATALINA_H
- spring aop实例
bijian1013
javaspringAOP
1.AdviceMethods.java
package com.bijian.study.spring.aop.schema;
public class AdviceMethods {
public void preGreeting() {
System.out.println("--how are you!--");
}
}
2.beans.x
- [Gson八]GsonBuilder序列化和反序列化选项enableComplexMapKeySerialization
bit1129
serialization
enableComplexMapKeySerialization配置项的含义
Gson在序列化Map时,默认情况下,是调用Key的toString方法得到它的JSON字符串的Key,对于简单类型和字符串类型,这没有问题,但是对于复杂数据对象,如果对象没有覆写toString方法,那么默认的toString方法将得到这个对象的Hash地址。
GsonBuilder用于
- 【Spark九十一】Spark Streaming整合Kafka一些值得关注的问题
bit1129
Stream
包括Spark Streaming在内的实时计算数据可靠性指的是三种级别:
1. At most once,数据最多只能接受一次,有可能接收不到
2. At least once, 数据至少接受一次,有可能重复接收
3. Exactly once 数据保证被处理并且只被处理一次,
具体的多读几遍http://spark.apache.org/docs/lates
- shell脚本批量检测端口是否被占用脚本
ronin47
#!/bin/bash
cat ports |while read line
do#nc -z -w 10 $line
nc -z -w 2 $line 58422>/dev/null2>&1if[ $?-eq 0]then
echo $line:ok
else
echo $line:fail
fi
done
这里的ports 既可以是文件
- java-2.设计包含min函数的栈
bylijinnan
java
具体思路参见:http://zhedahht.blog.163.com/blog/static/25411174200712895228171/
import java.util.ArrayList;
import java.util.List;
public class MinStack {
//maybe we can use origin array rathe
- Netty源码学习-ChannelHandler
bylijinnan
javanetty
一般来说,“有状态”的ChannelHandler不应该是“共享”的,“无状态”的ChannelHandler则可“共享”
例如ObjectEncoder是“共享”的, 但 ObjectDecoder 不是
因为每一次调用decode方法时,可能数据未接收完全(incomplete),
它与上一次decode时接收到的数据“累计”起来才有可能是完整的数据,是“有状态”的
p
- java生成随机数
cngolon
java
方法一:
/**
* 生成随机数
* @author
[email protected]
* @return
*/
public synchronized static String getChargeSequenceNum(String pre){
StringBuffer sequenceNum = new StringBuffer();
Date dateTime = new D
- POI读写海量数据
ctrain
海量数据
import java.io.FileOutputStream;
import java.io.OutputStream;
import org.apache.poi.xssf.streaming.SXSSFRow;
import org.apache.poi.xssf.streaming.SXSSFSheet;
import org.apache.poi.xssf.streaming
- mysql 日期格式化date_format详细使用
daizj
mysqldate_format日期格式转换日期格式化
日期转换函数的详细使用说明
DATE_FORMAT(date,format) Formats the date value according to the format string. The following specifiers may be used in the format string. The&n
- 一个程序员分享8年的开发经验
dcj3sjt126com
程序员
在中国有很多人都认为IT行为是吃青春饭的,如果过了30岁就很难有机会再发展下去!其实现实并不是这样子的,在下从事.NET及JAVA方面的开发的也有8年的时间了,在这里在下想凭借自己的亲身经历,与大家一起探讨一下。
明确入行的目的
很多人干IT这一行都冲着“收入高”这一点的,因为只要学会一点HTML, DIV+CSS,要做一个页面开发人员并不是一件难事,而且做一个页面开发人员更容
- android欢迎界面淡入淡出效果
dcj3sjt126com
android
很多Android应用一开始都会有一个欢迎界面,淡入淡出效果也是用得非常多的,下面来实现一下。
主要代码如下:
package com.myaibang.activity;
import android.app.Activity;import android.content.Intent;import android.os.Bundle;import android.os.CountDown
- linux 复习笔记之常见压缩命令
eksliang
tar解压linux系统常见压缩命令linux压缩命令tar压缩
转载请出自出处:http://eksliang.iteye.com/blog/2109693
linux中常见压缩文件的拓展名
*.gz gzip程序压缩的文件
*.bz2 bzip程序压缩的文件
*.tar tar程序打包的数据,没有经过压缩
*.tar.gz tar程序打包后,并经过gzip程序压缩
*.tar.bz2 tar程序打包后,并经过bzip程序压缩
*.zi
- Android 应用程序发送shell命令
gqdy365
android
项目中需要直接在APP中通过发送shell指令来控制lcd灯,其实按理说应该是方案公司在调好lcd灯驱动之后直接通过service送接口上来给APP,APP调用就可以控制了,这是正规流程,但我们项目的方案商用的mtk方案,方案公司又没人会改,只调好了驱动,让应用程序自己实现灯的控制,这不蛋疼嘛!!!!
发就发吧!
一、关于shell指令:
我们知道,shell指令是Linux里面带的
- java 无损读取文本文件
hw1287789687
读取文件无损读取读取文本文件charset
java 如何无损读取文本文件呢?
以下是有损的
@Deprecated
public static String getFullContent(File file, String charset) {
BufferedReader reader = null;
if (!file.exists()) {
System.out.println("getFull
- Firebase 相关文章索引
justjavac
firebase
Awesome Firebase
最近谷歌收购Firebase的新闻又将Firebase拉入了人们的视野,于是我做了这个 github 项目。
Firebase 是一个数据同步的云服务,不同于 Dropbox 的「文件」,Firebase 同步的是「数据」,服务对象是网站开发者,帮助他们开发具有「实时」(Real-Time)特性的应用。
开发者只需引用一个 API 库文件就可以使用标准 RE
- C++学习重点
lx.asymmetric
C++笔记
1.c++面向对象的三个特性:封装性,继承性以及多态性。
2.标识符的命名规则:由字母和下划线开头,同时由字母、数字或下划线组成;不能与系统关键字重名。
3.c++语言常量包括整型常量、浮点型常量、布尔常量、字符型常量和字符串性常量。
4.运算符按其功能开以分为六类:算术运算符、位运算符、关系运算符、逻辑运算符、赋值运算符和条件运算符。
&n
- java bean和xml相互转换
q821424508
javabeanxmlxml和bean转换java bean和xml转换
这几天在做微信公众号
做的过程中想找个java bean转xml的工具,找了几个用着不知道是配置不好还是怎么回事,都会有一些问题,
然后脑子一热谢了一个javabean和xml的转换的工具里,自己用着还行,虽然有一些约束吧 ,
还是贴出来记录一下
顺便你提一下下,这个转换工具支持属性为集合、数组和非基本属性的对象。
packag
- C 语言初级 位运算
1140566087
位运算c
第十章 位运算 1、位运算对象只能是整形或字符型数据,在VC6.0中int型数据占4个字节 2、位运算符: 运算符 作用 ~ 按位求反 << 左移 >> 右移 & 按位与 ^ 按位异或 | 按位或 他们的优先级从高到低; 3、位运算符的运算功能: a、按位取反: ~01001101 = 101
- 14点睛Spring4.1-脚本编程
wiselyman
spring4
14.1 Scripting脚本编程
脚本语言和java这类静态的语言的主要区别是:脚本语言无需编译,源码直接可运行;
如果我们经常需要修改的某些代码,每一次我们至少要进行编译,打包,重新部署的操作,步骤相当麻烦;
如果我们的应用不允许重启,这在现实的情况中也是很常见的;
在spring中使用脚本编程给上述的应用场景提供了解决方案,即动态加载bean;
spring支持脚本