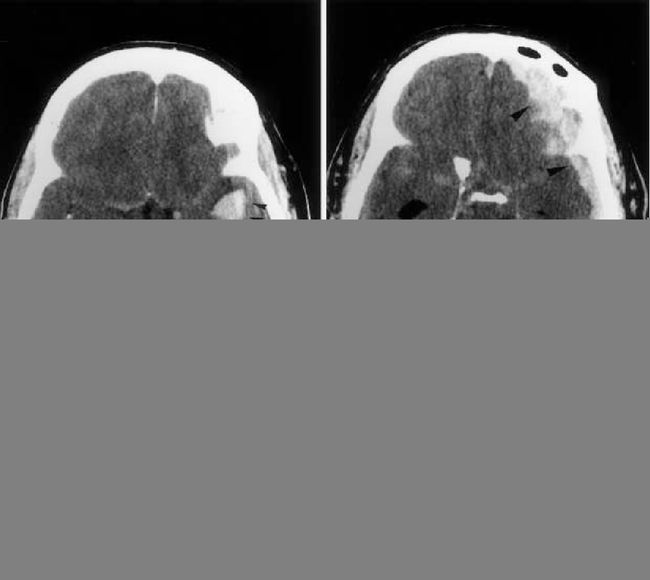
脑水肿和升高的颅内压
“脑水肿”是指“过量的水”在脑实质内的“病理性聚集”。
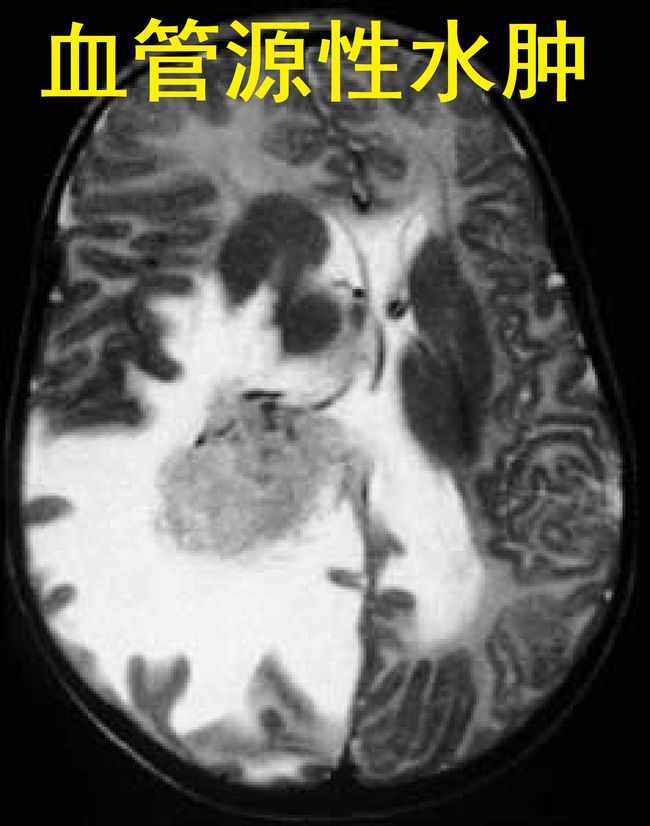
当“血脑屏障”的通透性增加,血液中的蛋白质、电解质和水产生外溢,进入实质性的细胞外间隙时,则产生了“血管源性水肿”。
“血管源性水肿”共同病因包括“轴内和轴外的脑肿瘤”及“脑脓肿”。
“血管源性水肿”对“脑组织的”影响是不成比例地,较多影响“皮层下白质”,而“大脑皮层”和“皮层下灰质”则相对不受影响。
当脑实质内的细胞膜破裂,使得水从细胞外转移到细胞内时,则产生了“细胞毒性水肿”。
“细胞毒性水肿”最常见的原因是“缺血性脑卒中”。不太常见病因包括“肝性脑病”和“雷氏综合征”。
“细胞毒性水肿”同时影响灰质和白质结构,导致影像上“皮质-皮层下结构”的界限消失。
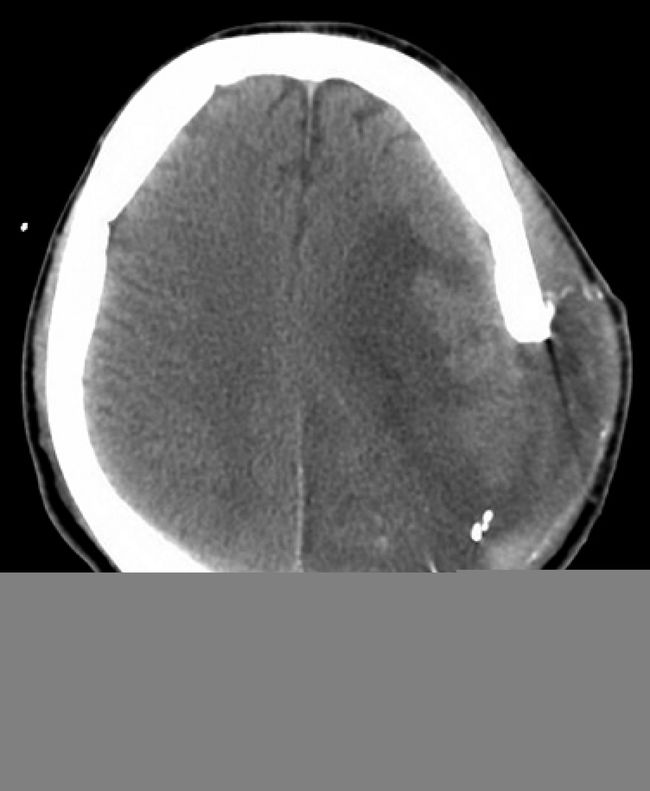
“创伤性脑损伤”和“脑内出血”能同时导致“细胞毒性水肿”和“血管源性水肿”。
当脑脊液从脑室内经过“室管膜”移行到脑实质内,从而形成“静水压性脑水肿”,其典型原因是梗阻性脑积水。
“脑水肿”会导致“颅内脑组织体积”的增加。“全脑水肿”则主要导致“颅内压全面升高”;而“局灶性脑水肿”可导致伴有或不伴有“颅内压”升高的“脑疝综合征”的发生。
脑水肿的治疗
“脑水肿”的治疗策略在很大程度上取决于“基础病因”和“脑水肿的类型”。
“梗阻性脑积水”引起的“静水压型水肿”的主要治疗方法是“脑脊液的分流”,通常是通过放置“脑室腹腔分流”而实现。
根据潜在的病因,“血管源性水肿”的治疗可以通过“皮质类固醇”、“渗透型药物”和“手术减压”来实现。
“细胞毒性水肿”的治疗方案则要有限的多得多。当“渗透型药剂”被用作一种暂时性措施且疗效不佳时,在适当的场合里可以考虑“外科手术减压”。
皮质类固醇
从1960年代开始,“地塞米松”一直作为治疗“轴内和轴外脑肿瘤”周围性“血管源性水肿”的中流砥柱。
“皮质类固醇”在“脑脓肿”引起的“血管源性水肿”治疗中的作用尚不明了。
尽管应用广泛,很少有临床试验用于确定“皮质类固醇”治疗“血管源性水肿”的疗效、最佳剂量和最适的持续时间。
地塞米松的初始剂量为每6小时4mg,随后的剂量根据临床表现而调整。
适合“外科切除”和“放疗”的脑肿瘤,“地塞米松”可在几周内逐渐减量到停药。
对于无法治疗的脑肿瘤,“地塞米松”作为一种姑息治疗措施,其剂量需要随着时间的延长而增加。
在“瘤周水肿”的急性治疗中、“地塞米松”的使用应仅限于可归因于“脑水肿”,而不是“局灶性肿瘤”引起的“神经损害症状”的患者。这些症状包括“脑移位”引起的严重头痛、下降的精神状态。
应警惕新发现的、等待组织学诊断的、怀疑“中枢神经系统淋巴瘤”的脑肿瘤,虽然不常见,但“皮质类固醇”的早期使用会引起“肿瘤坏死”,从而使得对患者进行了错误的诊断。
除去对“中枢神经系统淋巴瘤”的治疗,早期开始“皮质类固醇”治疗,还没有被证明能改变“脑瘤的临床病程”。
“皮质类固醇”在治疗“细胞毒性水肿”方面并没有显示出疗效。最新的“美国心脏协会管理指南”不建议在“脑梗死”和“小脑梗死”伴水肿的患者中使常规使用“地塞米松”。
类似地,不建议在“自发性脑内出血”患者中常规使用“皮质类固醇”。
“2017年脑外伤基础指南”指出,在“重度脑外伤”患者中,“高剂量甲强龙使用”与“增加的死亡率”有关,应当禁止使用。
重点总结
→ “皮质类固醇”在“细胞毒性水肿”的治疗方面是无效的,在“重型创伤性脑损伤”患者的治疗中是禁忌的。
→频繁使用“高渗盐水”可引起“高氯性代谢性酸中毒”,这和“神经危重病管理”中很高的死亡率有关。加用“醋酸盐的缓冲高渗溶液”可能会降低发生“高氯性代谢性酸中毒”的机会。
→在频繁使用“甘露醇”治疗的患者中,应监测血清渗透压。当血清渗透压超过320 mOsm/kg~340 mOsm/kg,或当渗透压间隙超过20 mOsm/kg时,应停止使用“甘露醇”。
→ “渗透性药剂”可暂时性用作“脑卒中”和“脑内出血”有关的“细胞毒性水肿”的治疗措施,但证明其有效的证据很弱。这些病变可能需要“外科手术减压”。
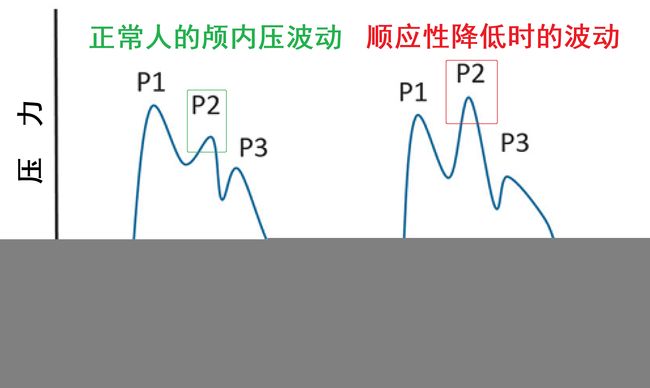
→在“全脑水肿”导致“颅内顺应性”变差的情况下,与头部水平位置、充血、高碳酸血症、发烧或疼痛有关的“颅内体积的微小变化”都可能会加剧已经“增高的颅内压”。
→ “颅内压的自发波动”,称之为Lundberg A波和B波,可能会导致持续数分钟的“颅内压自限性增加”。这些波动是“颅内顺应性差”的一个指标,但通常它们不经治疗就能自行缓解。
→采用“全身性升压”来增加“脑灌注压”,可反射性引起“脑血管收缩”,从而降低了颅内血容量,因而降低了“颅内压”。然而,“过度的脑灌注”可能会导致“血脑屏障破坏区域”出现“血管源性水肿”.
→现在的“脑创伤基金会指南”建议,“重型颅脑损伤患者”的颅内压应保持22毫米汞柱或以下,脑灌注压要≥50毫米汞柱~60毫米汞柱。
→一个最近的临床试验研究,将依据颅内压的治疗方案和一项依据临床检查和影像检查的研究进行了比较,发现两组的治疗结果并显着性差异(P>0.05)。
→ “戊巴比妥钠”滴注用于降低颅内压可导致严重的药物副作用,如“丙二醇毒性”、免疫抑制、胃肠动力受损和分布异常性休克。
→近期的一项临床试验表明,作为“重型颅脑损伤”的一种神经保护策略,“早期诱导低温”直接导致了“颅内压的降低”,但接受“低温治疗”的患者的“神经功能预后”很差。
→“诱导低体温”仍然是治疗“难治性颅内高压”的一种有用的“三线干预措施”,但是,一种有效的、包括对“寒战”的多种治疗方式的“低温治疗方案”也是必需的。
→最近的一项临床试验表明,去骨瓣减压术在治疗“重型颅脑损伤”的难治性颅内压升高方面,可提高患者生存率,减少患者重残的机会,但是“单纯的内科治疗”相比,更多的患者是在“植物状态下”存活。
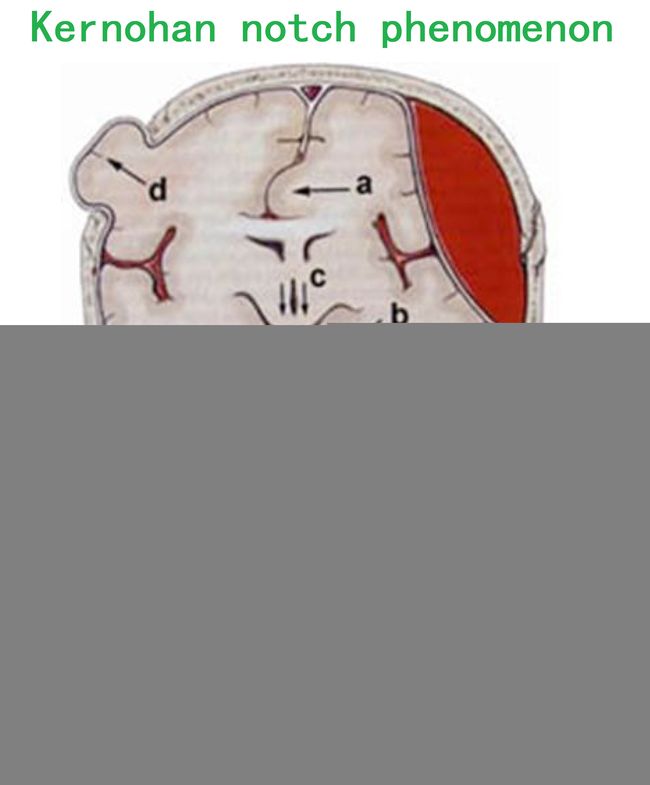
→“小脑幕切迹疝”发生时,“瞳孔扩大”与“占位病变”位于同侧,偏瘫可在对侧,原因是皮质脊髓束直接受累;但偏瘫也可能是在同侧,因为对侧大脑脚受压于小脑幕游离缘,即“Kernohan切迹现象”。
→连续的“床边瞳孔定量检测”,可在“小脑幕切迹疝”的“临床客观征象”出现前的几个小时就能检测到“瞳孔收缩速度”的降低,这可为“脑疝的预先治疗”提供时间。
→虽然有些患者能从“小脑幕切迹疝”中存活和恢复,但其后遗症可能包括“继发性脑干出血”,即Duret brainstem hemorrhage,“同侧大脑前动脉卒中”, “对侧大脑后动脉卒中”。
→ “后窝占位病变”可引起“小脑扁桃体疝”或“经过幕切迹的小脑上疝”,可不伴有“颅内压升高”或“瞳孔改变”。
来自魏社鹏的解读:
医学是个一门需要终生学习的职业。
很久很久很久没有查看过脑水肿的文献了,脑子里关于脑水肿的知识昨天还停留在上个世纪。
今天终于全面领会了脑水肿分为三种,第三种名字已经不再是间质性脑水肿了,而是静水压性脑水肿。
我们很多治疗脑水肿的药物都是针对血管源性水肿的,例如地塞米松,例如甘露醇。而不是针对细胞毒性水肿和静水压性水肿,后二者的治疗主要靠外科手段,例如去骨瓣减压和脑脊液外引流。
针对血管源性水肿,探索性的治疗药物还有:西乐葆,硫酸镁,阿托伐他汀。
脑瘤患者离不开地塞米松,尤其是终末期患者,地塞米松的使用不再是逐渐减量,而是需要逐渐加量。