生物界“AlphaGo”来了!蛋白结构预测AlphaFold大胜传统人类模型
乾明 编译整理
量子位 出品 | 公众号 QbitAI
AlphaGo和AlphaZero又有新兄弟,这次轮到科学家惊呆了。
DeepMind近日宣布,过去两年一直在研发AlphaFold:一个用人工智能加速科学发现的系统。
它仅仅基于蛋白质的基因序列,就能预测蛋白质的3D结构,而且结果比以前的任何模型都要精确。
在“蛋白质结构预测奥运会”CASP比赛中,力压其他97个参赛者。《卫报》报道称,AlphaFold预测出了43种蛋白质中25种蛋白质的最精确结构。在同一类别中排名第二的队伍,只预测出了3种。
△竞赛结果,谷歌为G043
相关的研究者纷纷表示,DeepMind厉害!很想知道他们方法的细节。
对于这项研究,DeepMind称其为“DeepMind在科学发现领域的第一个重要里程碑”,在生物学的核心挑战之一上取得了重大进展。
《卫报》评论称,这将“开启医学进步的新时代”。
到底是个多大的进展?
任何给定的蛋白质能做什么,取决于它独特的3D结构。 所以,能精确预测蛋白质的3D结构意义非凡。
首先,它能够帮助科学家更好地理解蛋白质在人体内的作用。对于诊断和治疗由蛋白质错误折叠引起的疾病,比如阿尔茨海默氏症、帕金森氏症、亨廷顿氏症等,至关重要。
其次,它会提高我们对身体及其工作原理的认识,使科学家能够更有效地设计新的、有效的疾病治疗方法。
随着我们通过模拟和模型获得更多关于蛋白质形状和它们如何运作的知识,会使药物开发方面更容易,同时也会降低相关的实验成本。
第三,它也有助于更好地设计蛋白质,一个例子是,可以推动可生物降解酶的进步,帮助我们控制像塑料和石油这样的污染物。
事实上,研究人员已经开始对细菌进行工程改造,使其分泌蛋白质,让废物可生物降解,进而变得更容易处理。
不过,仅仅根据基因序列来确定蛋白质的3D形状是一项复杂的任务。
挑战在于,基因序列中只包含蛋白质组成部分氨基酸残基的序列信息,这些氨基酸残基会形成长链。 预测这些长链如何折叠成复杂的3D结构,被称为“蛋白质折叠问题”(protein folding problem)。
蛋白质越大,氨基酸之间的相互作用越多,建模也就更复杂,困难度也会成倍上升。正如利文索尔佯谬(Levinthal’s paradox)中指出的那样,在找到一个蛋白质正确的3D结构之前,要列举一个典型的蛋白质所有可能的构型,需要的时间比宇宙存在的时间还要长。
那么,DeepMind解决这个问题的思路是怎样的呢?
DeepMind方案:基于深度神经网络
DeepMind表示,他们专注于从零开始模拟目标形状,而不是使用以前解决的蛋白质作为模板。
因此,在预测蛋白质结构的物理性质方面,DeepMind达到了非常高的准确性,然后使用两种不同的方法,来构建完整的蛋白质结构预测。
这两种方法都依赖深度神经网络,需要训练深度神经网络从基因序列中预测蛋白质的两种特性:
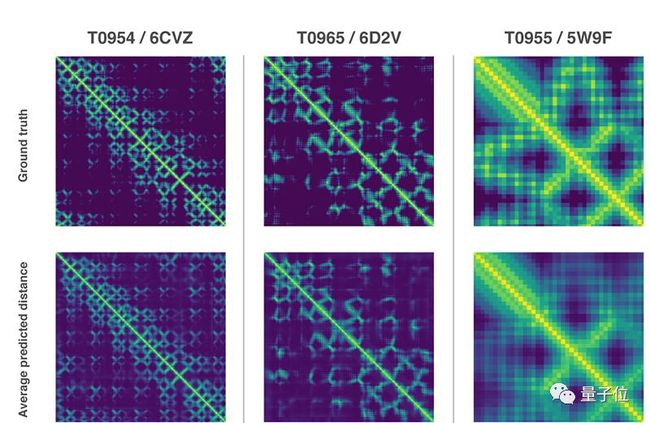
1) 成对的氨基酸之间的距离;
2) 连接这些氨基酸的化学键之间的角度。
具体的操作步骤为:
训练一个神经网络来预测蛋白质中每对残基之间的距离分布。然后,将这些概率组合成一个分数,用来估计一个蛋白质结构的准确度。
此外,DeepMind还训练了一个单独的神经网络,基于所有距离的总和来评估初步给出的蛋白质结构与正确答案的接近程度。
然后,基于这些评分函数,去找到符合预测的结构。
DeepMind使用的第一种方法,基于结构生物学中常用的技术,用新的蛋白质片段反复替换蛋白质结构的片段,他们训练了一个生成神经网络来发明新的片段,用来不断提高蛋白质结构的评分。
第二种方法是通过梯度下降法优化得分,这是机器学习中常用的一种数学技术,可以进行小的、增量的改进,从而得到高精度的结构。
他们将这项技术应用于整个蛋白质链,而不是那些在组装前必须单独折叠的片段,从而减少了预测过程的复杂性。
还有“一吨”多的想法
DeepMind的目标,是将AlphaFold打造成基础科学领域的AlphaGo和AlphaZero。他们表示,
我们首次涉足蛋白质折叠领域的成功表明,机器学习系统可以整合各种信息来源,帮助科学家快速找到复杂问题的创造性解决方案。
正如我们已经看到人工智能如何通过AlphaGo和AlphaZero等系统帮助人们掌握复杂的游戏一样,我们同样希望有一天,人工智能的突破也将帮助我们掌握基础的科学问题。
DeepMind的首席执行官Demis Hassabis对此信心满满。
“我们还没有完全解决蛋白质折叠问题,这只是第一步,”他说。“这是一个极具挑战性的问题,但是我们有一个良好的体系,我们还有’一吨’多的想法还没有实施。”
— 完 —
年度评选申请
加入社群
量子位AI社群开始招募啦,欢迎对AI感兴趣的同学,在量子位公众号(QbitAI)对话界面回复关键字“交流群”,获取入群方式;
此外,量子位专业细分群(自动驾驶、CV、NLP、机器学习等)正在招募,面向正在从事相关领域的工程师及研究人员。
进专业群请在量子位公众号(QbitAI)对话界面回复关键字“专业群”,获取入群方式。(专业群审核较严,敬请谅解)
诚挚招聘
量子位正在招募编辑/记者,工作地点在北京中关村。期待有才气、有热情的同学加入我们!相关细节,请在量子位公众号(QbitAI)对话界面,回复“招聘”两个字。
量子位 QbitAI · 头条号签约作者
վ'ᴗ' ի 追踪AI技术和产品新动态