基质辅助激光解吸电离(也就是通常所说的MALDI)于1987年首次由Hillenkamp 及Karas提出,如今已经30年。从那时起,通过应用这一“软电离”技术与飞行时间质谱(MALDI -TOF MS)的结合,成功地实现了为生物大分子提供快速和高度可靠检测手段的目的,同时也为生命科学领域提供了全新的分析方法。相比其他质谱技术,MALDI-TOF操作简便,不需要接受分析化学培训的专业人员就可以使用。特别是近年来在基因分型分析、生物标志物鉴定、病原体鉴定、质谱成像等应用的发展,越来越被临床检测领域所青睐。
近几年,国内在MALDI-TOF MS仪器的研发与生产快速起步,涌现了一批科研人员和企业,大大推动了MALDI-TOF MS国产化的进程。MALDI-TOF MS将可能成为首个由中国企业掌握最领先核心技术,并引领技术发展的质谱仪品类,这对我国在生物大分子分析研究、临床分子诊断应用等方面有极大的推动。
我于30年前开始,参与了一系列基于ESI及MALDI质谱产品的研发及研发管理工作,谨借此技术发表30年之际,对MALDI-TOF质谱技术的发展及其将来做作简单的回顾与展望。
关于MALDI的起源
MALDI在2002年与另一“软电离”技术电喷雾电离(ESI)同时得到了诺贝尔奖委员会的关注,日本岛津公司的田中耕一因激光解吸电离(LDI)技术的开发,与电喷雾电离的发明人John Fenn由于“开发了用于生物大分子质谱分析的软解吸电离方法”而分享了2002年诺贝尔化学奖。尽管田中耕一的方法使用了基于激光的软解吸电离方法从而获得诺贝尔化学奖,但他经常被错误地认为是MALDI的发明人。其实MALDI(基质辅助激光解吸电离)是首次由德国University of Münster科学家Hillenkamp 及Karas提出的,它与田中所发现的方法有一些本质上的区别。尽管两种方法都使用了激光,但在MALDI中,分析物混入基质中并被基质包围,基质分子吸收激光能量并将其中一部分转移到分析物(如蛋白质、核酸分子)上。而田中的方法则是在甘油中使用金属纳米粒子的悬浮液,分析物位于纳米颗粒的表面上。
通过实践的验证,Hillenkamp 和Karas所开发的基质辅助激光解吸的离子化效率更高,成为之后被广泛采用的技术。但田中是首先发表了可以使用激光解吸电离来分析和检测蛋白质类生物大分子,同时提醒了我们只是蛋白质离子化还是不够的,必须通过改进仪器的其他部分,尤其是探测器,而达到生物大分子分析的目的。
严格意义上讲,当今被广泛采用的MALDI-TOF质谱技术实际上是两个核心技术的组合,即基质辅助激光解吸电离与飞行时间离子分离技术。基质辅助激光解吸电离除与飞行时间结合外,同样可以与其它离子分离手段如四级杆、离子阱等相连接。但脉冲式的激光解吸电离方式无疑与在飞行时间质谱中同样采用脉冲式离子提取方式在耦合上有着许多优势,从而促成了MALDI-TOF这一质谱技术的出现。这一质谱仪器的发展史也是MALDI这一分子电离技术与TOF离子分离技术的相互依赖、相互推进的发展历程。
脉冲触发飞行时间的质谱仪设计在MALDI出现之前十几年就已经出现。在美国Texas A&M University的Macfarlane等通过放射性元素Californium-252轰击样本表面,以放射性自然脉冲触发飞行时间计时的原理设计了等离子体解吸电离(Plasma Desorption Ionization)飞行时间质谱仪,并用来分析较高极性的有机生物分子,成为当时最为成功、被认为最有潜力的蛋白质大分子分析的质谱工具。1984年首款基于这类原理的商业化产品由Bio-Ion Nordic AB生产并销售,该公司于1989年被Applied Biosystems Inc.收购。但这一技术可谓是昙花一现,很快就被崭露头角的激光解吸技术所取代。
激光电离(Laser Desorption)被研究得更久,但是直到适当吸收激光能量的基质被引入前的几十年中,在生物分子分析中的应用非常有限。Franz Hillenkamp,Michael Karas及其同事在80年代中期发现将丙氨酸与色氨酸混合并用266 nm激光脉冲照射可以更容易地将其电离,从而推断色氨酸吸收激光能量并帮助非吸收能力的丙氨酸电离,因而赋予了基质辅助激光解吸电离(MALDI)这个术语。当与这种“基质”混合时,分子量高达2843 Da的多肽Melittin同样可被电离。对更大分子的激光解吸电离的突破发生在1987年,岛津公司的田中耕一和他的同事使用了将甘油中的30 nm钴金属粉末与337nm氮气激光器相结合的“超细金属加液体基质法”用于电离。使用这种基质与激光的组合,田中完成了对分子量34,472 Da羧肽酶-A蛋白生物分子的电离,证明了激光波长和基质的适当结合可以使蛋白质电离。随后,Karas和Hillenkamp使用烟酸基质和266 nm激光电离了67 kDa的白蛋白(Albumin)。
Karas和Hillenkamp在1988年Bordeaux国际质谱会议上发布了使用静态电场反射式飞行时间质谱仪结合MALDI电离获得的β-半乳糖苷酶(分子量116,900)的光谱图,首次展示了单电荷离子质量大于100,000的质谱图,标志着MALDI-TOF MS新时代的来临。
Karas和Hillenkamp在1988年Bordeaux国际质谱会议上发布了使用静态电场反射式飞行时间质谱仪结合MALDI电离获得的β-半乳糖苷酶(分子量116,900)的质谱图
但从上图中质谱峰宽上可以看出,在初期工作中使用静态电场反射式飞行时间质谱获得的蛋白质量分辩能力是相当低的。人们很快就意识到这主要是由于离子在飞行过程中碎裂所致。
MALDI-TOF MS的诞生
第一台用于大分子分析的实用MALDI-TOF质谱仪是由美国Rockefeller University的Beavis和Chait在Hillenkamp发现MALDI后的几个月内搭建的。这是一个简单的线性飞行时间质谱,采用单静态加速电场,漂移管,和探测器。该仪器的加速电压高达30kV,飞行长度为2米。线性飞行时间分析仪的一个主要优点在于飞行过程中解离破碎的离子与稳定离子几乎同时到达离子探测器,从而消减了Hillenkamp等在反射式分析器中观察到的离子色散,提高了质量分辨能力。Beavis和Chait还对MALDI的基质进行了广泛的研究,实现了MALDI的进一步的改进。其开发的肉桂酸衍生物基质表明在260 nm和360 nm紫外波段间的任何波长都可以用来激光解吸蛋白质,使得波长为337 nm的更小型和相对便宜的氮气激光器同样可以应用在MALDI仪器上,取代了笨重昂贵的Nd:YAG激光器,受到20世纪90年代初商用仪器开发研究人员的青睐,直到至今还被广泛采用在商业化产品中。
首批商业化MALDI-TOF产品出现于上个世纪90年代初,由Dr. Marvin Vestal创建的Vestec公司(被PerSeptive Biosystems收购后又并入Applied Biosystems Inc公司)及本人当时所在的Finnigan公司在1990年分别开发生产出MALDI-TOF产品。Finnigan开发的LaserMAT飞行时间质谱仪是首款采用氮气激光器的线性MALDI-TOF产品,飞行管长度只有0.5米。而Vestec生产的飞行时间质谱仪采用了更长的飞行管,因此性能会好一些。下图是作者在1991年LaserMAT产品展台前的留影。
1991年本文作者周晓光在LaserMAT产品展台前留影
相比于几乎同时出现的电喷雾电离质谱市场的快速发展及应用推广,初期MALDI-TOF产品商业化的进程遇到了一些麻烦。这主要是由于TOF仪器性能偏低,特别是TOF的质量分辨能力不足,质量测量精度不高,如上述Finnigan LaserMAT的质量分辨率只有一两百,不能满足MALDI电离用于生物大分子的检测需求。但从另外一个角度看,MALDI电离技术的巨大潜力为飞行时间质量分析器提出了更高的要求,大大刺激了为这种电离技术特别定制改进的TOF仪器的发展。
TOF技术的发展
飞行时间(TOF)质谱在上世纪40年代中期首先由University of Pennsylvania的W. E. Stephens提出。当时在美国Bendix Aviation Corporation Research Laboratories工作的Wiley和McClaren于50年代中期完成了第一个实用型飞行时间(TOF)质谱仪的设计,并系统的描述了提高质量分辨能力的方式,首先提出了脉冲加速的时间聚焦概念,并描述了实现聚焦的一般条件。这些条件同样适用于MALDI以及其他电离技术,为之后的MALDI飞行时间质谱的发展打下了理论基础。但在之后的很长时间内,这项技术被普遍认为是研究离子特性基础研究的一种奢饰品,并没有被广泛应用于分析化学及解决实用问题之中。直到上世纪70年起,由于等离子体解吸电离(PD)、二次离子质谱(SIMS),特别是基质辅助激光解吸电离(MALDI)等脉冲离子源的出现,这项技术才重新引起大家关注。
早期高分辨MALDI-TOF MS的几项关键技术
理想的离子源是应该产生一个狭窄而几乎平行的离子束,不同质量大小的离子通过电场加速到达检测器的飞行时间与离子的初始位置和速度无关。而在MALDI解吸电离过程中,被检分子是被包埋在沉积在作为离子加速器电极的样品靶板表面上的基质晶体之中的。当激光脉冲对样本晶体照射时,产生包括带电离子在内的解吸物质羽流。普遍认为离子以百米至千米/秒的初始速度分布飞出。如果相同大小的两个离子以不同的初速度在飞行管中加速,则它们将在不同的时间到达离子探测器,导致峰展宽。正是由于离子间初速度的不同,造成了线性MALDI-TOF分辨率降低。因此提高线性MALDI飞行时间分辨率的关键之一就是在对离子初始速度分布进行再聚焦,以补偿离子初始速度的差异。Wiley和McClaren在1953年发表的文章中就已经有了具体的描述,但之后被大多科研人员遗忘了。
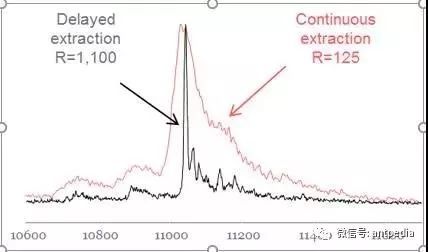
MALDI离子源出现后,1994年美国Utah State University的Lennon和Brown报道了在电离激光脉冲之后采用精确延迟的提取脉冲可以显著提高MALDI-TOF的分辨能力。Marvin Vestal马上意识到并将已经报道过的MALDI离子初速度分布与线性式和反射式飞行时间分析仪的聚焦关联连接起来,花了近一年的时间系统性地建立了TOF分析仪中各组件的理论模型,用以针对MALDI离子源的TOF分析器性能优化。其中最重要的工作之一就是重新发现和整合了延迟离子提取(Delayed Extraction),并将其引入到了MALDI-TOF仪器的设计中。这一技术是通过延迟离子提取电场的施加来改变不同初始速度的离子被加速的持续时间,最终使所有离子都同时到达探测器。这一改进将线性飞行时间的质量分辨能力提高了10倍以上。
延迟离子提取与连续离子提取质谱图对比
另外一种补偿MALDI离子生成初始动能差异的改进是通过在线性飞行时间管终端加入离子反射器。反射器(Reflectron)飞行时间的概念最早是由苏联科学家Mamyrin于1973年提出,它是由一系列均匀间隔的电极组成,在电极上施加离子飞行方向的反向电场。飞行管中相同m / z离子由于动能和速度的差异将导致进入反射器深度不同。具有较大动能的离子先到达并进入反射器,深入到反射场中飞行路径比具有较少动能的离子更长,因此与持后离子同时到达检测器。建立在Marvin的理论研究基础上,Applied Biosystems公司设计开发产生了Voyager系列产品,首次为蛋白质大分子分析提供了质量分辨能力超过10,000、质量精度高达10 ppm的高分辨MALDI-TOF质谱仪。从90年代中期开始,在市场上使用的商业化MALDI-TOF仪器中有一半以上是基于Marvin的理论设计的。
早期的MALDI-TOF仪器虽然有许多优点,但有一个主要限制:它们只能得到分析物的分子量,但无法测定结构。 因此,这些仪器不能用来确定对蛋白质化学家来说至关重要的蛋白质序列或翻译后修饰。为了通过MALDI-TOF获取蛋白、多肽结构信息,20世纪90年代早期德国科学家Kaufmann和Spengler利用亚稳态衰变离子在无电场区域飞行过程中碎裂后再被反射器分离,从而获得碎片离子质量信息,即所谓的后源衰变(Post Source Decay)技术,进行了多肽测序的工作。这一手段在某种意义上弥补了MALDI-TOF无法获取多肽结构信息的不足,但毕竟PSD碎片离子与通常的MS/MS碎片离子所包含的分子结构精度还是有很大差距。为了弥补这一缺陷,Marvin Vestal通过完善理论,将其扩展到串联TOF质谱,成功构建了MALDI-TOF-TOF仪器的设计理论,开发出Applied Biosystems公司的4700蛋白质组分析仪及后来升级版的AB 4800 TOF-TOF 质谱仪。这些仪器至今还在大多数蛋白质组学中心使用。 MALDI-TOF MS和MS-MS系统对包括蛋白质组学,糖组学,细胞信号,结构生物学,细胞器成像和聚合物科学等许多重要研究领域产生了巨大的影响。Marvin也因为在MALDI-TOF,TOF-TOF方面的贡献于2010年获得世界质谱界颁发的最高奖美国质谱学会杰出贡献奖。
在MALDI-TOF技术出现的早期,它主要是被应用在蛋白质的鉴定中。质谱蛋白鉴定的一种方法是通过将提取的蛋白质组经过内切酶的作用分割成多肽,然后比对MALDI-TOF MS质谱图中的多肽峰与从蛋白数据库所生成的多肽质量匹配程度,达到蛋白鉴定的目的。这种方法通常被誉为肽质量指纹谱分析(Peptide Mass Fingerprinting,PMF)。另外一种鉴定蛋白的方法是通过MALDI TOF-TOF将蛋白内切后的产生的多肽在串联质谱内轰撞成离子碎片,然后通过蛋白多肽串联质谱数据库搜索匹配多肽信息来确定蛋白。
相比蛋白和多肽,核酸的MALDI-TOF分析比较迟后,直到Becker研究小组1993报道了3-羟基吡啶甲酸(3-HPA)可作为良好的基质才有所突破。其中一个爆发点是应用于基因位点的单核苷酸多态性鉴定。1997年Applied Biosystems的Haff 和Smirnov首先建立了利用单碱基延伸(Single-base Primer Extension)化学与MALDI-TOF相结合的单核苷酸多态性(SNP)鉴定的质谱方法。这一SNP检测的主要优势在于可以在一个样品反应体系中同时检测多达几十个SNP位点(如图所示乳腺癌1号基因的检测)。
乳腺癌1号基因的SNP检测质谱图
2000年Applied Biosystems就已完成了基于这一方法的商业化产品开发工作。但由于商务上的考量,并没有将这一产品推向市场。而真正出现在市场上基于单碱基延伸质谱分析的商业化产品是几年后由Sequenom(现为Agena)公司推出的 MassARRAY产品。随着多位点SNP基因分型在临床及精准医疗应用中推广,以单碱基延伸化学与MALDI-TOF检测相结合的检测手段越来越被重视。
质谱成像技术
在MALDI-TOF技术出现后,美国Vanderbilt University的Richard Caprioli意识到这一分子检测技术具有二维扫描的特性,自90年代中期开始了利用激光扫描结合质谱分析的分子成像技术,探索开发一种新的方法来确定生物大分子在组织切片中的分布,特别是对传统的免疫化学无法进行分析的样本。他们使用的方法是用基质液滴喷洒冷冻组织切片,并用配备有精细激光焦点的MALDI-TOF仪器对组织样品进行扫描。这项技术,不光可以获取样品中的分子信息,同时可以在无化学标记的状态下获得生物分子在复杂表面的空间分布。这一结合为生物组织学研究人员提供了可以用于组织表面的直接生物分子表征的化学“显微镜”。
小鼠肾脏质谱影像
Richard Caprioli也因在成像质谱(Imaging Mass Spectrometry)上的开拓性工作,于2014年获得美国质谱学会颁发的杰出贡献奖。
MALDI自30年前出现至今已经成为分析各种非挥发性分子,包括蛋白质,肽,寡核苷酸,脂质,聚糖和其他具有生物分子的成熟技术。但在常规临床检测应用领域中的突破也只是出现在近年的临床病原体鉴定上。2001年美国University of Maryland的Ryzhov和Fenselau通过质谱分析微生物细胞内丰富的核糖体蛋白质分子指纹,提出了利用MALDI-TOF鉴定病原微生物的可能性。这种质谱分子指纹技术后被验证比基于微生物实验室通常使用的各种表型和生物化学测试方法更精确,速度更快。而且也为微需氧菌、厌氧菌、真菌、结核分枝杆菌及病毒等难鉴定、难培养病原体的鉴定弥补了生化鉴定方法的不足,被临床实验室逐渐所采纳。国外两家公司布鲁克、生物梅里埃推出的以线性MALDI-TOF仪器为基础的临床病原微生物鉴定系统已相继被美国食品和药物管理局(FDA)及国内药监部门批准用于病原体鉴定的临床应用。
MALDI的局限与改进
基于Vestal在90年代中期建立的MALDI-TOF仪器设计理论上开发的商业化产品出现后至今,该技术从根本上基本没有改变。但要进一步将此分析方法推向更宽广的临床检测领域,我们还面对着不少挑战,还需克服限制此质谱仪器被广泛接受的许多因素,例如仪器的制造成本和操作复杂性高,较差的可靠性,以及速度,全谱灵敏度分辨率和质谱光谱重现性不佳等。特别是这些因素造成人们普遍认为MALDI-TOF不是定量的分析手段,在临床分析应用中的进一步推广也因此受到影响。
要从应用角度解决质谱定量分析需要从几个方面着手:样品前处理,点样方式和仪器本身的定量分析误差。虽然在本世纪初Applied Biosystems相继开发了化学试剂iCAT(Isotope-coded affinity tag)和iTRAQ(Isobaric tags for relative and absolute quantitation)同位素代码标记定量技术,在一定程度上缓解了定量分析的瓶颈,但仪器本身的局限一直没有得到解决。我们必需从根本上寻找答案,也就是从离子生成、离子提取传输和离子检测几个层次入手。
首先,样本与基质分子形式的结晶层在MALDI靶板上的分布是不均的,因此优质的质谱图是需要通过寻找结晶层中“甜点”而获得。而通常此类仪器采用的氮气激光器的发射频率被限制在50Hz左右,所以通常在单位时间内仅有一小部分(通常<1%)样品分子被激光照射电离和分析,使每个叠加后的质谱图中离子强度重现性非常不稳定,误差会高达30%以上。而新一代的MALDI-TOF(如融智生物的QuanTOF)采用了5000Hz以上的半导体激光器,结合快速二维移动平台控制及高速离子探测与数据采集,可以在相同时间内完成几万到几十万次的激光照射,电离分析靶点上的大部分样品,减少了样品数量变化和分布不均造成的影响。
另外影响质量分析重现性的因素包括在MALDI离子源内的离子提取及加速电场的施加方式。上一代MALDI-TOF设计中,这些电压是加在靶板上的,造成在整个靶板上电场分布不均,从而使点在靶板不同位置上的离子感应到不同的电场,使得离子飞行时间的波动。而在新一代的仪器设计中(如QuanTOF)采用了靶板接地的专利技术,消除了靶板边缘电场的波动,进一步提高了质谱光谱的重现性。这一改进使质量检测的均一性会更好,特别对需要在空间维度上进行扫描的质谱成像应用有更大的意义。
新一代MALDI-TOF的另一改进是在全质量范围的检测性能。Wiley和McClaren在50年代就对飞行时间(TOF)质谱设计中无法对不同大小离子在初始空间及速度上同时完成聚焦有了阐述,加上通常MALDI-TOF激光照射入射角度的不对称性,使得传统MALDI-TOF仪器设计中有造成质量偏倚性的许多因素,在不同质量区间的分辨率、灵敏度有较大的区别。QuanTOF通过激光照射光学系统,离子光学系统,延迟离子提取,离子聚焦传输及混合离子检测器的创新设计及全面改进,实现了质谱分析在全质量范围内的分辨率、灵敏度的同步性能提升,提高了质谱定量检测分析的重现性。下图展示了对极高分子量蛋白质检测的能力。
新一代MALDI-TOF检测极高分子量蛋白的质谱图
新一代MALDI-TOF的定量分析性能提升可以从全血样品中血红蛋白糖化率测定上看出。下图中所示为3个不同糖化率的血红蛋白样本(分别为6%,9%,14%),每个样本被重复点在靶板上24个不同样点所获得的72张质谱光谱图的叠加。糖化峰三组不同浓度离子强度的重现性高达98%以上。
新一代MALDI-TOF检测3个不同糖化率的血红蛋白样本质谱图
全谱可定量MALDI-TOF将打开全新应用的大门
创新技术的进一步发展正在推动MALDI-TOF迈向更光明的未来,它将成为一项标准化技术被应用于疾病的病理学,个体化临床检测领域。MALDI方法可用于分析任何含有目标分析物的体液,包括血液和血液制品,母乳,脑脊液,淋巴液,唾液,尿液,胃和消化液,眼泪,大便,精液,前列腺液,阴道液,羊水和来源于组织的间质液。特别是新一代MALDI-TOF定量性能的提升将可更快被用于常规临床检测使用,除了用于病原体鉴定的用途外,我们将会看到这一技术将会被推广到:直接从血清,组织提取物和其他体液进行的癌症分型;组织成像;蛋白质修饰分析;小分子药物(体内)分布;生物标志物的鉴定和验证;质谱免疫测定;多肽定量;诊断和治疗相关生物标志物的临床测定等。