MP综述:植物-微生物互作的系统生物学
植物-微生物互作的系统生物学
Systems Biology of Plant-Microbiome Interactions
Molecular Plant
Impact Factor 10.812| CiteScore 7.15
https://doi.org/10.1016/j.molp.2019.05.006
发表日期:2019-05-22
第一作者:Patricia A. Rodriguez 1
通讯作者:Pascal Falter-Braun 1,4 Email: [email protected]
合作作者:Michael Rothballer1, Soumitra Paul Chowdhury1,Thomas Nussbaumer1,2, Caroline Gutjahr3
主要单位:
1网络生物学研究所,亥姆霍兹慕尼黑中心,德国环境卫生研究中心,德国慕尼黑(Institute of Network Biology (INET), Helmholtz Zentrum Munchen, German Research Center for Environmental Health, Munich, Germany)
2德国奥格斯堡慕尼黑工业大学环境医学研究所(Institute of Environmental Medicine (IEM), UNIKA-T, Technical University of Munich, Augsburg, Germany)
3植物遗传学,慕尼黑工业大学生命科学学院,德国弗雷辛(Plant Genetics, TUM School of Life Science Weihenstephan, Technical University of Munich (TUM), Freising, Germany)
4微生物-宿主相互作用,路德维希-马克西米利安-大学,生物学院,德国慕尼黑(Microbe-Host Interactions, Faculty of Biology, Ludwig-Maximilians-Universitat (LMU) Munchen, Munich, Germany)
日报
尽管本综述已经对植物-微生物互作的系统生物学进行了详实的阐释,但同时仍有许多疑问未能解决。为了解释基因的、微生物的、及代谢之间相互作用的,包括介导微生物-宿主相互作用的信号事件的复杂的关系,我们需要综合定量系统生物学方法,虽然Castrillo等人(2017)揭示了植物营养应激反应、免疫系统功能和微生物组装配之间的联系,但可能只是冰山一角,许多令人兴奋的机制仍有待发现,在这篇综述中,我们关注的是细菌间的相互作用以及小范围内丝状真核生物与宿主间的相互作用。本综述在进行大量前沿性工作汇报的同时也提出了很多疑问:
1、是什么决定了特殊的微生物-宿主互作的结果;
2、植物的免疫系统是如何区分开致病菌及有益菌并对抗前者促进后者的;
3、关于有益菌群与内共生菌在促进或中和有益效果方面的相互作用如何;
4、微生物释放的根际信号是如何被植物共同解释的以及不同分子对植物生长和抗逆性的协同或拮抗作用有多大;
5、植物如何将对微生物的识别与营养相关的信号结合起来;
6、如何通过植物识别和信息处理系统来实现有益菌和病原菌的区分,这将是未来十年植物系统生物学的一个关键问题;
相信带着疑问去阅读会带来更深刻的理解,同时了解前沿的研究方向。
摘要
ABSTRACT
自然环境中,植物与多样化的微生物相互接触且以各种复杂的方式相互作用。尽管为了更好地了解植物的防御病害机制而对植物与病原菌的相互作用进行过密集的研究,然而许多微生物及微生物组对他们的宿主有很多实质性的益处。这些益处包括促进营养的吸收、加速植物生长、增强抗逆性,提高对非生物逆境胁迫(热、干旱、盐)的抵抗力。然而,细菌菌株或它们的组合对宿主的有益影响通常是品种及物种特异性的,这就为大范围使用造成了困难。值得注意的是许多激发植物免疫反应的信号在分子水平上高度相似且在病原菌或有益菌中常常是相同的。因此,我们仍不清楚是什么决定了特殊的微生物-宿主互作的结果,以及是什么因素使植物能够区分开有益菌及病原菌。为了解释基因的、微生物的、及代谢之间的相互作用,包括介导微生物-宿主相互作用的信号事件的复杂关系,我们需要综合定量系统生物学方法。
关键字:植物系统生物学,植物微生物,微生物组,合成群落,微生物-宿主交互作用
Key words: plant systems biology, plant microbiome, microbial communities, SynComs, microbe-host interactions
引言
Introduction
近些年微生物的世界已经引起了人们极大地关注,随着测序费用的降低,使得对与宿主相关微生物的组成及动态变化的深度分析成为可能,无论对于人类还是植物,微生物在增加宿主健康方面的巨大潜力已经得到充分认可。展望未来精准农业,有益微生物的定向应用对于抵御来自于生物的、微生物的胁迫,确保产量稳定也许是一条可持续的途径。然而,大多数有益微生物都有密切的致病亲缘关系。人们还不清楚植物的免疫系统是如何区分开致病菌及有益菌并对抗前者促进后者繁殖。从进化的角度看,似乎甚至最早的真核生物就被多样的原核生物包围,从而真核生物进化成能区分有益菌及致病菌。因此,一个涉及到真核生物各个方面根深蒂固复杂的相互作用被预见到。因此,要了解微生物-宿主间的相互关系需要系统的优化生物“组学”及数量遗传学模型方法。
植物微生物组
Plant Microbiome
植物与种类繁多的微生物共生,包括细菌、卵菌、真菌、古菌以及极少探索的病毒世界。植物微生物组的组成是由非生物环境因素及其生物群落之间复杂的多边相互作用决定的。对于宿主来说,基于相互作用的结果,微生物被认为是互惠的、共生的或致病的。在这篇综述中,我们关注的是细菌间的相互作用以及小范围内丝状真核生物与宿主间的相互作用。
宿主相关微生物组的组成和动态
Composition and Dynamics of Host-Associated Microbial Communities
植物,植物器官及根源土壤的微生物组分析展现了一个多样性的高度动态变化的植物微生物组。一些研究表明,细菌群落结构组成是由不断变化的环境因素如土壤、季节、日间情况以及宿主因素如物种、生长阶段、区划等因素共同决定的。土壤和空气及其特性为植物相关的微生物提供了物理空间。空气中植物部分(即地上部)的微生物组容易被长距离的运输过程影响。然而,根部(即地下部)的微生物组会被土壤类型、土壤形成史,养分含量及水分含量所影响。尤其是在生长季,土壤也影响地上部的植物相关的微生物组。地下发现了更丰富、功能更好特征的微生物组。土体土的物种丰富度最高,根际部位减少(详者注:有时根际反而上升,即有土,又有根的作用),植物内部最少(植物内生菌),表明细菌生长有很强的区域选择性。与此同时,微生物细胞的数量从土体土到根表是逐渐增加的,表明对于被选的物种来说是一个优越的生长条件。尽管土壤具有丰富的生物多样性,植株根际及植物圈内的微生物组是由四个细菌门主导,包括放线菌门、拟杆菌门、厚壁菌门及变形菌门。有趣的是相同的细菌门也被富集在人体肠道内,表明它们适应与复杂的真核生物相互作用。这种相互作用的潜力可能是由于它们能够代谢宿主过剩的或主动提供的可被利用的营养物质。植物固定的碳的40%能够通过根被释放到根际,植物在塑造微生物组中扮演的积极的作用是显而易的。
细菌群落间有强烈的相互作用,比如它们之间的对抗、竞争和互利共生。微生物相互作用的共同模式是营养竞争、交换,甚至相互依赖,与此同时微生物间代谢物的相互交换有利于一些物种的生长。这也能扩展到细菌与真菌间的相互作用,因为植物与丛植菌根、真菌、固氮根瘤菌形成共生体的能力对周围微生物的群落有强烈的影响。因此,群落微生物间直接的协作与竞争的关系能够影响微生物的组成及对宿主的效应,并决定着给定条件下,微生物相互关系的结果。尽管直接的微生物与微生物之间的相互作用机制并不是本综述的重点,但当引进新的物种或群落到农业领域时,或当试图在复杂的微生物组中筛选有益物种时,记住这些也很重要。
鉴于根对于根际微生物具有强的选择力,植物基因型是否以品种的形式影响微生物组的组成这个问题被提出来。已有研究表明,与不同植物物种相关的微生物组可能有很大的差异。最初在玉米、大麦、拟南芥及其近缘种上的研究表明生态型或品种对于特定土壤根部的微生物组影响甚微,对于宿主基因型仅仅贡献了微生物组变化的5%-7%。这些差异仅仅是数量上的,他们不能找到一个细菌分类用来诊断给定的宿主基因型。目前,玉米根际微生物大规模领域的研究,用了27个玉米基因型,一个生长季内在五块不同的田块取样且进行五年,成功的鉴定了根相关的微生物组,展示了可重复的植物基因型关联。他们鉴定了143个OTUs且显著相关于植物基因型,尽管受植物年龄、气候和土壤因素混杂的影响。植物宿主的基因型对单个微生物种类的影响更为显著。在水培系统中,只用了根际微生物组中单独的一株菌(根际有益菌荧光假单胞菌 WCS365)筛选了大概200株自然界中的拟南芥物种。尽管保持大多数微生物组的完整,然后在自然土壤中种植选定的材料,发现其中两种材料可以抑制一些假单胞菌科的生长。因此,个别品种能够影响微生物组的结构,并且有时是以精确的方式。
这些相互作用不是静态的,新型的“请求帮助”的假设认为在特定的环境中植物招募能够缓解植物压力的特定微生物。我们首先注意到的是当植物生长在低的磷素或氮素条件下,能够招募运输营养的AM真菌与固氮根瘤菌。招募似乎是更为普遍的,然而,在被拟南芥透明孔菌(Hyaloperonospora arabidopsidis)感染后,拟南芥特定的招募了由三个菌株组成的协作组用来帮助其抵御侵染甚至增强土壤抗病能力使其成为抑病土,从而保护下一代植物不受病原菌侵害。因此,植物对微生物组的塑造并不局限于单个物种,而是可以扩展到小的微生物组。合成群落的应用已经开始帮助解开其潜在的关系。
通过合成群落了解微生物组与宿主的关系
Understanding Microbiome–Host Relationships Using SynComs
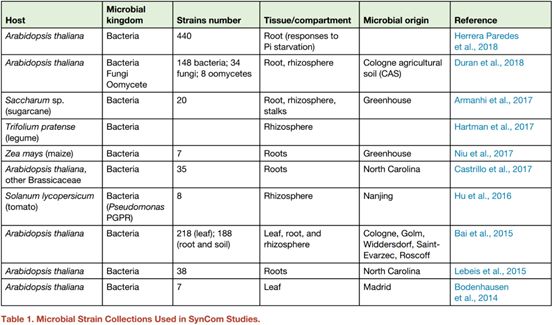
自然环境中,根际的多个物种界间相互关系的复杂性使阐明植物-微生物关联的机制和遗传学特性具有挑战性。在一个可控的环境中,一个强有力的研究其复杂性的方法是使用细菌合成群落(表1)。首先从一批分离的菌株培养开始,在无菌地环境中,合成群落能被混合并被用作给定宿主的接种剂。这允许剖析一个或少量的菌株群落是如何影响植物,以及宿主基因是如何影响微生物组成。筛选出的七个菌株的合成群落代表了拟南芥叶际的绝大多数门,相对于55A拟南芥突变体。对微生物组影响干扰最强的宿主等位基因体是影响角质层形成的突变体,然而免疫的突变体在这一环境中却很少受到影响。对于玉米根际,一个具有代表性的菌群组合被用于调查单个菌株对玉米整个群落结构的功能贡献。当去除一个群落成员导致物种丰富度的下降,这表明该菌株在已测试的菌群组合中具有关键作用。
表1:用于合成群落研究的微生物菌种收集
Duran等人(2018)报道了一个令人兴奋的研究,通过研究拟南芥根的微生物组来了解微生物间跨界的相互作用。在剖析研究了细菌、真菌、卵菌后,他们建立了对所有三组微生物的培养,用以探究他们的相互作用。在没有细菌的情况下,真菌和卵菌对植物的生长和存活有很强的危害作用。这两种效应在有细菌共培养时被中和。假单胞菌科及丛毛单胞菌科的菌株尤其有效;然而在缺乏来自这两个科各自的18个菌株时,其它细菌仍然对植物的存活有积极地影响。因此,细菌群落有助于维持微生物平衡,保护宿主植物免受丝状真核微生物的危害。
一个识别潜在功能关系的分析方法利用了日益增加的微生物组数据集。类似于转录的共表达网络,识别微生物组成员间正、负共发生相关关系是可能的,这也许反映了协同和拮抗的功能关系。这种关系可以表示为网络,并使用图论方法进行分析。如果相关性反映了功能相互作用,共现网络也许有助于制定对于微生物组的控制策略。初步结果表明,在来自相同界的微生物中正相关更为丰富,然而,正如前面的例子所示,在界与界的相互关系中负相关更为常见。在另一项研究中,一些细菌类群与致病的小麦真菌索氏根霉菌呈负相关。与其他生物网络相似,中心物种也可以被识别出来,它们之间有着大量的正负相关的相互作用,因此对群落的形成显得非常重要。因此,网络方法可以成为理解宿主相关微生物组动力学的重要工具。
植物相关微生物组对宿主具有有益的作用,但根际微生物组成和定植效率受环境因素、寄主的遗传和生理状态的影响。合成群落及网络的方法对于剖析形成因素及理解微生物组装配高度相互依赖的因果关系是重要的研究工具。植物的免疫系统需要区分有益微生物及致病微生物,并建立适当或完全相反的定殖激活或防御反应。
益生菌的功能及与病原体的相似之处
Functions of Beneficial Microbes and Similarities to Pathogens
在有益菌群中,在细胞内定殖的内共生菌因其能促进植物生长和增强植物抗逆性而被广泛研究。这些内生菌中研究得最好的是AM和根瘤共生菌。AM共生体发生在近80%的陆栖植物和真菌的球囊菌门(Glomeromycota)之间,它们通过交换光合作用固定的有机碳来增加植物的营养。根瘤与固氮菌的共生关系仅限于真双子叶植物中的一个分支,即,豆目Fabales、壳斗目Fagales,葫芦目Cucurbitales以及蔷薇目Rosales,其中的豆科植物与根瘤菌形成根瘤共生体,其他的植物则与弗兰克氏菌属(Frankia)的细菌有关。
相比之下,植物促生菌或植物根际促生菌被定义为“独立生存的植物有益菌,它能够促进植物的健康”,尤其是当植物暴露于非生物或生物的胁迫时。许多菌株有助于应对不只一种胁迫环境,这使得它们在各种环境下对农业应用具有吸引力。例如,从阿尔及利亚北部的盐渍土壤中分离出来的巴西固氮螺菌(Azospirillum brasilense)NH,能够显著的促进与提升不毛之地盐渍土壤中硬质小麦的生长及产量。在拟南芥中,Paraburkholderia(之前称为伯克氏霍尔德菌Burkholderia)能诱导细胞壁的增强及光合色素的增加从而提升耐寒性。此外伯克氏霍尔德菌能够增强宿主抵御细菌、真菌病原体的能力。据报道芽孢杆菌(Bacillus velezensis)NBRI-SN13也有同样的特征,这能够保护水稻抵抗多样的非生物胁迫,包括高温、低温、冰冻。类芽孢杆菌属中的菌株能为其宿主提供多样的益处,包括固氮、磷酸盐溶解和生物防治。一些分子机制已经被确定有助于有益的效果,包括通过化学途径增加营养物质的可利用性和浓度(固氮、磷酸盐或钾的溶解、铁的吸收),以及通过信号分子改变宿主生理状况。
除了这些相关与非生物胁迫的效应外,许多根际促生菌能够增强宿主抵抗病原体的能力。相较于由病原体激发的系统获得性抗性,诱导的系统性抗性可由根际非致病性及共生的微生物或化学诱导物激发。相似于获得性抗性,诱导性抗性使地上部植物组织能抵抗微生物病原体的侵袭。例如大麦接种假单胞菌属,能够增强作物抵抗真菌病原体禾顶囊壳菌(全蚀病的病原体)的能力。在苜蓿属的苜蓿中,AM真菌Rhizosphagus irregularis能够增强其对野油菜黄单胞菌的抵抗力,根瘤菌能够增强对白粉病的抵抗力。在一些情况下,微生物混合物比接种单一菌株具有更明显和更一致的效果。短小芽孢杆菌、枯草芽孢杆菌及萎蔫短小杆菌的组合对于提升黄瓜抵御不同病原菌的能力是更高效的。恶臭假单胞菌、鞘氨醇单胞菌属、巴西固氮螺菌、不动杆菌属的合成群落提高了玉米的抗旱性,并且通过接种黄单胞菌、寡养单胞菌和微杆菌提高了拟南芥真菌病原体的抵抗力。
总之,关于有益菌群与内共生菌在促进或中和有益效果方面的相互作用,我们知之甚少。例如根瘤菌在日本莲上的定殖,使其他的内生菌能够沿着侵染线搭便车在根瘤上定殖,侵染线是一种源于植物的亚细胞结构,能够引导根瘤菌进入根瘤内。这些共生体可能是中性的,也可能是有益的,但他们可能会导致植物碳的流失,对植物生长和产量造成不利的影响。几种AM真菌与植物根际促生菌的协作已经被介绍,用植物根际促生菌(芽孢杆菌或多肌芽孢杆菌)共接种AM真菌摩西球囊霉或地表球囊霉后,番茄植株的生长速度比单独接种任何一种微生物都要快。与此类似,将AM真菌与PGPR共接种后,番茄根结线虫病的发生率也明显降低。
虽然许多根际植物促生菌,特别是商业上可用的菌株,在不同的植物上定殖并发挥有益的作用,但它们的性能具有很强的物种或品种特异性。小麦品种对有益菌株的定植和反应性不同,例如巴西固氮螺菌属或者恶臭假单胞菌属。对于小麦,我们比较了AM真菌根内球囊霉、植物根际促生菌恶臭假单胞菌、及两者的结合对Mercato和Avalon的栽培品种的系统启动效应。在Mercato中,这两种微生物在启动和胼胝体沉积方面具有显著的协同作用,而在Avalon中,单独接种和联合接种后,胼胝体的反应是同等的微弱,Avalon的根也较少被这两种微生物定殖。
正如上面讨论的,植物也可以招募特定的微生物来帮助其应对特定的非生物或生物胁迫。一般来说,PGPR定植的触发型或本构型品种能力的分子决定因素尚不完全清楚。除了直接的遗传决定因素,如,沟通能力,间接因素也可能发挥作用。例如,栽培品种对养分的不同要求可能是决定一种条件是否经历胁迫的一个因素,从而决定PGPRs是否被招募。宿主微生物研究的重要问题是潜在的遗传决定因素与招募微生物的分子机制以及益生菌的能力,例如,将这种能力培育进入现有的优良品种。为了避免不良后果,这要求作物具备能够区分有益菌与密切相关的有害病原体的能力。
是敌是友:密切相关的益生菌与病原体
Friends or Foes: Closely Related Beneficials and Pathogens
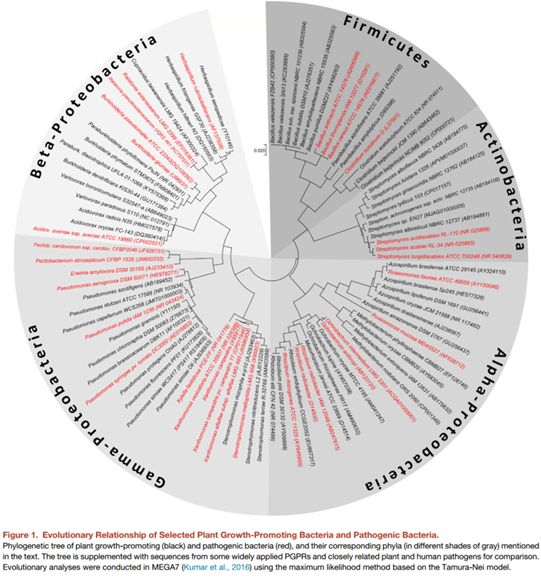
致病和有益的生活方式都需要与宿主识别和沟通,如从生物营养源中获益的能力,以及至少部分抑制宿主免疫反应的能力。对于内生菌与互惠共生体尤其如此,它们与病原体类似,能够进入植物宿主组织,待在那儿,但不会对宿主造成伤害,而且往往对宿主有益。由于这些相似的需求,实质上在宿主相关的所有微生物门中,与致病性和有益的生活方式密切相关的物种可以被发现(图1)。通常,在同一属内发现具有相反效果的菌的关系,例如,类芽孢杆菌科中:固氮类芽胞杆菌,解淀粉类芽孢杆菌;杆菌属中:贝莱斯芽孢杆菌,蜡样芽胞杆菌,及假单胞菌属中的水曲霉,丁香假单胞菌,以及甚至属于相同的种,例如绿脓假单胞菌。在链霉菌属中,铅青链霉菌可以保护植物抵御真菌病原体,尽管穿孔疥癣虫引起土豆、甜菜和胡萝卜的块茎及根部腐烂。在甘蔗、高粱和水稻中,锈菌属的成员通常是温和的病原体,尽管织片草螺菌及一些红白草螺菌据报道能够促进甘蔗的生长。尤其是内生菌,尽管被定义为生活在植物内部的共生体,一个在植物或人宿主中从有益的到致病的宽泛的相互作用能够被检测到。在蕨类植物中,用普通有益的荧光假单胞菌接种其细菌内生菌会导致有害影响。人肉毒杆菌是白三叶草中的一种有效的内生植物生长促进剂,但会导致在受其影响地区放牧的牛致命的肉毒中毒。在AM真菌中,可以观察到类似的宿主基因型依赖的相互作用结果,共生可能导致生长抑制。这一现象的分子原因尚未确定,但这可能是由于非最佳的兼容性导致的碳排放增加。有趣的是,在一组高粱的记载中记录了其对AM真菌不同的生长响应,他们之间强烈的正相关与负相关的关系依赖于植物与真菌的基因型;负生长反应与防御相关基因的表达相关。一个有趣的事情是从其宿主Serendipita籼稻(之前的Piriformospora籼稻)中分离根瘤菌F4,一种互利共生的根部真菌能够在多重高等植物上定殖包括大麦和拟南芥。endobacterium和真菌之间的联系对于真菌来说似乎是至关重要的的,S.籼稻不能通过endobacterium菌抗生素治疗得到完全治愈。R.
radiobacter F4是一种与特征明显的植物病原体R.
radiobacter C58(之前的根癌农根菌)密切相关的病原菌。当R.
radiobacter F4被用作接种剂接种在不同植物上时,R.
radiobacter F4被检测为植物内生菌,而且它的有益效果很难与接种真菌区分开来(包括endobacterium)。这使得F4成为真正的PGPR,并暗示着S.籼稻也许是PGPR的载体。
图1. 植物促生菌与致病菌的进化关系
植物促生菌(黑色)和致病菌(红色)的系统发育树,以及文中提到的相应的门(不同灰度)。该树补充了一些广泛应用的PGPRs的、密切相关于植物的及人类病原体的序列,以供比较。使用MEGA7基于Tamura-Nei模型的最大似然法进行了进化分析。
因此,有益的和致病的微生物具有共同的生理特征和进化相似性,在一定程度上,致病表型的表现可能取决于微生物的微小差异,有时甚至取决于宿主。相反,植物必须进化出复杂的机制来区分一种潜在的有益微生物(可以确保生存)和一种密切相关的潜在致命病原体。
分子的微生物-宿主相互作用的系统生物学方法
Systems Biological Approaches to Molecular Microbe–Host Interactions
在感染的情况下,植物免疫系统的遗传学及机制研究已经让我们大体上理解植物-病原体的相互作用。然而,如何通过植物识别和信息处理系统来实现有益菌和病原菌的区分,这将是未来十年植物系统生物学的一个关键问题。
植物对微生物的感知
Plant Perception of Microbes
成功的病原体和内生菌必须首先克服结构障碍像细胞壁、蜡质表皮角质层以及基本的抗菌产品,如组成型抗菌物质。这一共同的需求可能在一定程度上解释了有益菌和病原体在进化上的接近性。靠近细胞膜,微生物的存在是由植物表面被称为模式识别受体接收器的识别(PRRs)。这种对保守的病原体或微生物相关分子模式(PAMPs/MAMPs)的识别(如细菌鞭毛蛋白或延伸因子),导致细胞内信号传导,最终导致防御反应,被称为病原体或微生物引发的免疫(PTI/MTI)。MTI包括活性氧和氮氧化物的生产,气孔关闭,定向的胼胝质沉积,营养成分的转移,抗菌代谢产物的释放,植物防御激素信号的启动和转录变化。暴露于两片叶共生体中的拟南芥的转录组分析显示这些非致病性微生物确实激活了植物的第一层免疫反应。在共生体处理上大约有400个基因被诱导并且部分与由病原体P.syringae诱导的宿主基因重叠。强烈的免疫反应也许部分解释了受益者对ISR的诱导,然而,它并没有说明植物如何识别受益者。
PRRs的存在与否可以作为微生物定植于宿主范围的决定因素,然而,有益菌和病原体的分子模式即使不完全相同,也是相似的,这反过来又使它们难以按特定的PRRs进行区分。研究PRR功能的主要模型之一是FLS2,它能识别flg22-细菌鞭毛蛋白中最保守的基序。FLS2需要一个共受体BAK1来激活下游信号。有趣的是,BAK1也是BRI1的共同受体(不敏感的油菜素类固醇1),BRI1是一种富含亮氨酸的重复受体激酶(LRR-RK)能够感知植物油菜素类固醇(BR)并且在防御和生长信号之间起着整合的作用和额外的受体识别蛋白质的其他部分。西红柿在不依赖FLS2时可以通过FLS3而感知flgll-28,而水稻致病菌avenorax Acidovorax则具有不同的鞭毛蛋白基序CD2-1,其受体至今仍不为人所知。有趣的是,一些A. avenae菌株避免被鞭毛蛋白糖基化识别。与同样被病原体利用的这种掩蔽相比,一些有益菌具有避免被一种或另一种受体检测的抗原表位。然而,除了MAMP-掩蔽或逃避机制,许多受益者可能是通过鞭毛蛋白识别的并通过未知的机制抑制全面的免疫反应。Garrido-Oteret等展示了大多数由通过对拟南芥中纯化flg22的感知诱导的拟南芥基因受共生根瘤菌129E定植的影响而下调的。他们的分析表明,这种共生体有能力通过其他途径干扰MAMP-诱导的转录反应。由于该根瘤菌不具有III型分泌系统(T3SS)或者结瘤因子生物合成基因,信号似乎是通过其他杂聚肽PRRs复合物而起作用的。
共生生物与植物相互作用表明了潜在的敌友区分机制。在第一次接触时,AM真菌和根瘤菌会触发短暂的防御性反应,这些反应很快就会被抑制。已有研究表明,原癌基因和结瘤因子信号在这种抑制中起重要作用。这两种共生信号具有这样的能力即它们能够依赖于一个包含许多保守的共生蛋白的信号级联引发核钙振荡。宿主通过赖氨酸-基序 (LysM)受体激酶(RLK)感知结瘤因子,人们怀疑Myc因子也存在类似的受体。其中一些受体似乎也介导了对病原体的识别。OsCERK1是一个LysM-RLK,对水稻菌根真菌共生和稻瘟病菌抗性的建立具有重要意义,这表明它在共生反应和防御反应之间起着“分子开关”的作用。尽管这种潜在的双重功能的分子机制尚不清楚,我们仍认为特异性来自于与其他LysM-RLK的相互作用。这种双重功能的其他例子表明,这可能是一种更广泛使用的机制。NFP是一个蒺藜状苜蓿的结瘤因子受体,也能对感知与防御三叶炭疽杆菌、卵菌属无丝酵母菌属euteiches以及疫霉菌进行调节。
对典型PRRs和LysM-RLK的详细研究表明受体与辅受体之间组合的物理相互作用对于信号的特异性和信号的整合非常重要。自然界中的植物根系同时与大量的MAMPs和许多不同的信号分子进行接触。因此,通过相互作用的受体网络对不同的信号分子进行组合和定量的感知,对特定的微生物组合做出特定的响应,这是不太可能,也是有可能的。因此,需要对PRR信号整合全局系统方法。SmakowskaLuzan等人(2018)的蛋白质组规模的互作研究是全面了解这一关键植物感知系统的重要一步。利用生化降温实验,他们绘制了由拟南芥中225个LRRRKs(CSILRR)所形成的物理细胞表面相互作用网络。CSILRR揭示了所有LRR-RKs的高度互联性,它们集中在几个模块中,其生物学相关性尚待阐明。重要的是,作者表明不仅直接的相互作用,而且间接的网络效应调节下游的信号输出,并且整个网络共同提供植物免疫系统的平衡反应。利用LRR-RK网络表征综合信息处理是了解植物免疫的关键。
细菌信号:群体感应和共生因素
Bacterial Signaling: Quorum Sensing and Symbiosis Factors
除了感知保守的微生物模式,植物还利用代谢物、挥发物、共生信号和群体感应(QS)分子介导的细菌交流。n-酰基高丝氨酸内酯(AHL)是细菌联络的关键成分,同时也能被植物感知到。对有益菌Acidovorax radicis N35来说,这已被证明,这里产生ahl的野生型菌株能够抑制大麦的防御反应,而接种不产生ahl的突变体后,黄酮类化合物的防御作用增强。其他的例子显示了AHLs对寄主植物的促生和启动作用,如苜蓿,番茄,拟南芥、大麦。由于致病菌也会产生AHL,这些信号物质不太可能单独为植物提供足够的信息来调节其防御反应。QS分子的组合和浓度可能表明了不平衡的微生物组成。尽管AHLs的生理效应已经得到了一些详细的描述,但植物感知这些细菌分子的途径和机制尚不清楚。有趣的是,脂质壳寡糖,也就是原癌基因和结瘤的共生因子,甚至在不形成共生关系的植物中,也能促进根系发育、种子萌发和植物生长。因此,共生因子识别和信号系统在一定程度上独立于宿主的共生能力。需要进一步的研究来了解微生物释放的根际信号是如何被植物共同解释的,以及不同分子对植物生长和抗逆性的协同或拮抗作用有多大。
微生物-宿主相互作用的激素信号传导
Hormone Signaling in Microbe–Host Interactions
植物激素信号传导本质上是所有植物生理过程的中枢。防御反应通常由水杨酸(SA)、茉莉酸(JA)和乙烯(ET)介导。而SA介导SAR和对生物营养和半生物营养病原体攻击的防御,JA和ET介导ISR和对坏死营养物质和昆虫的防御。其他激素主要控制发育过程(生长素,赤霉素[GA], BR,或细胞分裂素[CK]),或非生物胁迫的反应(脱落酸[ABA])。除了这些看似简单的分类,然而,很明显激素信号是高度整合的,多种激素会影响任何感兴趣的过程。因此,植物激素对植物与微生物的双向交流也有重要意义。例如,在磷酸盐或氮缺乏的情况下,从根部分泌独脚金内酯来吸引AM真菌,它们的生物合成在定植后受到抑制。相反,GA、SA和ET抑制AM和根瘤共生,而生长素和脱落酸对AM的发育具有浓度依赖性的积极影响。结节形成需要细胞分裂素信号和局部生长素信号。茉莉酸在共生体建立中的作用是模棱两可的,可以是积极的、消极的,也可以是中性的,这取决于条件和植物种类。
激素信号系统受到有益菌和致病菌的积极调节。最著名的,冠菌素(COR)是一个由致病的P. syringae pv. tomato DC3000(Pst)产生的毒素,他模仿植物茉莉酸-异亮氨酸(JA-Ile),甚至更为活跃。这种基于茉莉酸的防御机制的激活导致了适当的水杨酸介导的半生物营养Pst防御的抑制。一般来说,病原体操纵植物信号来抑制防御反应,并将营养物质重新分配到受感染的组织中,从而实现持续的致病性定植。有益菌株往往对SA-JA平衡产生相反的影响,在拟南芥、P. cens Pf4、P. aeruginosa Pag或B. velezensis LJ02中,这可以以不同的方式表现,它们会引起植物不同部位内源SA水平的升高;其他菌株降低JA-Ile水平,并且Paraburkholderia phytofirmans PsJN降低了JA-生物合成的表达和损伤诱导的JA积累。因此,微生物源的植物激素根据植物与微生物的个体组合调节多种作用。尽管不同的研究报告了相反的结果,SA信号系统对根微生物组的形成也起着关键作用。一项研究只报道了SA突变体对微生物组组成的轻微影响。相比之下,Lebeis等(2015)报道,缺乏SA的合成或感知能力的拟南芥突变体改变了根际微生物组,而相应的JA和ET突变体则没有观察到这种效应。
除了对病原体和有益菌这些常见的调节防御外,许多PGPRs通过产生生长素、赤霉素或细胞分裂素来调节植物的生长,特别是根系的生长。为了剖析潜在的复杂性,利用包括代谢组学、全局网络分析、激素表征分析以及植物和土壤中分子过程的集中定量建模在内的系统生物学方法来补充遗传学将是非常重要的。后者是植物根系生长素信号转导的积极研究方向,目前已有先进的模型。这种定量模型的开发是通过详细的力学知识实现的且荧光生长素报道者提供生长素分布的时间解析数据。两者都为定量时间解析模型提供了基础。通常缺少关于分子和受体的定量数据,这些分子和受体将给定的生长素浓度转化为特定的转录反应,虽然关于生长素浓度对受体对影响的初步数据是可用的。为了理解微生物与宿主之间的相互作用,SA信号通路的模型将是强有力的。最近描述的SA受体(NPR1、NPR3、NPR4)共同介导对不同SA浓度的反应。相比之下,较远的家族成员BOP1和BOP2似乎在SA信号中没有功能,但却参与了豆科植物开花和结瘤等发育过程。同时,NPR1(也许还有它的旁系同源基因)的生物化学调控是复杂的,涉及多个细胞间隔、氧化还原电位、磷酸化和降解。因此尽管对于模型发展的关键要素是知道的,包括TGA转录因子、信号网络组件,但是对这一关键免疫信号系统的了解还不完全。荧光SA传感器的发展以及定量蛋白水平和结合数据的发展是SA信号定量建模的重要内容。
除了个别途径外,所有激素信号通路都是相互联系的,很少有生物学反应是由单一激素介导的。Tsuda等对拟南芥免疫过程中SA、JA、ET之间的信号传导进行了大量的破译工作。他们将激素信号网络分为四个部分(SA, JA, ET,和PAD4),用一组MAMPs和效应剂刺激后,定量评估属于这些区域的所有可能突变体的免疫。他们的工作表明,激素网络的组成与添加剂、增效作用和代偿作用之间存在很强的相互作用。该小组后来的工作使他们提出,PTI信号网络对干扰具有高度缓冲性,例如对病原体效应物的干扰。
互作网络分析
Interactome Network Analysis
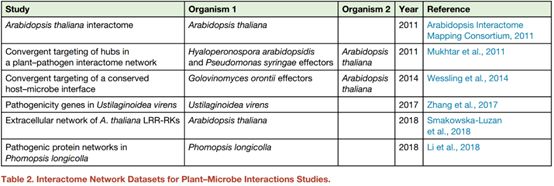
在缺乏定量动态模型的情况下,分子相互作用网络方法可以很有效地识别分子宿主-微生物相互作用的模块、路径、组件和系统级模式。为了将宿主与微生物的相互作用数据置于宿主生物学的背景下,需要一个参考蛋白网络。植物相互作用组分析始于发表第一份物理蛋白质-蛋白质相互作用的实验图谱,该图谱描述了数千种拟南芥蛋白质之间的相互作用:拟南芥互作-1 (AI-1),它提供了植物分子连接性的第一个综合视角。自那时以来,编制了补充的和更专业的地图,这便于分析具体的进程(表2)。对于膜蛋白,利用裂解泛素系统可以获得一个大约包含12000个蛋白-蛋白相互作用的图。一个G蛋白相互作用体揭示了G蛋白在调控细胞壁修饰中的新作用,这是一个与防御高度相关的过程。近年来,利用蛋白质间图谱技术,构建了一种用于真菌大豆拟茎点种腐病菌(大豆种子腐烂的原因)的蛋白质-蛋白质相互作用网络。也就是在生物之间的保守蛋白质对之间传递相互作用的注释以及允许疾病相关亚网络的检测。
表2. 植物-微生物互作研究的网络数据集
病原体和有益微生物可将数百种(毒力)效应蛋白传递到寄主植物的胞质和质外体中,以调节植物的防御和生理功能。为了理解宿主与微生物之间的相互作用,需要以一种综合的、时间解析的方式来理解它们的功能。最初的植物靶向致病菌效应物是通过小规模研究来表征的,结果表明,毒力效应物可以改变宿主蛋白功能,干扰免疫反应,促进疾病的发生,这就是导致植物产生效应因子激活的感病性。通过宿主抗性蛋白(R蛋白)识别病原体效应器可导致触发效应免疫(ETI)。为了获得系统水平的效应蛋白功能,一个大规模的相互作用体研究(PPIN-1)绘制了细菌病原体Pst和拟南芥卵菌病原体活体营养型卵菌的毒力效应蛋白与AI-1宿主网络中的蛋白之间的相互作用。后来的一项后续研究增加了来自活体营养的子囊菌Golovinomyces orontii的效应因子之间的相互作用。数据显示,来自三种病原体的效应因子部分地聚集在共同的宿主蛋白上,其中许多是宿主网络中高度连接的中心节点。根据收敛程度的不同,宿主蛋白的基因验证率在目标蛋白为100%和目标蛋白为40%之间,除了收敛性,许多效应因子还能在宿主网络中靶向蛋白质,这可能是高度缓冲的免疫信号网络的结果。群体遗传学分析显示,在高靶向蛋白质的直接网络附近存在着积极和平衡选择的证据。因此,病原体施加的选择性压力似乎被围绕效应器靶标的网络所吸收。这一发现强化了宿主与微生物之间的相互作用是由高度集成的网络介导的这一观点,并且只能通过对孤立通路的分析才能完全理解。对鼠疫耶尔森菌相互作用体的研究表明,病原体似乎重新排列了宿主网络,而不是破坏了网络的完整性。
效应蛋白的存在并不局限于病原体,菌根真菌、内生真菌和固氮根瘤菌也具有调节植物免疫反应和共生相互作用的效应蛋白。一些PGPRs,如P. simiae WCS417,和许多复杂的微生物组数据集中的变形杆菌菌株被预测具有功能性的T3SS和效应器。对于有益的印度乳杆菌和根瘤菌,它们的毒力效应物在富有成效的及有益的相互作用中是重要的。T3ss介导的埃氏慢生根瘤菌的效应物甚至可以使结瘤因子独立于大豆的结瘤。除了T3SS外,许多变形杆菌还具有IV型和VI型分泌系统,可以将细菌蛋白传递到宿主和其他微生物中。P.simiae WCS417有两个T6SS位点,不仅可以向其植物宿主传递效应因子,还可以向其他竞争微生物传递效应因子,从而调节周围的微生物组。蛋白质组学方法有助于揭示微生物效应库的多样性。一项研究比较了有益的土壤真菌炭疽杆菌与致病真菌炭疽杆菌的基因组,发现它们的分泌体并没有本质上的不同,但有益真菌在植物体内的效应基因减少了50%,致病性相关基因的激活也减少了。因此,微生物的分泌物以及分泌物效应器的数量和性质可能构成有益菌和病原体之间的一个重要鉴别点。最有可能的是,有益的效应体的完善对非致病性相互作用很重要。系统生物学的一个重要挑战将是了解针对宿主网络不同部分效应器的全局动态,以及这种动态如何相关于ETS及EIT,以及病原菌和有益菌之间分泌的效应器的系统水平和动态差异是什么。
除了蛋白质,近年来,RNA作为宿主和微生物之间重要的通讯分子而出现,它们通过细胞外囊泡(EVs)传递给宿主。首先在哺乳动物细胞中发现,EVs存在于细菌、古生菌和真核生物中。从灰霉病菌中提取的小RNA对拟南芥的宿主防御基因具有靶向性. 植物能够通过宿主诱导的基因沉默(HIGS)利用dsRNA沉默这些外来转录本, 在真菌感染过程中,植物EVs和多泡体在胞间连丝周围聚集,以促进感染部位胼胝质沉积。 EVs及其RNA载体构成了另一个联络层,其意义才刚刚显现。
转录调控网络
Transcriptional Regulatory Networks
转录谱分析被广泛使用及关键研究的结果在本文中被提到。虽然比较转录组学是常规的,但共表达相关网络和因果调控网络较少使用。共表达网络基于这样一个概念,即时间序列的转录谱可能表明转录之间的因果关系。加权基因相关网络分析(WGCNA)是一种常用的基因层次聚类成共表达模块的方法。这些模块与信号网络连接、代谢途径或表型特征进行比较。除了WGCNA之外, Saelens等人系统比较了42种不同的聚类、分解、双聚类和迭代网络推理方法。这些技术已经被应用于拟南芥和其他植物,如玉米和小麦以探索它们与微生物的相互作用。所识别的模块提供了对共有相同功能基因的首次洞察并有助于更好地理解其与感染或共生相关的过程。
土壤中的代谢交换和营养竞争
Metabolic Exchanges and Nutrient Competition in the Soil
微生物与宿主相互作用的基本原理之一是代谢交换。植物提供光合作用产生的40%的复合碳通过根进入根际来滋养微生物。相反,真菌和细菌促进植物对磷、氮和铁等基本营养物质的溶解和吸收。营养物质的重定位是病原菌通过效应因子和激素信号进行植物重编程的一个重要目标。基因组级代谢模型已被用来研究单个生物体的代谢,群落层面反应的建模正在取得进展,但具有挑战性。原核生物的代谢模型是目前常用的模型;在植物方面,已经建立了拟南芥、大麦、玉米、高粱、甘蔗和油菜的代谢模型。因此,可以通过网络比较分析有益菌和病原菌的代谢能力。Mithani等人(2011)验证了假单胞杆菌已进化成为一种植物致病性生活方式的代谢特化的假说。对9株假单胞菌代谢网络的比较表明致病的假单胞杆菌与有益的相关荧光假单胞菌 Pf-5的代谢非常相似,因此代谢可能不是一个关键的区别特征。近年来,一个针对疫霉菌感染卵菌的生命阶段特异性基因组级代谢模型被建立起来,该模型可以预测不同细胞间和病原体阶段的生化反应。通过测定代谢物的水平来限制这些模型的建立,从而获得更精确的定植环境下植物和微生物代谢变化的图像,这将是非常重要的。
整合多组学建模
Integrated Multi-omics Modeling
虽然植物和它们的微生物组之间有明显的互利关系,而且“呼救”可以招募微生物来支持宿主,但目前还不清楚植物如何将对微生物的识别与营养相关的信号结合起来。磷通常以高的浓度存在,但植物可吸收的正磷酸盐在土壤中是稀缺的。在一个优秀的多组学中,系统生物学实践中,Castrillo等人(2017)阐明了营养和防御之间的联系。通过结合16S rRNA基因测序、全基因组表达分析、合成群落(SynComs)的分析和建模,以及功能分析,他们表明植物的磷酸盐饥饿反应(PSR)在调节根微生物组方面具有重要作用。他们证明,与野生型相比,不同的根相关微生物组是由磷摄入缺乏的和磷高积累的拟南芥突变体装配而成的。转录因子PHR1,也可能是PHL1,是PSR和免疫反应的整合因子,如PHR1和PHR1;phl1突变株对卵菌和病原菌的抗性较强。PSR与植物免疫之间的联系似乎不仅受到周围微生物组的调节,还受到病原体的调节,这再次提出了有益菌与病原体之间的差异的问题。
从系统生物学到农作物保护
From Systems Biology to Crop Protection
理解微生物-宿主生物学的概念和分子进展对理解作物-微生物之间的关系越来越有帮助。对于新出现的引起红枝兰叶斑病的叶面真菌大麦病原菌Ramularia collo-cygni,McGrann等人(2016)使用装配的基因组草图预测大约1000种蛋白质的分泌物。基于植物细胞壁降解酶数量的减少和与几丁质识别规避相关基因的存在,他们提出,R. colo -cygni首先表现为植物内生菌,不引起植物疾病症状,然后植物转变为坏死营养阶段。了解这种动力学以及潜在的分子过程和信号将是系统生物学分析的一个重要方面。在另一项研究中,研究了四种纹孢菌在草上的宿主特异化。Rhynchosporia是一种半生物营养性真菌病原体,在寄主叶片细胞间基质中生长相对缓慢,无明显症状。Penselin等(2016)发现来自R. commune的6个特异性效应蛋白似乎负责稳定生物营养生长阶段,有利于坏死营养破坏阶段,因此为治疗提供了线索。在一项结合多组学方法的引人注目的研究中,研究了有益微生物对单子叶植物生物量增加和对生物和非生物胁迫的更高耐受性的影响。Fiorilli等(2018)利用表型分析、转录组学、分子和代谢组学方法研究了小麦病原菌半透黄单胞菌、保护性共生体AM真菌与宿主之间的三向相互作用。他们提出了一个两步走的方法来赋予黄单胞菌对AM-处理小麦的抗性,首先,在AM-处理过的植物的根和叶中发生了广谱防御(BSD)反应的激活,第二,在细菌感染时切换到病原体特异性防御(PSD),最终导致对抗病原体的保护效应。
前景:为可持续精准农业量身定制微生物组
Perspective: Tailored Microbiomes for Sustainable Precision Agriculture
多种多样的抗压能力使有益微生物成为农业生产可持续集约化有吸引力的工具。在新兴的大数据驱动的精准农业中,作物健康不断受到远程监控,有针对性的益生菌处理可能在指定的时间和地点得到精确应用。为了实现这一愿景,有必要培育出能够在不增加病原体易感性的情况下,从混合的有益微生物中获得最佳收益的品种。因此,深入了解微生物与宿主的相互作用、它们的遗传决定因素以及对其他植物生长参数的影响是必要的(图2)。Castrillo等人(2017)揭示的植物营养应激反应、免疫系统功能和微生物组装配之间的联系可能只是冰山一角,许多令人兴奋的机制仍有待发现。
图2. 在植物根际和叶际中复杂多样的有机体间相互作用的示意图
有益菌用绿色表示,真菌和致病菌用红色表示,共生细菌为灰色,丛枝菌根真菌为蓝色,其他有益真菌为黄色。相应颜色的箭头表示文本中描述的已知交互作用。右边的插图表示主图像中小帧的放大倍数。
同样重要的是微生物制剂,它们能够定殖于生长在自然土壤中作物的根际。因此,控制土壤微生物组需要了解微生物组动力学以及控制微生物组的植物机制。在益生菌制剂的开发、多品种栽培与同步、以及在田间合成群落的传递等方面也存在一些实际问题。
从战略上讲,了解参考生物体中宿主与微生物的兼容性,将有助于将这些见解应用于作物和潜在遗传学的鉴定上。一旦在作物中确定了基因的决定因素,益生菌的能力就可以成为育种者的目标。威胁农业生产力的非生物和生物胁迫条件可以通过在田间施用益生菌混合体加以抵消。由于微生物-宿主相互作用的复杂性,系统生物学必须在理解这些复杂的有机体间的关系方面发挥重要作用。
Published: May 22, 2019
编译:马腾飞 南京农业大学
责编:刘永鑫 中科院遗传发育所
猜你喜欢
- 10000+: 菌群分析
宝宝与猫狗 提DNA发Nature 实验分析谁对结果影响大 Cell微生物专刊 肠道指挥大脑 - 系列教程:微生物组入门 Biostar 微生物组 宏基因组
- 专业技能:生信宝典 学术图表 高分文章 不可或缺的人
- 一文读懂:宏基因组 寄生虫益处 进化树
- 必备技能:提问 搜索 Endnote
- 文献阅读 热心肠 SemanticScholar Geenmedical
- 扩增子分析:图表解读 分析流程 统计绘图
- 16S功能预测 PICRUSt FAPROTAX Bugbase Tax4Fun
- 在线工具:16S预测培养基 生信绘图
- 科研经验:云笔记 云协作 公众号
- 编程模板: Shell R Perl
- 生物科普: 肠道细菌 人体上的生命 生命大跃进 细胞暗战 人体奥秘
写在后面
为鼓励读者交流、快速解决科研困难,我们建立了“宏基因组”专业讨论群,目前己有国内外5000+ 一线科研人员加入。参与讨论,获得专业解答,欢迎分享此文至朋友圈,并扫码加主编好友带你入群,务必备注“姓名-单位-研究方向-职称/年级”。技术问题寻求帮助,首先阅读《如何优雅的提问》学习解决问题思路,仍末解决群内讨论,问题不私聊,帮助同行。
![]()
学习扩增子、宏基因组科研思路和分析实战,关注“宏基因组”
![]()
![]()
点击阅读原文,跳转最新文章目录阅读
https://mp.weixin.qq.com/s/5jQspEvH5_4Xmart22gjMA